
分析 A中仅含有O、K、Fe三种元素,在常温和干燥的条件下化合物A可以稳定的存在,但它在水溶液中不稳定,一段时间后转化为红褐色沉淀,同时产生一种气体单质,该红褐色沉淀为Fe(OH)3;可推知A含有Fe元素.A的化合物用硫酸溶解,再加入加KOH,生成沉淀灼烧得到红棕色固体粉末1.60g为氧化铁,由铁元素守恒可知,3.96g化合物A含铁:$\frac{1.6g}{160g/mol}$×2=0.02mol,不含结晶水的盐10.44g为硫酸钾,3.96g化合物A中含钾:$\frac{10.44g}{1744g/mol}$×2-0.08mol=0.04mol,3.96g化合物A中含氧:$\frac{3.96g-0.02mol×56g/mol-0.04mol×39g/mol}{16g/mol}$=0.08mol,故钾、铁、氧的个数比为:0.04mol:0.02mol:0.08mol=2:1:4,故A的化学式为:K2FeO4;高铁酸钾与水反应生成氧气和Fe(OH)3、氢氧化钾,反应方程式为4K2FeO4+10H2O=4Fe(OH)3+8KOH+3O2↑,据此解答.
解答 解:中仅含有O、K、Fe三种元素,在常温和干燥的条件下化合物A可以稳定的存在,但它在水溶液中不稳定,一段时间后转化为红褐色沉淀,同时产生一种气体单质,该红褐色沉淀为Fe(OH)3;可推知A含有Fe元素.A的化合物用硫酸溶解,再加入加KOH,生成沉淀灼烧得到红棕色固体粉末1.60g为氧化铁,由铁元素守恒可知,3.96g化合物A含铁:$\frac{1.6g}{160g/mol}$×2=0.02mol,不含结晶水的盐10.44g为硫酸钾,3.96g化合物A中含钾:$\frac{10.44g}{1744g/mol}$×2-0.08mol=0.04mol,3.96g化合物A中含氧:$\frac{3.96g-0.02mol×56g/mol-0.04mol×39g/mol}{16g/mol}$=0.08mol,故钾、铁、氧的个数比为:0.04mol:0.02mol:0.08mol=2:1:4,故A的化学式为:K2FeO4.
(1)由上述分析可知,A的化学式为:K2FeO4;高铁酸钾与水反应生成氧气和Fe(OH)3、氢氧化钾,反应方程式为4K2FeO4+10H2O=4Fe(OH)3+8KOH+3O2↑,
故答案为:K2FeO4;4KFeO4+10H2O=4Fe(OH)3↓+3O2↑+8KOH;
(2)化合物A可作为一种“绿色高效多功能”水处理剂,可由FeCl3和KClO在强碱性条件下反应制得,其反应的离子方程式为:2Fe3++3ClO-+10OH-=2FeO42-+3Cl?+5H2O 或2Fe(OH)3+3ClO-+4OH-=2FeO42-+3Cl?+5H2O,
故答案为:2Fe3++3ClO-+10OH-=2FeO42-+3Cl?+5H2O 或2Fe(OH)3+3ClO-+4OH-=2FeO42-+3Cl?+5H2O;
(5)A.高铁酸钾在碱性条件下生成,而醋酸钠溶液呈碱性,故A正确;
B.高铁酸钾在水溶液中不稳定,与酸反应,故B错误;
C.铁离子与反应生成的KOH反应,使高铁酸钾在水溶液中更不稳定,故C错误;
D.高铁酸钾在碱性条件下生成,故D正确;
故答案为:AD.
点评 本题考查无机物推断,属于计算型推断,综合考查学生阅读题目获取信息的能力、计算能力、设计实验能力等,题目难度较大,需要学生具有扎实的基础知识与灵活运用知识解决问题的能力.


科目:高中化学 来源: 题型:解答题
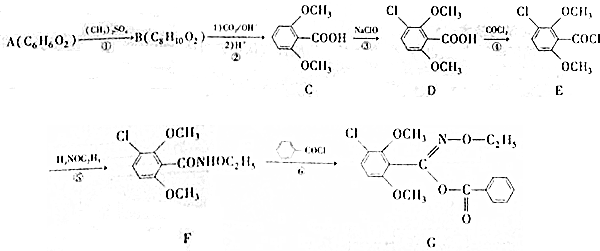
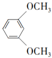 ;⑤的反应类型为取代反应.
;⑤的反应类型为取代反应.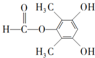 、
、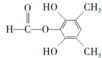 .
. 为原料制备
为原料制备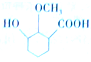 的合成路线
的合成路线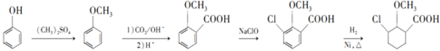
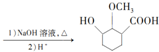
 (无机试剂可任选)
(无机试剂可任选)查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
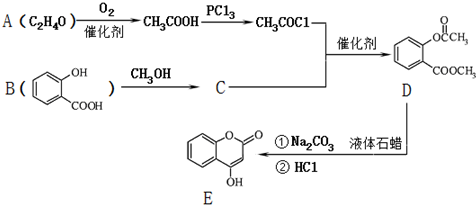
 .
. ;
;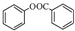 )是一种重要的有机合成中间体.试写出以苯、甲苯为原料制取该化合物的合成路线流程图(无机原料任选).
)是一种重要的有机合成中间体.试写出以苯、甲苯为原料制取该化合物的合成路线流程图(无机原料任选).查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 该物质属于盐类 | |
| B. | 该物质是Al(OH)3和Na2CO3的混合物 | |
| C. | 1mol NaAl(OH)2CO3最多可消耗3mol H+ | |
| D. | 该药剂不适合于胃溃疡患者服用 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
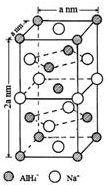 氢化铝钠(NaAlH4)是一种新型轻质储氢材料,掺入少量Ti的NaAlH4在150℃时释氢,在170℃、15.2MPa条件下又重复吸氢.NaAlH4可由AlCl3和NaH在适当条件下合成.NaAlH4的晶胞结构如右图所示.
氢化铝钠(NaAlH4)是一种新型轻质储氢材料,掺入少量Ti的NaAlH4在150℃时释氢,在170℃、15.2MPa条件下又重复吸氢.NaAlH4可由AlCl3和NaH在适当条件下合成.NaAlH4的晶胞结构如右图所示.  .
. 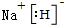 .
.  (标明配位键).
(标明配位键). 查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 要完成实验需称取10.6gNa2CO3•10H2O晶体 | |
| B. | 定容后把容量瓶倒转摇匀,发现液面低于刻度,再补充几滴水至刻度线,会导致溶液浓度偏高 | |
| C. | 配制时若容量瓶不干燥,含有少量蒸馏水会导致浓度偏低 | |
| D. | 定容时俯视刻度线会导致浓度偏高 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 等物质的量浓度的各溶液pH关系为:pH(Na2CO3)>pH(NaCN)>pH(CH3COONa) | |
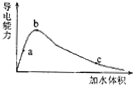
| B. | 冰醋酸中逐滴加水,则溶液的导电性、醋酸的电离程度、pH均先增大后减小 | |
| C. | 混合溶液中含有等物质的量的Na2CO3和NaHCO3,则一定存在c(Na+)+c(H+)═c(OH-)+c(HCO3-)+2c(CO32-) | |
| D. | a mol/LHCN溶液与b mol/LNaOH溶液等体积混合后,所得溶液中c(Na+)>c(CN-),则b一定大于a |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com