
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 18g |
| 18g/mol |
| 1 |
| 2 |
| 1 |
| 2 |
| 22.4L |
| x |
| 282.8KJ |
| 582.1kJ |
| 46.1L |
| 116.8L |


科目:高中化学 来源: 题型:
| A、在等浓度溶液中滴加澄清石灰水观察是否有沉淀产生 |
| B、在少量固体样品中滴入几滴水,触摸试管看是否有温度变化 |
| C、在等浓度溶液中滴入几滴酚酞比较溶液颜色深浅 |
| D、取少量的固体试样加热后称量质量变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 根据已有知识判定下列说法不正确的是
根据已有知识判定下列说法不正确的是| A、它可使KMnO4溶液褪色 |
| B、它可跟银氨溶液生成银镜 |
| C、它可使溴水褪色 |
| D、它被催化加氢后最终产物的化学式为C10H20O |
查看答案和解析>>
科目:高中化学 来源: 题型:
- 3 |
| A、②⑥⑧ | B、④⑥⑧ |
| C、②④⑦⑧ | D、④⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:
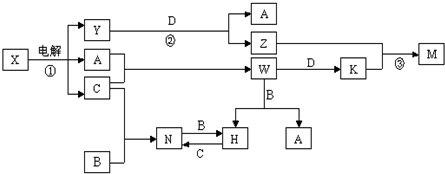
查看答案和解析>>
科目:高中化学 来源: 题型:
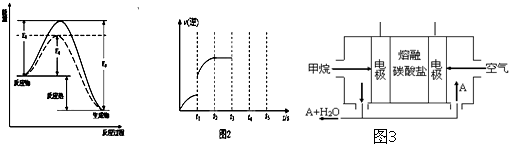
查看答案和解析>>
科目:高中化学 来源: 题型:
 (1)下列7种物质:
(1)下列7种物质:查看答案和解析>>
科目:高中化学 来源: 题型:
 石油是工业的血液,被誉为“黑色的金子”,是重要的能源资源和化工原料.
石油是工业的血液,被誉为“黑色的金子”,是重要的能源资源和化工原料.| 催化剂 |
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| A、①和③ | B、②和④ |
| C、④ | D、以上都不对 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com