
【题目】(加试题)氯化亚铜常用作有机合成工业中的催化剂,为白色晶体,不溶于乙醇,微溶于水,易溶于浓盐酸形成络合离子([CuCl2]-)。受潮露置空气中迅速氧化成碱式盐。实验室用下列流程制备:
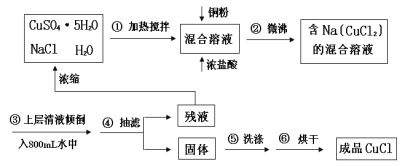
已知:Na[CuCl2](易电离,溶液无色) ![]() NaCl+CuCl↓(白色沉淀)。
NaCl+CuCl↓(白色沉淀)。
请回答以下问题:
(1)写出实验室制取Na[CuCl2]的离子方程式__________
(2)判断步骤②反应完全的现象是____________
(3)步骤③的目的是__________________________________。
(4)步骤④有关抽滤操作,下列说法正确的是_______
A. 选择抽滤主要是为了加快过滤速度,得到较干燥的沉淀
B. 在吸滤瓶和抽气泵之间应连接一个安全瓶,吸滤瓶应与安全瓶的长导管相接
C. 抽滤时不宜过滤胶状沉淀,否则易在滤纸上形成一层密实的沉淀
D. 洗涤沉淀时,应关小水龙头,使洗涤剂缓缓通过沉淀物
(5)定量 称取1.850g CuCl样品(杂质不参与反应),溶于一定量的0.5000mol·L-1FeCl3溶液中,加水稀释至200mL得到溶液,取20.00mL 用0.1000mol·L-1的Ce(SO4)2溶液滴定到终点,消耗18.00mLCe(SO4)2 。
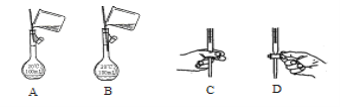
①此实验涉及溶液配制与定量滴定的基本操作中,其中合理的是___________;
②有关反应式:Fe3++CuCl=Fe2++Cu2++Cl- Ce4++Fe2+=Fe3++Ce3+则样品中CuCl的质量分数____________。
【答案】Cu2+ + 4Cl- + Cu = 2[Cu Cl2]- 反应溶液由蓝色转变成无色透明时为止 使Na[CuCl2]转化为CuCl AD BC 96.81%
【解析】
(1)硫酸铜、浓盐酸和铜反应生成Na[CuCl2]。
(2)铜离子为蓝色,Na[CuCl2]为无色,如果步骤②反应完全,则溶液中不存在铜离子的颜色。
(3)步骤③的目的是使Na[CuCl2]转化为CuCl。
(4)A.颗粒太小的沉淀易在滤纸上形成一层密实的沉淀,溶液不易透过,则选择抽滤主要是为了加快过滤速度,得到较干燥的沉淀。
B.在吸滤瓶和抽气泵之间应连接一个安全瓶,吸滤瓶应与安全瓶的短导管相接,否则易使水进入安全瓶。
C.胶状沉淀易透过滤纸而不易采用抽滤方法。
D.在洗涤沉淀时,应关小水龙头,使洗涤剂缓缓通过沉淀物,防止沉淀溶解而造成损失。
(5)①溶液配制时,向容量瓶中转移溶液时,溶液不能沾到容量瓶刻度线上面,在打开酸式滴定管活塞时,要把活塞放在手心的位置,手指从另一侧打开活塞。
②Fe3++CuCl=Fe2++Cu2++Cl- ,Ce4++Fe2+=Fe3++Ce3+可得到Ce4+~Fe2+~CuCl。
(1)硫酸铜、浓盐酸和铜反应生成Na[CuCl2],离子方程式为:Cu2+ + 4Cl- + Cu = 2[Cu Cl2]- ,故答案为:Cu2+ + 4Cl- + Cu = 2[Cu Cl2]-。
(2)铜离子为蓝色,Na[CuCl2]为无色,如果步骤②反应完全,则溶液中不存在铜离子的颜色,所以判断反应完全的现象是反应溶液由蓝色转变成无色透明时为止,故答案为:反应溶液由蓝色转变成无色透明时为止。
(3)步骤③的目的是使Na[CuCl2]转化为CuCl,故答案为:使Na[CuCl2]转化为CuCl。
(4)A.颗粒太小的沉淀易在滤纸上形成一层密实的沉淀,溶液不易透过,则选择抽滤主要是为了加快过滤速度,得到较干燥的沉淀,故A正确;
B.在吸滤瓶和抽气泵之间应连接一个安全瓶,吸滤瓶应与安全瓶的短导管相接,否则易使水进入安全瓶,故B错误;
C.胶状沉淀易透过滤纸而不易采用抽滤方法,故C错误;
D.在洗涤沉淀时,应关小水龙头,使洗涤剂缓缓通过沉淀物,防止沉淀溶解而造成损失,故D正确。
故选AD。
(5)①溶液配制时,向容量瓶中转移溶液时,溶液不能沾到容量瓶刻度线上面,在打开酸式滴定管活塞时,要把活塞放在手心的位置,手指从另一侧打开活塞,故选BC。
②Fe3++CuCl=Fe2++Cu2++Cl- ,Ce4++Fe2+=Fe3++Ce3+可得到Ce4+~Fe2+~CuCl,n(Ce4+)=0.1000molL-1×0.018L=0.0018mol,则1.850g样品中含有n(CuCl)=10×0.0018mol=0.018mol,质量m(CuCl)=0.018mol×99.5g/mol=1.791g,因此样品中CuCl的质量分数=(1.791g/1.850g)×100%≈96.81%,故答案为:96.81%。


科目:高中化学 来源: 题型:
【题目】现有四瓶失去标签的无色溶液,可能是CaCl2、AgNO3、HCl、Na2CO3中的其中一种,为了确定具体成分,随意将四瓶溶液标记为A、B、C、D后,进行了下列四组实验。
实验顺序 | 实验内容 | 实验现象 |
① | A+B | 无明显现象 |
② | B+D | 有气体放出 |
③ | B+C | 有沉淀生成 |
④ | A+D | 有沉淀生成 |
根据表中实验现象回答下列问题:
(1)A、B、C、D分别对应的溶质化学式为____________、___________、___________、___________;
(2)请分别写出上述实验②和③的离子方程式:
②________________________________________________________;
③________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)配平该反应的化学方程式:___
① FeSO4+ KMnO4+ H2SO4= K2SO4+ MnSO4+ Fe2(SO4)3+ H2O
②该反应中的氧化剂是___,氧化产物是____。
③若消耗3.16gKMnO4,则该反应转移的电子数目为____。
(2)已知反应:①Cl2+2KBr=2KCl+Br2,②2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,③Br2+K2S=2KBr+S。
①下列说法正确的是__。
A.上述三个反应都有单质生成,所以都是置换反应
B.氧化性由强到弱顺序为KMnO4>Cl2>Br2>S
C.反应②中还原剂与氧化剂的物质的量之比为8:1
D.反应③中1mol还原剂被氧化则转移电子的物质的量为2mol
②用单线桥法标出反应②中电子转移的方向和数目___。
2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下向10mL 0.1 mol·L-1 NaOH溶液中加入0.1 mol·L-1的一元酸HA溶液,pH的变化曲线如图所示。下列说法不正确的是
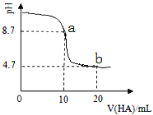
A. pH=4.7时,2c(Na+) = c(A-)+ c(HA)
B. 一元酸HA为弱酸
C. a、b两点所示溶液中水的电离程度不同,且a点比b点电离程度大
D. a点所示溶液中c(A-)>c(Na+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有机反应的化学方程式正确的是
A.CH3CH2Br+NaOH![]() CH2=CH2↑+NaBr+H2O
CH2=CH2↑+NaBr+H2O
B.2![]() +3Br2→2
+3Br2→2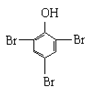 ↓
↓
C.n CH2=CH—CH3 ![]()
![]()
D.![]() +Br2
+Br2![]()
![]() +HBr
+HBr
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸晶体(H2C2O4·2H2O)加热到170 ℃以上分解,草酸的钠盐和钾盐易溶于水,而其钙盐难溶于水。某校化学兴趣小组欲探究草酸晶体受热分解的产物,设计了如下实验装置。
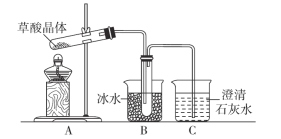
回答下列问题:
(1)C中的现象是___________。
(2)B装置的作用______________。
(3)下列说法不正确的是______________。
A.装置连接完成后,需先检查装置的气密性,然后加入药品
B.反应生成的CO2能完全被C中石灰水吸收
C.由实验可知,草酸分解只生成H2O和CO2
D.盛装草酸晶体的大试管应开口略向下倾斜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为探究某物质X(仅含两种元素)的组成和性质,设计并完成如下实验。(气体体积已转化为标况体积)
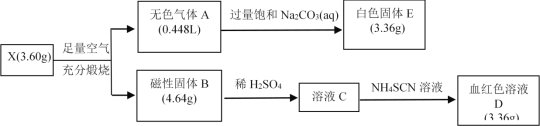
请回答下列问题:
(1)X的化学式为___________。
(2)A的结构式为________,E属于_______化合物(填离子或共价)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子形式存在(Cl2可与碘离子反应生成碘单质)。实验室从海藻中提取碘的流程如下:
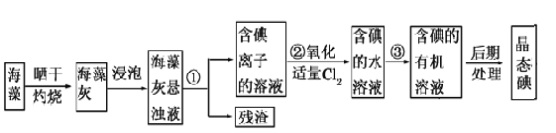
(1)指出提取碘的过程中有关实验操作的名称:③______;
(2)为使海藻灰中碘离子转化为碘的有机溶液,实验室里有漏斗、烧杯、玻璃棒、 集气瓶、酒精灯、导管、圆底烧瓶、石棉网以及必要的夹持装置、物品,尚缺少的玻璃仪器是_______。
(3)从含碘的有机溶剂中提取碘和回收有机溶剂,还需要经过蒸馏。指出图中所示的实验装置中的错误之处:
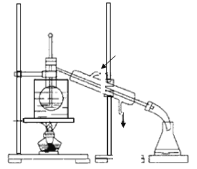
①______,
②______,
③______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用98%的浓硫酸(密度为1.84 g/cm3 )配制100 mL l mol/L的稀硫酸。现给出下列仪器(配制过程中可能用到):①100 mL量筒 ②10 mL量筒 ③50 mL烧杯 ④托盘天平 ⑤100 mL容量瓶 ⑥胶头滴管 ⑦玻璃棒,按使用仪器的先后顺序排列正确的是.( )
A.④③⑦⑤⑥;B.②⑤⑦⑥;C.①③⑤⑥⑦;D.②⑥③⑦⑤⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com