

分析 (1)如图1所示:与电源正极相连的C1为阳极失电子发生氧化反应,与电源负极相连的C2为阴极得电子发生还原反应,据此分析解答;
(2)某同学一不小心,将一段铜棒掉入CuSO4溶液中,仍然完成电解CuSO4溶液实验,如图2所示,C1、C2均为碳棒,发现铜棒A端变粗,B端变细,说明A端为阴极得电子发生还原反应,B端为为阳极失电子发生氧化反应,根据电路中电子守恒计算.
解答 解:(1)①若C1、C2均为碳棒,则用惰性电极电解硫酸铜溶液时,阳极上氢氧根离子放电生成氧气、阴极上铜离子放电生成Cu,化学方程式为2CuSO4+2H2O$\frac{\underline{\;电解\;}}{\;}$2Cu+O2↑+2H2SO4,故答案为:2CuSO4+2H2O$\frac{\underline{\;电解\;}}{\;}$2Cu+O2↑+2H2SO4;
②若C1为铜棒,C2为碳棒,则与电源正极相连的C1为阳极铜失电子发生氧化反应,所以发生的现象为铜棒变细,故答案为:铜棒变细;
③工业电解精炼铜,阳极为粗铜,阴极为精铜,则C1为阳极是粗铜,故答案为:粗铜;
(2)①如图2所示,C1、C2均为碳棒,则与电源正极相连的C1为阳极氢氧根离子放电生成氧气,则电极反应式40H--4e-═O2↑+2H2O,故答案为:40H--4e-═O2↑+2H2O;
②铜棒A端变粗,则A端为阴极得电子发生还原反应,阴极反应为Cu2++2e-═Cu,所以电路中电子守恒,若标况下C1产生3.36L气体,则铜棒A端增重$\frac{3.36L}{22.4L/mol}$×2×64g/mol=9.2g,故答案为:9.2.
点评 本题考查电解池的工作原理,题目难度不大,本题注意电极反应式的书写以及串联电解池转移电子相等的特点.


 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 两种物质反应,不管怎样书写化学方程式,平衡常数不变 | |
| B. | 水的离子积常数Kw与温度无关 | |
| C. | 溶液中c(Ag+)•c(Cl-)大于Ksp时,将产生AgCl | |
| D. | 难溶电解质AB2饱和溶液中,c(A2+)=xmol/L,c(B-)=ymol/L,则Ksp值为xy |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
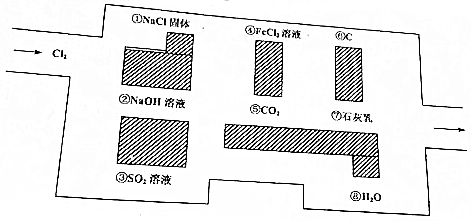
| A. | 分别与同浓度的稀盐酸反应 | B. | 分别加入NaOH溶液 | ||
| C. | 分别加入石灰水 | D. | 溶于水,比较其溶解性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 高纯度的晶体硅可以制备晶体管等半导体、电脑芯片和光导纤维 | |
| B. | PM 2.5是指大气中直径接近2.5×10-6m的颗粒物,它分散在空气中形成胶体 | |
| C. | 受强碱腐蚀致伤时,应先用大量水冲洗,再用2%醋酸溶液或饱和硼酸溶液洗,最后用水冲洗,并视情况作进一步处理 | |
| D. | NH4F水溶液中含有HF,因此NH4F溶液不能存放于玻璃试剂瓶中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 充电时,Ni(OH)2为阳极 | |
| B. | 放电时,Fe为正极,Ni2O3为负极 | |
| C. | 该新型蓄电池的电解质溶液呈碱性 | |
| D. | 充电时,阴极反应式为Fe(OH)2+2e-=Fe+2OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原电池能将全部化学能转变为电能 | |
| B. | 原电池的负极失电子,发生还原反应 | |
| C. | 原电池工作时,其负极不断产生电子并经外电路流向正极 | |
| D. | 原电池的电极一定要由两种不同的金属组成 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com