
| A. | NaOH、NaClO、Na2O | B. | HCl、HClO、MgCl2 | ||
| C. | NH3、CO2、Na2O2 | D. | C2H6、H2O2、C2H5OH |
分析 一般来说,活泼金属和活泼非金属元素之间易形成离子键,非金属元素之间易形成共价键,离子化合物中含有离子键,可能含有共价键,共价化合物中只含共价键,据此分析解答.
解答 解:A.NaOH和NaClO中有共价键和离子键,而Na2O中只有离子键,故A错误;
B.氯化氢和次氯酸中只含共价键,氯化镁中只含离子键,故B错误;
C.氨气、二氧化碳中只含共价键,过氧化钠中含有共价键和离子键,故C错误;
D.C2H6、H2O2、C2H5OH中都只含共价键,故D正确;
故选D.
点评 本题考查了化学键的判断,明确离子键和共价键的区别是解本题关键,根据定义来分析解答,注意不能单纯根据元素是否是金属判断离子键,如氯化铝中只含共价键.


科目:高中化学 来源: 题型:选择题
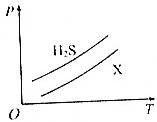 如图所示,表示1 g H2S与1g X气体在相同容积的密闭容器中压强(p)与温度(T)的关系,则X气体可能是( )
如图所示,表示1 g H2S与1g X气体在相同容积的密闭容器中压强(p)与温度(T)的关系,则X气体可能是( )| A. | N2 | B. | CH4 | C. | NO | D. | SO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
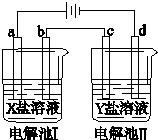
| A. | 若a是Zn,X是ZnSO4,则构成电镀池 | |
| B. | 当Y是硫酸铜,要构成电解精炼铜,则c是粗铜,d是精铜,且电解过程中硫酸铜溶液浓度不变 | |
| C. | 当X是CuCl2,Y是Na2SO4,用惰性电极电解,在I、II电解池中产生的气体物质的量之比为2:3 | |
| D. | 若去除电源,把b和c换成盐桥,可能构成原电池 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | Cl2、Br2分别与H2反应 | 比较氯、溴的非金属性强弱 |
| B | MgCl2、AlCl3溶液中分别通入NH3 | 比较镁、铝的金属性强弱 |
| C | Na2CO3溶液中加入稀H2SO4 | 比较碳、硫的非金属性强弱 |
| D | Fe、Cu分别与盐酸反应 | 比较铁、铜的金属性强弱 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酸性:HClO4<HBrO4<HIO4 | B. | 碱性:Ba(OH)2>Ca(OH)2>Mg(OH)2 | ||
| C. | 稳定性:PH3>H2S>HCl | D. | 氧化性:I2>Br2>Cl2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com