
分析 (1)根据A分子中碳、氢元素的质量分数计算出氧元素的质量分数,然后根据A的相对分子质量范围确定分子中O原子取值范围,进而确定O原子数目,结合氧元素质量分数确定A的相对分子质量;
(2)A分子中C、H原子个数比=1:2,可设A的分子式为(CH2)nOx,x由(1)计算得到,根据A的相对分子质量计算出n的值,确定A的分子式;
(3)A可与碳酸钠溶液反应生成二氧化碳,说明A分子中含有羧基,结合A的核磁共振氢谱为5组峰,且面积比为2:2:2:1:1确定其结构简式.
解答 解:(1)A分子中C和H的质量分数之和为53.8%,则氧元素的质量分数为:1-53.8%=46.2%,当相对分子质量为110时,A中最多含有氧原子个数为:$\frac{110×46.2%}{16}$≈3.2,当相对分子质量为100时,最少含有氧原子数目为:$\frac{100×46.2%}{16}$≈2.9,所以A中含有氧原子数为3,A的相对分子量为:$\frac{16×3}{46.2%}$≈104,
故答案为:3;104;
(2)A分子中C、H原子个数比=1:2,可设A的分子式为:(CH2)nO3,则14n+16×3=104,解得:n=4,所以A的分子式为:C4H8O3,
故答案为:C4H8O3;
(3)A可与碳酸钠溶液反应生成二氧化碳,说明A分子中含有羧基,由于A的分子式的不饱和度为2,则除了羧基外其它结构都为单键,A的核磁共振氢谱为5组峰,且面积比为2:2:2:1:1,则A的结构简式为:HOCH2CH2CH2COOH,
故答案为:HOCH2CH2CH2COOH.
点评 本题考查有机物分子式与结构式的确定,关键是计算确定A分子中氧原子数目,注意掌握常见有机物结构与性质,试题培养了学生的分析能力及化学计算能力.


科目:高中化学 来源: 题型:选择题
| A. | NH4+、Mg2+、SO42-、Cl- | B. | Ba2+、K+、I-、NO3- | ||
| C. | Al3+、Cu2+、SO42-、Cl- | D. | Na+、Ca2+、Cl-、AlO2- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe片与稀H2SO4的反应 | B. | Ba(OH)2•8H2O和NH4Cl反应 | ||
| C. | 盐酸和氢氧化钠的反应 | D. | 镁条在空气中的燃烧 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{53}^{131}$I是一种核素 | |
| B. | ${\;}_{53}^{131}$I核内的中子数为78 | |
| C. | ${\;}_{53}^{131}$I是碘的一种同素异形体 | |
| D. | ${\;}_{53}^{131}$I位于元素周期表中第5周期ⅦA族 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
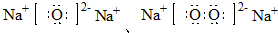 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③ | B. | ③ | C. | ①④ | D. | ①②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 7.8gNa2O2固体中含离子总数为0.4NA | |
| B. | 2.0gH218O和D216O的混合物中所含中子数为NA | |
| C. | 常温下,22.4LCH4中含C-H共价键数为4NA | |
| D. | 标准状况下,11.2LCCl4中含有的分子数为0.5NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com