
| A. | ls22s22p63s23p3 | B. | 1s22s22p3 | C. | 1s22s2sp2 | D. | 1s22s22p63s23p4 |
 全优点练单元计划系列答案
全优点练单元计划系列答案科目:高中化学 来源: 题型:选择题
 在一定温度和压强下,使Mg和Zn分别与等浓度、等体积的过量稀盐酸反应,产生气体的体积(V)与反应时间(t)的关系如图所示.下列叙述正确的是( )
在一定温度和压强下,使Mg和Zn分别与等浓度、等体积的过量稀盐酸反应,产生气体的体积(V)与反应时间(t)的关系如图所示.下列叙述正确的是( )| A. | 曲线a代表的是Zn的反应,曲线b代表的是Mg的反应 | |
| B. | 两个反应分别在2min、3min时达到化学平衡 | |
| C. | Mg和Zn的反应速率之比为3:2 | |
| D. | 用Fe代替Zn,其他条件不变,绘出的图象完全相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯酚、苯乙醇和苯乙酸都可以与钠反应生成氢气 | |
| B. | 受羟基的影响,苯环上的氢变得活泼,苯酚的溴代比苯的溴代更容易 | |
| C. | 用酸性高锰酸钾溶液可以鉴别苯和甲苯 | |
| D. | 纤维素、蔗糖、葡萄糖在一定条件下都可发生水解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①⑤⑥⑦ | B. | ②③④⑧⑨⑩ | C. | ①②⑤⑥⑦ | D. | ①⑤⑥⑦⑨⑩ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
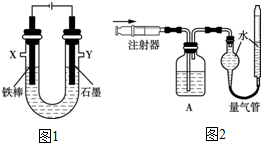
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
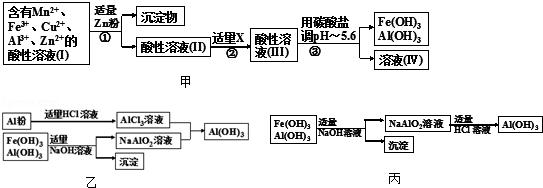
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 实验①中产生的气体为氨气,并可得原溶液中c(NH4+)=0.2 mol•L-1 | |
| B. | 实验③中的白色沉淀中一定有BaSO4,无BaCO3 | |
| C. | 原溶液中一定有K+,且c(K+)=0.4 mol•L-1 | |
| D. | 若要判断原溶液中是否有Cl-,无需另外设计实验验证 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
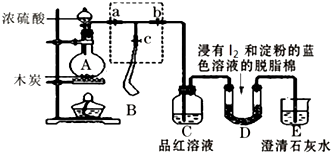
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验目的 | 实验操作 |
| A | 称取2.0gNaOH固体 | 先在托盘上各放一张滤纸,然后在右盘上添加2g砝码,左盘上添加NaOH固体 |
| B | 配制FeCl3溶液 | 将FeCl3固体溶解于适量蒸馏水 |
| C | 检验溶液中是否含有NH4+ | 取少量试液于试管中,加入NaOH溶液并加热,用湿润的红色石蕊试纸检验产生的气体 |
| D | 验证铁的吸氧腐蚀 | 将铁钉放入试管中,用盐酸浸没 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com