
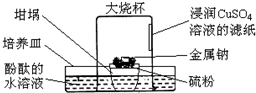
 倒置的坩埚盖子上放入硫粉,在硫粉中央放一小块钠,按图示搭建装置.用胶头滴管向金属钠滴加一滴水,立即倒扣上大烧杯,发现坩埚盖子内火星四溅,烧杯内出现大量白烟,下列说法错误的是( )
倒置的坩埚盖子上放入硫粉,在硫粉中央放一小块钠,按图示搭建装置.用胶头滴管向金属钠滴加一滴水,立即倒扣上大烧杯,发现坩埚盖子内火星四溅,烧杯内出现大量白烟,下列说法错误的是( )| A. | 水是钠与硫反应的催化剂 | B. | 酚酞的水溶液变红色 | ||
| C. | 钠与硫的反应是放热反应 | D. | 滤纸逐渐变黑 |
分析 倒置的坩埚盖子上放入硫粉,在硫粉中央放一小块钠,用胶头滴管向金属钠滴加一滴水,钠与水反应生成氢氧化钠和氢气,反应放热,立即倒扣上大烧杯,放出的热量引发钠与硫剧烈反应生成硫化钠,现象为坩埚盖子内火星四溅,烧杯内出现大量白烟,据此分析解答.
解答 解:A.钠与水反应生成氢氧化钠和氢气,反应放热,放出的热量引发钠与硫的反应,所以水不是催化剂,故A错误;
B.硫化钠为强碱弱酸盐,溶于水后,发生水解使溶液显碱性,所以酚酞的水溶液变红色,故B正确;
C.钠与硫反应引发后,不需要加热,就能继续反应说明其为放热反应,故C正确;
D.硫化钠与硫酸铜反应生成硫化铜黑色固体,故D正确;
故选:A.
点评 本题考查了钠与硫反应的实验,明确钠和硫的性质是解题关键,题目难度不大.


科目:高中化学 来源: 题型:选择题
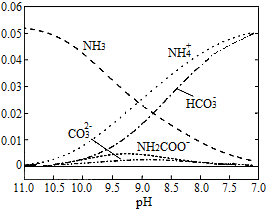 ,
,| A. | 在pH=8.0 时,c(NH4+)>c(HCO3-)>c(NH2COO-)=c(CO32-) | |
| B. | 随着C02的不断通入,Kw不变,但是水的电离受到促进 | |
| C. | 在溶液中pH不断降低的过程中,最终产物中含有NH2COO- | |
| D. | D、随着C02的通入,$\frac{c(O{H}^{-})}{c(N{H}_{3}{H}_{2}O)}$ 不断减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
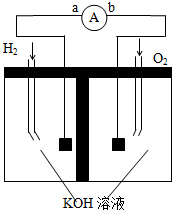 氢氧燃料电池是符合绿色化学理念的新型电池,图为电池示意图,据此回答下列问题
氢氧燃料电池是符合绿色化学理念的新型电池,图为电池示意图,据此回答下列问题查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | MgO$\stackrel{HCl}{→}$MgCl2溶液$\stackrel{电解}{→}$Mg | |
| B. | CH≡CH$→_{催化剂△}^{HCl}$CH2=CHCl$→_{△}^{催化剂}$ | |
| C. | HCHO$\stackrel{O_{2}}{→}$HCOOH$→_{NaOH}^{CH_{2}OH}$HCOOCH3 | |
| D. | CH2═CH2$→_{催化剂△}^{O_{2}}$CH3CHO$→_{△}^{银氨溶液}$CH3COOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
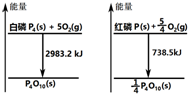
| A. | 白磷比红磷稳定 | |
| B. | 白磷燃烧产物比红磷燃烧产物稳定 | |
| C. | 1mol白磷转变为红磷放出2244.7kJ的热量 | |
| D. | 红磷燃烧的热化学方程式:4P(s)+5O2(g)→P4O10(s)+2954 kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
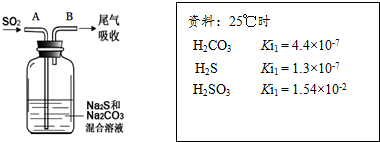
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 56(m-n)g | B. | 56(n-m)g | C. | 56ng | D. | 56(m-2n)g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com