
【题目】聚对苯二甲酸乙二醇酯(PET)俗称涤纶树脂,是一种重要的有机高分子材料。其结构为 。利用有机物A合成PET的路线如下图所示:
。利用有机物A合成PET的路线如下图所示:

已知:①![]() ;②
;② 。
。
根据题意回答下列问题:
(1)A的名称是_______,C所含官能团的名称是_______。
(2)由1,3-丁二烯可制备顺式聚1,3-丁二烯,写出顺式聚l,3-丁二烯的结构简式_______。
(3)A→D、B→C的反应类型分别为_______ 、_______。
(4)写出C+F→PET的化学反应方程式______________。
(5)G是F的同系物,其相对分子质量比F多28,G的核磁共振氢谱有三组峰,峰面积比为3:1:1,则符合该条件的G的同分异构体共有_____种。
(6)参照上述合成路线,以1,3-丁二烯为原料(无机试剂任选),设计制备丁苯橡胶( )的合成路线_______________。
)的合成路线_______________。
【答案】 乙烯 羟基 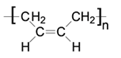 加成反应 取代反应(或水解反应)
加成反应 取代反应(或水解反应) 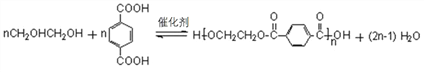 4
4 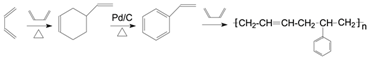
【解析】根据聚对苯二甲酸乙二醇酯(PET)的结构![]() 可知,C、F是乙二醇和,根据生成C和F的条件可知,C为乙二醇,F为对苯二甲酸,则B为1,2-二溴乙烷,A为乙烯;根据已知信息,乙烯与
可知,C、F是乙二醇和,根据生成C和F的条件可知,C为乙二醇,F为对苯二甲酸,则B为1,2-二溴乙烷,A为乙烯;根据已知信息,乙烯与![]() 反应生成D,D为
反应生成D,D为![]() ,E为对二甲苯。
,E为对二甲苯。
(1)根据上述分析,A为乙烯,C为乙二醇,所含官能团为羟基,故答案为:乙烯;羟基;
(2)由1,3-丁二烯可制备顺式聚1,3-丁二烯,顺式聚l,3-丁二烯的结构简式为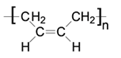 ,故答案为:
,故答案为: ;
;
(3)根据上述分析,A→D为加成反应、B→C为卤代烃的水解反应,属于取代反应,故答案为:加成反应;取代反应(或水解反应);
(4)C+F→PET的化学反应方程式为 ,故答案为:
,故答案为: ;
;
(5)G是F(![]() )的同系物,其相对分子质量比F多28,多2个甲基,G的核磁共振氢谱有三组峰,峰面积比为3:1:1,即6:2:2,则符合该条件的G的同分异构体有:
)的同系物,其相对分子质量比F多28,多2个甲基,G的核磁共振氢谱有三组峰,峰面积比为3:1:1,即6:2:2,则符合该条件的G的同分异构体有: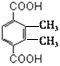 、
、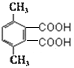 、
、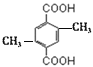 、
、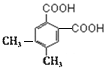 ,共4种,故答案为:4;
,共4种,故答案为:4;
(6)以1,3-丁二烯为原料制备丁苯橡胶( )。根据已知信息,首先需要制备苯乙烯,可以有2分子1,3-丁二烯发生加成反应生成
)。根据已知信息,首先需要制备苯乙烯,可以有2分子1,3-丁二烯发生加成反应生成![]() ,再由
,再由![]() 制备苯乙烯,最后苯乙烯与1,3-丁二烯发生加聚反应生成丁苯橡胶,合成路线为
制备苯乙烯,最后苯乙烯与1,3-丁二烯发生加聚反应生成丁苯橡胶,合成路线为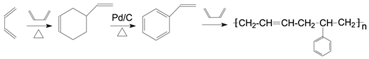 ,故答案为:
,故答案为: 。
。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示。已知Y、W的原子序数之和是Z的3倍,下列说法正确的是

A. 原子半径:X<Y<Z
B. 气态氢化物的稳定性:X>Z
C. 最高价氧化物对应水化物的酸性:Y>W
D. Z、W均可与Mg形成离子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随着材料科学的发展,金属钒及其化合物得到了越来越广泛的应用,并被誉为“合金维生素”。已知钒的原子序数为23,回答下列问题:
(1)钒被认为是一种稀土元素,广泛分散于各种矿物中,钾钒铀矿中的钒原子最外层已达到8 电子稳定结构,其化学式为K2H6U2V2O15(其中钒元素的化合价为+5价)。若用氧化物的形式表示,该化合物的化学式为:_______________________________。
(2)五氧化二钒是工业制造中的常用催化剂,如工业制硫酸中就利用五氧化二钒作催化剂。从含钒废催化剂中回收钒,传统的技术是“氧化焙烧法”,其具体流程为:
![]()
其中焙烧是将食盐和钒铅矿在空气中焙烧,这时矿石中所含的V2O5就转化为NaVO3,然后用水从烧结块中浸出NaVO3,再用稀硫酸酸化就得到V2O5的水合物,经过煅烧就可得到V2O5。
①配料在焙烧前磨碎的目的是_______________________。
②写出焙烧过程中V2O5发生反应的化学方程式:___________________________。
(3)测定钒含量的方法是先把钒转化成V2O5,V2O5在酸性溶液里转变成VO,再用盐酸、硫酸亚铁、草酸等测定钒。反应的化学方程式为:VO2++H2C2O4==VO++2CO2+H2O。若反应消耗0.9 g 草酸,参加反应的钒元素质量是_____g。
(4)以V2O5为催化剂,使SO2转化为SO3的反应如下:2SO2(g)+O2(g)![]() 2SO3(g)。某温度下,SO2的平衡转化率(a)与体系总压强(P)的关系如图所示。
2SO3(g)。某温度下,SO2的平衡转化率(a)与体系总压强(P)的关系如图所示。

根据图示回答下列问题:
①将2.0molSO2和1.0molO2置于10L密闭容器中,反应达平衡后,体系总压强为0.10MPa.该反应的平衡常数表达式为__________,等于______________。
②平衡状态由A变到B时,平衡常数K(A)______K(B)(填“>”、“<”或“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于化学电源的说法不正确的是( )
A.我们可以根据硫酸密度的大小来判断铅蓄电池是否需要充电
B.燃料电池是利用燃料和氧化剂之间的氧化还原反应,将化学能转化为热能,然后再转化为电能的化学电源
C.普通锌锰干电池中,发生氧化还原反应的物质大部分被消耗后,就不能再使用了
D.由Ag2O和Zn形成的碱性银锌纽扣电池,发生电化学反应时,Zn作为负极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质的性质与用途具有对应关系的是( )
A.NH4HCO3 受热易分解,可用作化肥
B.稀硫酸具有酸性,可用于除去铁锈
C.NH3 极易溶于水,可用作制冷剂
D.Al2O3 具有两性,可用于电解冶炼铝
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从能源开发、环境保护、资源利用等角度分析,下列说法正确的是( )
A.太阳能、风能、天然气和生物质能都是可再生能源
B.水煤气是一种二次能源,比煤直接燃烧污染小
C.研究采煤、采油新技术的目的就是提高产量以满足工业生产的需要
D.氢能是理想的清洁能源,目前储存与运输方便、安全
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乳化炸药中微量水的存在严重影响产品品质,Karl Fischer法是测定其中微量水含量常用方法,该方法是利用I2和SO2反应定量消耗水作为原理,据此回答下列问题:
(1)写出该反应的化学反应方程式:_______________________。
下图是某同学在实验室模拟Karl Fischer法的实验装置图:

(2)实验开始时,向D装置中加入10.00克乳化炸药样品和10.16克I2(已知I2过量),打开所有止水夹,向装置内部通入N2,其目的是_______________________。
(3)关闭止水夹K1,打开分液漏斗活塞,加入硫酸后关闭,充分反应后,A中仍有SO2产生,关闭K2,此时B的作用是_______________________。B在反应过程中还能起到的作用是___________________________。
(4)反应后,将D装置取下,用N2赶走剩余SO2后加适量水配成250.00mL溶液,取25.00mL用0.20mol·L-1Na2S2O3标准液滴定剩余I2单质,已知反应如下:2S2O32-+I2=S4O62-+2I-,多次实验平均与消耗Na2S2O32溶液20.00mL,则原乳化炸药中水的含量为_________(填百分比)。
(5)若在滴定过程中不小心将标准液洒出去几滴,则水含量测定结果将____________(填“偏高”、“ 偏低”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作正确的是
A.向燃着的酒精灯添加酒精
B.用量筒量取10.0mL浓硫酸并在量筒中加水稀释
C.用托盘天平称量固体药品时,药品放左盘砝码放右盘
D.定容时加水超过容量瓶瓶颈上的刻度线,用胶头滴管吸出多出的溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com