
 CH3COOCH2CH3+H2O已知:乙醛可氧化为乙酸(该方程式不用写)
CH3COOCH2CH3+H2O已知:乙醛可氧化为乙酸(该方程式不用写) 分析 以乙烯和水为主要原料制取乙酸乙酯:乙烯含有碳碳双键,与水发生加成反应生成乙醇,乙醇中的醇羟基能被催化氧化,生成乙醛,乙醛氧化生成乙酸,乙醇和乙酸发生酯化反应,酸脱羟基醇脱氢生成乙酸乙酯和水.
解答 解:以乙烯和水为主要原料制取乙酸乙酯:先是乙烯的加成生成乙醇,后是乙醇的催化氧化生成乙醛,乙醛氧化生成乙酸,乙醇和乙酸发生酯化反应生成乙酸乙酯.
乙烯含有不饱和的C=C双键,C=C双键中1个C-C断裂结合水提供的-H、-OH,发生加成反应,反应的方程式为:CH2=CH2+H2O$\stackrel{催化剂}{→}$CH3CH2OH;
乙醇催化氧化,生成乙醛和水,反应方程式为:2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O;
乙醛氧化生成乙酸,乙醛与新制氢氧化铜悬浊液在加热条件下发生反应生成乙酸、氧化亚铜和水,方程式为:CH3CHO+2Cu(OH)2$\stackrel{△}{→}$CH3COOH+Cu2O↓+2H2O,
乙醇和乙酸在浓硫酸作用下加热生成乙酸乙酯,反应的方程式为:CH3COOH+C2H5OH CH3COOCH2CH3+H2O,
CH3COOCH2CH3+H2O,
故答案为:CH2=CH2+H2O$\stackrel{催化剂}{→}$CH3CH2OH;2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O;CH3CHO+2Cu(OH)2$\stackrel{△}{→}$CH3COOH+Cu2O↓+2H2O;
CH3COOH+C2H5OH CH3COOCH2CH3+H2O.
CH3COOCH2CH3+H2O.
点评 本题考查有机物推断,涉及烯烃、醇、醛、羧酸性质与转化,侧重对有机物的结构与性质的考查,为高频考点,把握官能团与性质的关系为解答的关键,注意发生的反应类型,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 氢气 | B. | 甲烷 | C. | 乙烷 | D. | 一氧化碳 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 纯净物 | B. | 混合物 | C. | 化合物 | D. | 单质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铝和氢氧化钠溶液反应生成Al(OH)3和Na | |
| B. | 钠在空气中燃烧生成淡黄色的NaO2 | |
| C. | 铁在高温下与水蒸气反应生成Fe3O4和H2 | |
| D. | 用碳酸钠和氢氧化钙反应制NaHCO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属与盐溶液的反应都是置换反应 | |
| B. | 阴离子都只有还原性 | |
| C. | 离子化合物中肯定存在离子键,可能不存在共价键 | |
| D. | 与强酸、强碱都反应的物质只有两性氧化物或两性氢氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2CO3的摩尔质量为106 g | |
| B. | 金刚石与石墨互为同位素 | |
| C. | 常温下,4.6gNa中含有的质子数为2.2NA | |
| D. | 标准状况下,11.2LCO2完全参与反应,转移的电子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2SO2(g)+O2(g)$?_{500℃}^{V_{2}O_{5}}$2SO3(g)△H=-196.6kJ/mol,若2molSO2完全反应则放出热量等于196.6kJ | |
| B. | “冰,水为之,而寒于水”说明相同质量的水和冰比较,冰的能量高 | |
| C. | 已知C(石墨)=C(金刚石)△H=+1.9kJ/mol,则从能量角度看金刚石比石墨稳定 | |
| D. | 氢气的燃烧热为285.8kJ/mol,则氢气燃烧的热化学方程式为2H2(g)+O2(g)=2H2O(l)△H=-285.8kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 氢能被视作连接化石能源和可再生能源的重要桥梁.
氢能被视作连接化石能源和可再生能源的重要桥梁.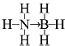 ;与氨硼烷互为等电子体的有机小分子是CH3CH3(写结构简式).
;与氨硼烷互为等电子体的有机小分子是CH3CH3(写结构简式).查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com