
| A. | 氧化剂与还原剂的物质的量之比是2:1 | |
| B. | 当生成22.4LSO2气体时,转移的电子数目是2NA | |
| C. | 该反应写成离子式是Cu+4H++SO42-$\frac{\underline{\;\;△\;\;}}{\;}$Cu+SO2↑+2H2O | |
| D. | 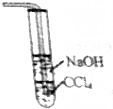 制备SO2装置尾气可用如图处理 |
分析 A.反应中浓硫酸起到氧化剂和酸的作用;
B.因不能确定气体存在的条件,则不能确定生成二氧化硫的物质的量;
C.浓硫酸中,硫酸主要以分子的形态存在;
D.二氧化硫不直接接触氢氧化钠溶液,可防止倒吸.
解答 解:A.由方程式可知铜和浓硫酸按1:2,反应生成二氧化硫和硫酸铜,反应中浓硫酸起到氧化剂和酸的作用,氧化剂与还原剂的物质的量之比是1:1,故A错误;
B.因不能确定气体存在的条件,则不能确定生成二氧化硫的物质的量,故B错误;
C.浓硫酸中,硫酸主要以分子的形态存在,离子方程式为Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$Cu2++SO42-+SO2+2H2O,故C错误;
D.二氧化硫不直接接触氢氧化钠溶液,可防止倒吸,且二氧化硫与氢氧化钠反应而防止污染,故D正确.
故选D.
点评 本题综合考查氧化还原反应,为高频考点,侧重于考查学生的分析、计算能力,注意把握浓硫酸的性质,难度不大.


科目:高中化学 来源: 题型:解答题
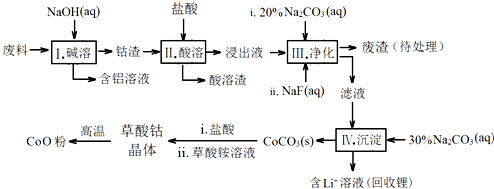
| Fe3+ | Co2+ | Co3+ | Al3+ | |
| pH(开始沉淀) | 1.9 | 7.15 | -0.23 | 3.4 |
| pH(完全沉淀) | 3.2 | 9.15 | 1.09 | 4.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 7.8 g Na2O2中存在的共价键总数为0.1NA | |
| B. | 2.4g石墨中含有C-C键个数为0.4NA | |
| C. | 标准状况下,22.4LCC14中所含分子数为NA | |
| D. | 0.1 mol氯化铁溶于1L水中,所得溶液中Fe3+的数目为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 元素f位于第三周期第Ⅲ族 | |
| B. | 离子的半径大小为r(d2一)>r(e+) | |
| C. | 元素g的最高价氧化物对应水化物的酸性比h的强 | |
| D. | 由x、z组成的一种四原子化合物的电子式为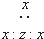 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
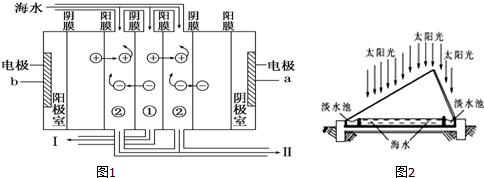
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 检查容量瓶瓶口是否漏水的方法是:往瓶内加入一定量水,塞好瓶塞.用食指摁住瓶塞,另一只手托住瓶底,把瓶倒转过来,观察瓶塞周围是否有水漏出即可 | |
| B. | 向装有2mL 2mol/L AlCl3溶液的试管中,逐滴加入0.01mol/L氨水3mL,产生沉淀且沉淀不溶解,说明氢氧化铝不溶于弱碱 | |
| C. | 用浓硫酸配制一定浓度的稀硫酸时,用量筒量取浓硫酸倒入盛水的烧杯中稀释,并用水洗涤量筒,洗涤液一并倒入烧杯中 | |
| D. | 如果不慎将酸粘到皮肤或衣物上,立即用较多的水冲洗,再用3%~5%的NaHCO3溶液来冲洗 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯的结构简式:CH2CH2 | B. | N2的结构式:N≡N | ||
| C. | Na的原子结构示意图: | D. | CH4分子的比例模型: |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com