
| A. | 84% | B. | 24% | C. | 19.6% | D. | 42% |
分析 乙醛(C2H4O)可以表示为C2H2.H2O,故乙炔(C2H2)、苯(C6H6)、乙醛(C2H4O)的混合气体可以看做C6H6、C2H2、H2O的混合物,进一步看作CH、H2O的混合物,根据O元素的分数计算H2O的质量分数,进而计算CH的质量分数,再根据CH中C、H质量之比为12:1,据此计算C元素的质量分数.
解答 解:乙醛(C2H4O)可以表示为C2H2.H2O,故乙炔(C2H2)、苯(C6H6)、乙醛(C2H4O)的混合气体可以看做C6H6、C2H2、H2O的混合物,进一步看作CH、H2O的混合物,O元素的分数为8%,故H2O的质量分数为$\frac{\frac{8%}{16}}{18}$=9%,故CH的质量分数1-9%=91%,CH中C、H质量之比为12:1,故C元素的质量分数为91%×$\frac{12}{13}$=84%,故选A.
点评 本题考查混合物中元素质量分数的计算,难度中等,关键是根据物质的化学式转化为CH与水的混合物.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | F-的原子结构示意图: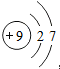 | B. | 乙烯的结构简式:CH2CH2 | ||
| C. | 葡萄糖的分子式:C6H12O6 | D. | 二氧化碳的电子式: |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
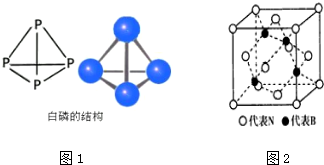
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | △H>0,△S>0的反应在所有温度下都能自发进行 | |
| B. | NH4HCO3(s)=NH3 (g)+H2O(g)+CO2(g)△H=+185.57 kJ•mol-1能自发进行,原因是体系有自发地向混乱度增加的方向转变的倾向 | |
| C. | △H<0、△S>0的反应在任何温度下都能自发进行 | |
| D. | 在其他外界条件不变的情况下,使用催化剂,可以改变化学反应速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 5 L Cl2与5 L HCl | |
| B. | 36 g H2O与44.8 L CO2 | |
| C. | 25℃,1.01×105 Pa时,等体积的空气与H2 | |
| D. | 0.2 mol O2与标准状况下2.24 L水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳碳间以单键结合,碳原子剩余价键全部与氢原子结合的烃一定是饱和链烃 | |
| B. | 分子组成符合CnH2n+2的烃一定是烷烃 | |
| C. | 正戊烷分子中所有原子均在一条直线上 | |
| D. | CH3CH(CH3)2在光照下与氯气反应,可以生成四种一氯代烃 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子间引力的大小 | B. | 分子数目的多少 | ||
| C. | 分子直径的大小 | D. | 分子间距离的大小 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com