
【题目】东晋《华阳国志·南中志》卷四中关于白铜的记载——云南镍白铜(铜镍合金),曾主要用于造币,亦可用于制作仿银饰品。回答下列问题:
(1)Ni2+基态原子的电子排布式为_______;3d能级上的未成对电子数为____。
(2)单质铜及镍都是由 _____键形成的晶体;元素铜与镍的第二电离能分别为:Icu =1958kJmol-1、INi=1753 kJmol-1,Icu >I Ni的原因是 ________________。
(3)Ni2+与丁二酮肟生成鲜红色丁二酮肟镍沉淀,该反应可用于检验 Ni2+。
2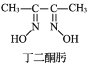 +Ni2+→
+Ni2+→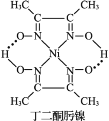 ↓+2H+
↓+2H+
①1 mol 丁二酮肟分子中含有σ 键的数目为_______mol。
②丁二酮肟镍分子中碳原子的杂化轨道类型为_____________。
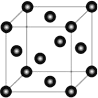
(4)Ni 的晶胞结构如图所示,镍晶体配位数目是__________ ;若 Ni 的原子半径为 d pm,Ni 的密度计算表达式是______g/cm3;Ni 原子空间利用率的计算表达式是_________。(Ni 的相对原子量用 Mr 表示)
【答案】1s22s22p63s23p63d84s2或[Ar]3d84s2 2 金属 铜失去的是全充满的3d10电子,镍失去的是4s1电子 15 sp3、sp2 12 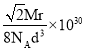
【解析】
(1)Ni为第28号元素,其基态原子核外电子排布式为1s22s22p63s23p63d84s2或[Ar]3d84s2,3d能级上未成对电子式为2;
(2)Ni和Cu都是由金属键形成的金属晶体,元素铜与镍的第二电离能分别为:Icu=1958kJmol-1、INi=1753kJmol-1,Icu>I Ni的原因是铜失去的是全充满的3d10电子,镍失去的是4s1电子;
(3)①已知丁二酮肟的结构式为![]() ,分子中含有13个单键和2个双键,则共有15个σ键,所以1mol丁二酮肟含有σ键数为15NA;
,分子中含有13个单键和2个双键,则共有15个σ键,所以1mol丁二酮肟含有σ键数为15NA;
②甲基上碳原子价层电子对个数是4且不含孤电子对,为sp3杂化,连接甲基的碳原子含有3个价层电子且不含孤电子对,为sp2杂化;
(4)镍晶体的晶胞为面心立方,配位数目是12;Ni的密度应由晶胞内Ni的质量除以晶胞体积计算,晶胞中Ni的个数有![]() =4个,故晶胞质量为
=4个,故晶胞质量为![]() g,又已知Ni原子的半径为d pm,晶胞棱长为
g,又已知Ni原子的半径为d pm,晶胞棱长为![]() pm,晶胞体积为
pm,晶胞体积为![]() pm3=
pm3=![]() cm3,故晶胞密度为
cm3,故晶胞密度为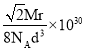 g/cm3;空间利用率的计算表达式为
g/cm3;空间利用率的计算表达式为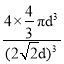


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】用50mL 0.50mol/L盐酸与50mL 0.55mol/LNaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
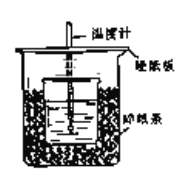
(1)从实验装置上看,图中尚缺少的一种玻璃用品是________________;由图可知该装置有不妥之处,应如何改正?___________________________________________________.
(2)烧杯间填满碎塑料泡沫的作用是__________________________________________.
(3)如果用60mL 0.50mol/L盐酸与50mL 0.55mol/LNaOH溶液进行反应,与上述实验相比,所求得的中和热数值___________(填“相等、不相等”)
(4)用相同浓度和体积的氨水(NH3·H2O)代替NaOH溶液进行上述实验,测得的中和热的数值会____________(填“偏大”、“偏小”、“无影响”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)写出下列物质在水溶液中的电离方程式
①H2SO4—____________________;
②Ba(OH)2—____________________;
③NaCl—____________________;
④CuSO4—____________________;
⑤Na2CO3—____________________;
⑥NH4NO3—____________________;
(2)写出下列微粒的结构示意图
①H____________________;
②Na____________________;
③O2-____________________;
④Mg2+____________________;
⑤最外层电子数为次外层电子数2倍的原子____________________;
⑥第二层电子数为第一层、第三层电子数之和的原子:______________________;
⑦氢元素存在着氕氘氚三种原子,它们的原子核内都含有一个质子,中子数分别为0、1、2,请用![]() 表示这三个原子____________________________________,这三种原子的关系是互为_____________。
表示这三个原子____________________________________,这三种原子的关系是互为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2020年3月24日,中国工程院院士、天津中医药大学校长张伯礼表示,中成药连花清瘟胶囊对于治疗轻型和普通型的新冠肺炎患者有确切的疗效。其有效成分绿原酸的结构简式如图,下列有关绿原酸说法正确的是
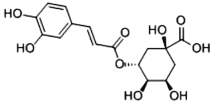
A.最多有 7 个碳原子共面
B.1mol 绿原酸可消耗 5molNaOH
C.不能使酸性高锰酸钾溶液褪色
D.能发生酯化、加成、氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是硫酸试剂瓶标签上的内容:

![]() 该硫酸的物质的量浓度为______
该硫酸的物质的量浓度为______![]() 。
。
![]() 某化学小组进行硫酸酸性实验探究时,需要配制
某化学小组进行硫酸酸性实验探究时,需要配制![]() 的稀硫酸,则需要取上述的浓硫酸______mL。
的稀硫酸,则需要取上述的浓硫酸______mL。
(3)下列情况使所配制硫酸溶液物质的量浓度偏高的是________,
A.未经冷却趁热将溶液注入容量瓶中
B.定容时仰视读数
C.移液时不慎将少量溶液滴在容量瓶外面
D.用量筒量取浓硫酸时仰视读数
E.加蒸馏水时不慎超过了刻度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 分子式为C5H11Cl的同分异构体有7种
B. 分子中有两个—CH3,分子式为C5H11Cl的同分异构体有3种
C. 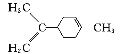 中所有碳原子一定在同一平面上
中所有碳原子一定在同一平面上
D. ![]() 中至少有16个原子共平面
中至少有16个原子共平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】0.5mol·L-1CH3COONa溶液和水的pH随温度的变化如图所示,下列分析错误的是
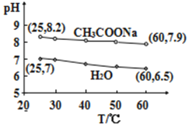
A.25℃,CH3COONa溶液的pH=8.2,显碱性
B.60℃,H2O中c(H+)=1×10-6.5mol·L-1,呈中性
C.60℃,CH3COONa溶液中c(OH-)=1×10-5.1mol·L-1
D.升高温度,CH3COONa溶液水解程度和pH都减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(9分)现有含NaCL、Na2SO4和NaNO3的混合物,选择适当的试剂将其转化为相应的沉淀或固体,从而实现CL-、SO42-、和NO3-的相互分离。相应的实验过程可用下图表示:
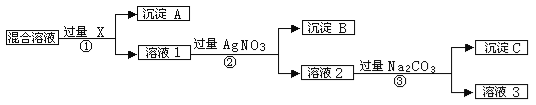
请回答下列问题:
⑴写出实验中下列物质的化学式:试剂X :_______,沉淀A:_______,沉淀B:______。
⑵上述实验流程中加入过量的Na2CO3的目的是___________________________________。
⑶按此实验方案得到的溶液3中肯定含有___________(填化学式)杂质;为了解决这个问题,可以向溶液3中加入适量的___________ ,之后若要获得固体NaNO3需进行的实验操作是________________(填操作名称)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化镁(MgO2)不溶于水,与酸反应生成H2O2,在医学上可作解酸剂。常温下MgO2较稳定,加热时会分解生成O2和MgO。MgO与H2O2反应可制得MgO2,同时放出大量热。一种制备MgO2的流程如图所示:
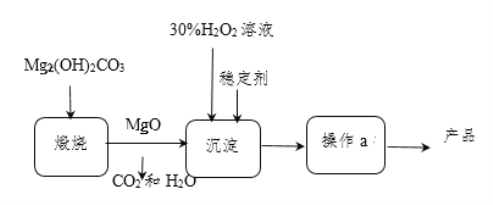
请回答下列问题:
(1)煅烧Mg2(OH)2CO3的化学反应方程式为_______________________;检验Mg2(OH)2CO3已分解完全的方法是______________________________。(写出实验操作和现象)
(2)上述制备过程中加入稳定剂的作用是___________;操作a为_____________。
MgO2产品中常会混有少量MgO,实验室可通过多种方案测定样品中MgO2的含量。某研究小组拟用下图装置测定样品(含MgO杂质)中MgO2的含量。
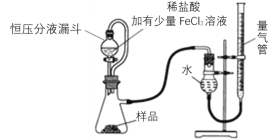
(3)研究小组的实验原理是(用化学方程式表示)①___________________________;
②2H2O2 → 2H2O +O2↑,稀盐酸中加入少量FeCl3溶液的作用是_______________。
(4)实验中使用恒压分液漏斗的优点是:使分液漏斗中的溶液顺利滴下、___________。
(5)反应结束后,先_________________,然后__________________,最后平视刻度线读数并记录。
(6)该小组记录的实验数据如下,样品的质量为m g;反应开始前量气管的读数为a mL;反应结束后量气管的读数为b mL,则样品中过氧化镁的质量分数为______(该实验条件下O2密度为ρ gL-1)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com