
| mg |
| 232g/mol |
| 3m |
| 2��232 |
| 3m |
| 2��232 |
| 60m |
| 58 |
| 60m |
| 58 |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 �ȣ����ڶԽǹ�ϵ��Ԫ�أ��䵥�ʡ���������������ƣ�����������������Գ���������þ�������ԣ����й����뼰�仯��������ʵ���������ȷ���ǣ�������
�ȣ����ڶԽǹ�ϵ��Ԫ�أ��䵥�ʡ���������������ƣ�����������������Գ���������þ�������ԣ����й����뼰�仯��������ʵ���������ȷ���ǣ�������| A��Be����������ˮ��Ӧ |
| B��Be��OH��2���Ȳ���ֽ� |
| C��BeO����ˮ��Ӧ |
| D��Be��OH��2����ǿ�Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����ʯ������ʳƷ�������� |
| B�������������ζƷ |
| C�����ɾ�ʢʳ�� |
| D��С�մ���������ͷ۵���Ҫ�ɷ�֮һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
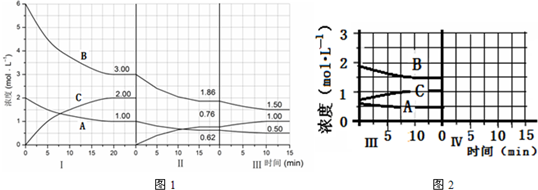
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| �� �� | �������Լ� | �й����ӷ���ʽ |
| ��1��HNO3��H2SO4�� | ||
| ��2��Cu��Fe�� | ||
| ��3��NaCl��Na2CO3�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
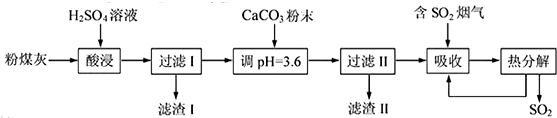
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| Ԫ�� | A | B | C | D |
| ��� ��Ϣ |
�䵥����һ�ֱ����ж��ֿ�������������ɫ���� | �䵥�ʼ��н����ԣ�����һ���ķǽ����ԣ������ڽ����� | �������������ǵ��Ӳ�����2���������γ��۵��Ӳ�ȴ���ȶ����� | ������Ӻ�����Ӳ�ṹ��Arԭ�ӵ��Ӳ�ṹ��ͬ�����ʳ������ڻ�ɽ��ڸ�����ؿǵ��Ҳ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A����������ģ�ͣ� |
| B����CH3��3COH�����ƣ�2��2�����Ҵ� |
| C����ȩ�Ľṹʽ��CH3CHO |
D���ǻ��ĵ���ʽ�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com