
下列有关化学用语以及化学基本概念的表述中正确的一组是
A. 过氧乙酸(CH3COOOH)与羟基乙酸(HOCH2COOH)所含官能团相同,两者互为同分异构体
B. 日本福岛核电站泄露的放射性核素 Ⅰ和
Ⅰ和 Cs,前者比后者少4个中子
Cs,前者比后者少4个中子
C. 亚硫酸氢钠和碳酸氢钠的电离方程式都表示为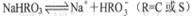
D. 次氯酸的结构式为HOCl,过氧化氢的电子式为
 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:高中化学 来源: 题型:
下列叙述正确的是( )
A.所有卤代烃都难溶于水,且都是密度比水大的液体
B.所有卤代烃都是通过取代反应制得
C.卤代烃不属于烃类
D.卤代烃都是良好的有机溶剂
查看答案和解析>>
科目:高中化学 来源: 题型:
已知某溶液中只存在OH-、H+、NH 、Cl-四种离子,某同学推测该溶液中各离子浓度大小顺序可能有如下四种关系:
、Cl-四种离子,某同学推测该溶液中各离子浓度大小顺序可能有如下四种关系:
①c(Cl-)>c(NH )>c(H+)>c(OH-)
)>c(H+)>c(OH-)
②c(Cl-)>c(NH )>c(OH-)>c(H+)
)>c(OH-)>c(H+)
③c(NH )>c(Cl-)>c(OH-)>c(H+)
)>c(Cl-)>c(OH-)>c(H+)
④c(Cl-)>c(H+)>c(NH )>c(OH-)
)>c(OH-)
填写下列空白:
(1)若溶液中只溶解了一种溶质,该溶质的名称是________,上述离子浓度大小顺序关系中正确的是________(选填序号)。
(2)若上述关系中③是正确的,则溶液中溶质的化学式是_________________。若上述关系中④是正确的,则溶液中溶质的化学式是________。
(3)若该溶液由体积相等的稀盐酸和氨水混合而成,且恰好呈中性,则混合前盐酸的物质的量浓度(填“大于”“小于”或“等于”,下同)________氨水的物质的量浓度,混合前盐酸中c(H+)和氨水中c(OH-)的关系:
c(H+)______c(OH-)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关合成氨工业的说法中,正确的是 ( )。
A.从合成塔出来的混合气体中,氨气占15%,所以生产氨的工厂的效率都
很低
B.由于氨易液化,N2和H2在实际生产中循环使用,所以总体来说,氨的产
率很高
C.合成氨工业的反应温度控制在500 ℃,目的是使化学平衡向正反应方向
移动
D.我国合成氨厂采用的压强是10~30 MPa,因为该压强下铁触媒的活性最
大
查看答案和解析>>
科目:高中化学 来源: 题型:
哈伯因发明了由氮气和氢气合成氨气的方法而获得1918年诺贝尔化学奖。现将氢气和氮气充入某密闭容器中,在一定条件下反应的有关数据为:
| 项目 | H2 | N2 | NH3 |
| 起始时 | 5 mol·L-1 | 3 mol·L-1 | 0 |
| 2 s末 | 2 mol·L-1 |
(1)氢气和氮气反应生成氨气(在2 s内)的反应速率v(H2)=__________。若此时已达平衡,则可求得平衡常数为__________。
(2)下图表示合成NH3反应在时间t0→t6中反应速率与反应过程曲线图,则在下列达到化学平衡的时间段中,化学平衡常数最大的一段时间是__________。
①t0→t1 ②t2→t3 ③t3→t4 ④t5→t6
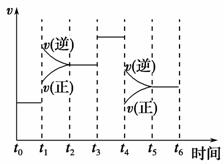
若t1时改变的条件是升高温度,则说明合成NH3反应的焓变ΔH________0(填“大于”或“小于”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关实验原理或操作正确的是
A. SO2气体的还原性较强,不能使其通过浓硫酸干燥
 B. 滴定管洗净后经蒸馏水润洗,即可注入标准液进行滴定
B. 滴定管洗净后经蒸馏水润洗,即可注入标准液进行滴定
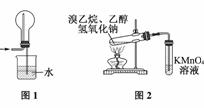
C. 用图1装置吸收多余的HCl气体
D. 用图2装置检验溴乙烷发生消去反应生成乙烯
查看答案和解析>>
科目:高中化学 来源: 题型:
恒温(1100℃)恒容密闭容器中发生反应:
Na2SO4(s)+4H2(g) Na2S(s)+4H2O(g)。下列说法正确的是
Na2S(s)+4H2O(g)。下列说法正确的是
A. 该反应的平衡常数表达式K=c(H2O)/c(H2)
B. 若容器内气体的密度或压强保持不变,均说明该反应已达到平衡状态
C. 若Na2SO4足量,改变起始充入H2的浓度,达平衡时H2的转化率不变
D. 若初始时投入2.84gNa2SO4与一定量H2反应达平衡时容器内固体共有2.264g,则Na2SO4的转化率为45%
查看答案和解析>>
科目:高中化学 来源: 题型:
甲、乙两烧杯中各盛有100 mL 3 mol/L的盐酸和氢氧化钠溶液,向两烧杯中分别加入等质量的铝粉,反应结束后测得生成的气体体积比为甲:乙=1:2,则加入铝粉的质量为( )
A.5.4g B.3.6g C.2.7g D.1.8g
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上把Cl2通入冷NaOH溶液中制得漂白液(主要成分NaClO)。一化学小组在室温下将氯气缓缓通入NaOH溶液,模拟实验得到ClO-、ClO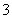 等离子其物质的量(mol)与反应时间t(min)的关系曲线。下列说法错误的是( )
等离子其物质的量(mol)与反应时间t(min)的关系曲线。下列说法错误的是( )

A.工业制取漂白液的化学反应方程式为Cl2+2NaOH===NaCl+NaClO+H2O
B.a点时溶液中各离子浓度:c(Na+)>c(Cl-)>c(ClO3-)=c(ClO-)>c(OH-)>c(H+)
C. t2~t4,ClO-离子的物质的量下降的原因可能是3ClO-= 2Cl-+ClO3-
D.使用漂白液时,为了增强漂白效果,可以向漂白液中加入浓盐酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com