
��������(NaClO)�Ͳ�������(NaClO)������Ҫ�ĺ�����������
(l) NaClO2�У���Ԫ�صĻ��ϼ�Ϊ________��
(2)ijͬѧ��ʵ����̽��������һ�ּ��û���������Һ(NaClO)���������������ͼ��װ�ã���ʯī���缫��ⱥ���Ȼ�����Һ��
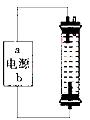
��ͨ��ʱ��ΪʹCl2����ȫ���գ��Ƶ��н�ǿɱ������������Һ�����Դ��b�缫����Ϊ_________�������������������������������Ͷ��
��װ���з�����Ӧ���йػ�ѧ����ʽΪ________�� ��ֵ�����Һ�и�����Ũ���ɴ�С˳��Ϊ____________��
����˵��ʹ�ø�װ����������Һ��һ���ŵ��һ��ע������____ ��
(3)��ѧ����С��Ϊ�ⶨijƷ�ơ�84����Һ����NaClO�ĺ�������λ�����Һ���� NaCIO������������������ʵ�顣��֪��
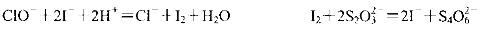
ȡ10 mL������Һ����ƿ�У�Ѹ�ټ��������������ữ�ĵ⻯����Һ���ܷ⡢���
��ϣ��������ü����ӡ�Ȼ����뼸�ε�����Һ����c mol/L�����������(Na2S2O3)
����Һ�ζ���ƽ����ȥVmL�����������Һ����á�84����Һ����NaCIO�ĺ���
Ϊ_________g/mL���ú�c��V��ʽ�ӱ�ʾ����
(4)�����ǹ������ⷨ�����������ƵĹ�������ͼ��
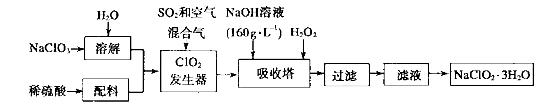
��֪��(i)NaClO2 ���ܽ�����¶����߶������ʵ������¿ɽᾧ����: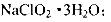
(ii)��ClO2�ֽⱬը��һ����ϡ����������ϡ�͵�10%���½ϰ�ȫ��
(iii) HClO2�ɿ�����ǿ�ᡣ
�ٷ������з�����Ӧ�����ӷ���ʽΪ___________________�ڷ������й�����������ÿ�����__________________��
���������ڵķ�Ӧ�Ļ�ѧ����ʽΪ__________________������������Ϊ��ֹ����ԭ��NaCI�����û�ԭ���Ļ�ԭ��Ӧ���С����⣬������ѡ��Ļ�ԭ��_________������ţ���
A.Na2O2 B��Na2S C.FeCl2
�۴���Һ�еõ�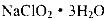 �־����ʵ�����������_________������ţ���
�־����ʵ�����������_________������ţ���
A.���� B������ C.���� D.���� E����ȴ�ᾧ
��֪ʶ�㡿���������� B1 D2C1 F4 A3
���𰸽�������1����3��1�֣�
��2��������1�֣� ��2NaCl��2H2O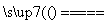 2NaOH��H2����Cl2�� Cl2��2NaOH===NaCl��NaClO��H2O��2�֣� c(Na��)��c(ClO��)��c(OH��)��c(H��) ��2�֣�
2NaOH��H2����Cl2�� Cl2��2NaOH===NaCl��NaClO��H2O��2�֣� c(Na��)��c(ClO��)��c(OH��)��c(H��) ��2�֣�
�۷��㡢��ݣ�1�֣� ���ɵĿ�ȼ�����壬Ҫ��ʱ�������������Σ�գ�1�֣�
��3��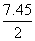 ��10-3cV��2�֣�
��10-3cV��2�֣�
��4����2ClO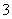 ��SO2��2ClO2����SO
��SO2��2ClO2����SO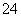 ��2�֣� ϡ��ClO2�Է�ֹ��ը��1�֣�
��2�֣� ϡ��ClO2�Է�ֹ��ը��1�֣�
��2NaOH��2ClO2��H2O2=2NaClO2��2H2O��O2����2�֣� A��1�֣�
��BED��2�֣�
�������Ÿ����������ϼ۴�����Ϊ0֪NaClO2�У���Ԫ�صĻ��ϼ�Ϊ+3
�Ƣ�ΪʹCl2����ȫ���գ�������������������b���������Ȼ�����Һ��������������ơ�����������2NaCl��2H2O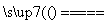 2NaOH��H2����Cl2����Ȼ�����������������պ÷�ӦCl2��2NaOH===NaCl��NaClO��H2O�����ܷ�Ӧ�ɿ�����NaCl��H2O
2NaOH��H2����Cl2����Ȼ�����������������պ÷�ӦCl2��2NaOH===NaCl��NaClO��H2O�����ܷ�Ӧ�ɿ�����NaCl��H2O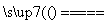 NaClO��H2���� NaClO��ˮ��ʹ��Һ�ʼ��ԣ��������Ũ�ȴ�С�� c(Na��)��c(ClO��)��c(OH��)��c(H��)��ʹ�ø�װ����������Һ��һ���ŵ��Ƿ��㣬��ݣ�ͨ�缴���ɴ������ƣ�����������������Ҫע�ⲻ��ʹ������
NaClO��H2���� NaClO��ˮ��ʹ��Һ�ʼ��ԣ��������Ũ�ȴ�С�� c(Na��)��c(ClO��)��c(OH��)��c(H��)��ʹ�ø�װ����������Һ��һ���ŵ��Ƿ��㣬��ݣ�ͨ�缴���ɴ������ƣ�����������������Ҫע�ⲻ��ʹ������
�Ǹ���NaClO~I2~2Na2S2O3
74.5 2mol
m Vc��10-3��m=37.25Vc��10-3g����3.725Vc��10-3g/mL
�Ȣٷ�������ͼ֪ClO3-��C1O2��ClԪ�صĻ��ϼ۽��ͣ�������������������Ӧ��ClO3-������������Ӧ���ӷ���ʽΪSO2+2ClO3-=2C1O2+SO42-�����ݴ�ClO2�ֽⱬը֪�������й������������Ӧ��ϡ��ClO2���Է�ֹ��ը���ڸ���ClO2��NaClO2֪�������ڵķ�Ӧ��ClO2����H2O2����2ClO2+H2O2 +2NaOH=2NaClO2+2H2O+O2�����������У��ɴ���H2O2���Լ��ǻ�ԭ������ӽ��ģ���ѡNa2O2������ѡ�û�ԭ��̫ǿ��Na2S��FeCl2������ò���NaClO2��������FeCl2�����������ʢۿ�ͨ����ȴ�ᾧ�����˵õ����壬����ҺŨ��ƫС����������Ũ��������ȴ�ᾧ�����ˡ�
��˼·�㲦���������ಽ����Ӧ�ļ�����ù�ϵʽ�����������̣���ȷ�����ķ�Ӧ�ǽ�������ij��÷�����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���ôӶ�������ȡ���л���A�ϳɿ��᳦��ҩ��Y��������ѧƷ���ϳ�·�����£�
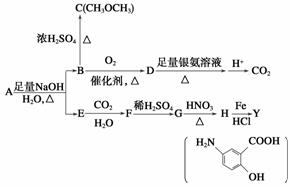
��ʾ��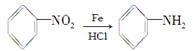
����������Ϣ�ش�
(1)D����NaHCO3��Һ��Ӧ��D�й����ŵ�������________��B��C�ķ�Ӧ������________________________________________________________________________��
(2)д��A����B��E�Ļ�ѧ��Ӧ����ʽ
________________________________________________________________________
________________________________________________________________________��
(3)A��ͬ���칹��I��J����Ҫ��ҽҩ�м��壬��Ũ����������£�I��J�ֱ�����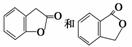 ������I��J���Լ�Ϊ________________��
������I��J���Լ�Ϊ________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ˮ��Һ���ܴ��������һ����
A��Ba2+��Na+��SO42—��Cl— B��MnO4—��SO32—��H+��K+
C��AlO2—��Mg2+��K+ ��HCO3— D��K+�� Na+�� NO3— ��SO42—
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�������£�pH=1��ij��ҺA�к���NH4+��K+��Na+��Fe3+��Al3+��Fe2+��CO32-��NO3-��Cl-��I-��SO42���е�4�֣��Ҹ����ӵ����ʵ���Ũ�Ⱦ�Ϊ0.1mol/L����ȡ����Һ�����й�ʵ�飬ʵ��������ͼ��ʾ��
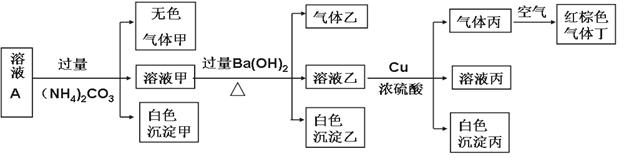
�����й�˵����ȷ���� �� ��
A. ������һ����BaCO3��������BaSO4
B��ʵ������Cu 14.4g,���������嶡�����Ϊ3.36L
C������Һ��һ����NO3-��Al3+��SO42����Cl-��������
D.���ɵļס��ҡ��������Ϊ��ɫ��������ˮ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����й����ӷ���ʽ��������ʵ�������ȷ����
A.�ö��Ե缫���MgCl2��Һ:2Cl����2H2O H2��+Cl2��+2OH��
H2��+Cl2��+2OH��
B.��Ba(OH)2��Һ�еμ�ϡ����:Ba2++OH-+H++SO42-=BaSO4��+H2O
C. (NH4)2Fe(SO4)2��Һ�����NaOH��Һ��Ӧ��Fe(OH)2: Fe2++2OH - =Fe(OH)2
D. C12ͨ�����ʯ��ˮ��:C12+2OH - =C1-+CIO-+H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ij��Һ���ܺ���Cl����SO42����CO32����NH4+��Fe3+��Al3+��K+��ȡ����Һ100mL���������NaOH��Һ�����ȣ��õ�0.02mol���壬ͬʱ�������ɫ���������ˣ�ϴ�ӣ����գ��õ� 1.6g���壻��������Һ�м�����BaCl2��Һ���õ� 4.66g����������ij������ɴ˿�֪ԭ��Һ��
��A�����ٴ���5������
��B��Cl��һ�����ڣ���c��Cl������0.4mol/L
��C��SO42����NH4+��һ�����ڣ�Cl�����ܲ�����
��D��CO32����Al3+һ�������ڣ�K+���ܴ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��Ba(OH)2��Һ����μ���ϡ���ᣮ������������⣺
(1)д����Ӧ�����ӷ���ʽ___________________________
(2)������������£����ӷ���ʽ��(1)��ͬ����________(�����)��
A����NaHSO4��Һ�У���μ���Ba(OH)2��Һ����Һ������
B����NaHSO4��Һ�У���μ���Ba(OH)2��Һ��SO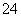 ǡ����ȫ����
ǡ����ȫ����
C����NaHSO4��Һ�У���μ���Ba(OH)2��Һ������
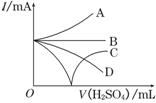
(3)����������ϡH2SO4ֱ�����������������л����Һ�еĵ�������(�õ���ǿ��I��ʾ)�ɽ��Ƶ�����ͼ�е����߱�ʾ��________(�����)��
(4)����װ��Ba(OH)2��Һ�ձ��ﻺ������KAl(SO4)2��Һ��Ba2+ǡ����ȫ��Ӧ����Ӧ�����ӷ���ʽ�� _________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��1 molij��̬����2 mol Cl2�����ӳɷ�Ӧʱ�������еIJ�����̼ԭ��ȫ��ת��Ϊ����̼ԭ�ӣ����ò�������2 mol Cl2����ȡ����Ӧ������ֻ��C��Cl����Ԫ�صĻ���������̬����(����)
A����ϩ B����Ȳ C����ϩ D����Ȳ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��һ���¶��£�������X������Y��0.16mol����10L�����ܱ������У�������Ӧ��X��g��+Y��g�� 2 Z��g��
2 Z��g��  H<0��һ��ʱ���ﵽƽ�⣬��Ӧ�����вⶨ���������±���
H<0��һ��ʱ���ﵽƽ�⣬��Ӧ�����вⶨ���������±���
| t/min | 2 | 4 | 7 | 9 |
| n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
����˵����ȷ����
A.��Ӧǰ2 min ��ƽ������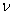 (Z)=2.0
(Z)=2.0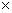 10-3mol·L-1·min-1
10-3mol·L-1·min-1
B. �����������䣬�����¶ȣ���Ӧ�ﵽ��ƽ��ǰ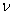 (��)>
(��)>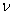 (��)
(��)
C. ���������������䣬��ʼʱ�������г���0.32mol ����X��0.32 mol ����Y���ﵽƽ��ʱ��n(Z)<0.24mol
D. �����������䣬��ƽ����ϵ���ٳ���0.16mol ����X����ԭƽ����ȣ��ﵽ��ƽ��ʱ������Y��ת��������X�������������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com