

| 1.7g |
| 18g/mol |
| 13.2g |
| 44g/mol |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| A、②⑤ | B、①②③ |
| C、①②③⑤ | D、全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 阳离子 | Na+、Ba2+、NH4+ |
| 阴离子 | CO32-、Cl-、OH-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、 Zn、MnO2干电池放电时MnO2被氧化 Zn、MnO2干电池放电时MnO2被氧化 |
B、 电解精炼铜时,阳极减少的质量与阴极增加的质量一定相等 电解精炼铜时,阳极减少的质量与阴极增加的质量一定相等 |
C、 K分别于M、N连接,均可保护Fe电极,且都称为“牺牲阳极的阴极保护法” K分别于M、N连接,均可保护Fe电极,且都称为“牺牲阳极的阴极保护法” |
D、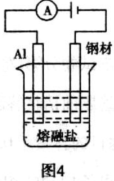 在钢材上电镀铝,熔融盐中Al和Cl元素只以AlCl4-、Al2Cl3-,形式存在,则阳极反应式为:Al-3e-+7AlCl4-=4Al2Cl3- 在钢材上电镀铝,熔融盐中Al和Cl元素只以AlCl4-、Al2Cl3-,形式存在,则阳极反应式为:Al-3e-+7AlCl4-=4Al2Cl3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、升高温度可减小反应速率 |
| B、加入合适的催化剂可提高反应速率 |
| C、达到平衡时,v(正)=v(逆)=0 |
| D、达到平衡时,NO2转化率为100% |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
 二氧化氯(ClO2)是目前国际上公认的第四代高效、无毒的消毒剂,是一种黄绿色的气体,易溶于水.实验室可用NH4Cl、盐酸、NaClO2(亚氯酸钠)为原料制备ClO2的流程如下:
二氧化氯(ClO2)是目前国际上公认的第四代高效、无毒的消毒剂,是一种黄绿色的气体,易溶于水.实验室可用NH4Cl、盐酸、NaClO2(亚氯酸钠)为原料制备ClO2的流程如下:
查看答案和解析>>
科目:高中化学 来源: 题型:

| 物质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 开始沉淀pH | 6.0 | 7.5 | 1.4[ |
| 沉淀完全pH | 13 | 14 | 3.7 |

查看答案和解析>>
科目:高中化学 来源: 题型:
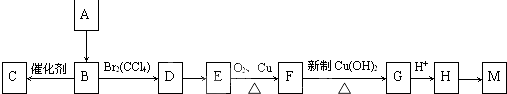
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com