
下列关于常见物质的工业冶炼说法正确的是
A.工业制金属钠:电解饱和食盐水
B.工业制溴:某些植物具有富集溴的能力,从海产品中提取溴是工业上获取溴的重要途径
C.冶炼铝:电解Al2O3,同时加入冰晶石(Na3AlF6),目的是为了降低Al2O3的熔融温度
D.硫酸工业:在氧气充足的情况下,从接触室进入吸收塔的气体中不可能含有SO2
科目:高中化学 来源:2014-2015江苏省扬州市高一上学期期末化学试卷(解析版) 题型:填空题
(8分)化学与人类生活密切相关。请按要求,回答下列问题:
(1)漂白粉有效成分的化学式为 ,其能消毒杀菌是因有强 性。
(2)KAl(SO4)212H2O的俗名为 ,因其溶于水生成 而具有净水作用。
(3)酸雨的pH小于 ,含亚硫酸的酸雨久置后pH (增大、减小或不变)。
(4)小苏打可用于治疗胃酸过多,其反应的离子方程式为 。
查看答案和解析>>
科目:高中化学 来源:2014-2015江苏省扬州市高二上学期期末化学(必修)试卷(解析版) 题型:选择题
14C的放射性可用于考古断代。下列关于14C的说法中正确的是
A.质量数为6 B.质子数为6 C.电子数为14 D.中子数为14
查看答案和解析>>
科目:高中化学 来源:2014-2015山东省枣庄市高一上学期期末化学试卷(解析版) 题型:选择题
下表各选项中,不能利用置换反应通过Y得到W的一组化合物是
选项化合物 | A | B | C | D |
Y | CO2 | Fe2O3 | SiO2 | FeCl3 |
W | MgO | Al2O3 | CO | CuCl2 |
查看答案和解析>>
科目:高中化学 来源:2014-2015山东省枣庄市高一上学期期末化学试卷(解析版) 题型:选择题
下列有关溶液组成的描述合理的是
A.无色溶液中可能大量存在Al3+、NH4+、Cl-、OH-
B.酸性溶液中可能大量存在Na+、ClO-、SO42-、I-
C.弱碱性溶液中可能大量存在Na+、K+、Cl-、HCO3-
D.红色溶液中可能大量存在Fe3+、K+、Cl-、SCN-
查看答案和解析>>
科目:高中化学 来源:2014-2015山东省枣庄市高一上学期期末化学试卷(解析版) 题型:选择题
1998年诺贝尔化学奖授予科恩(美)和波普尔(英),以表彰他们在理论化学领域作出的重大贡献。他们的工作使实验和理论能够共同协力探讨分子体系的性质,引起整个化学领域正在经历一场革命性的变化。下列说法正确的是
A.化学不再是纯实验科学 B.化学不再需要实验
C.化学不做实验,就什么都不知道 D.未来化学的方向还是经验化
查看答案和解析>>
科目:高中化学 来源:2014-2015江西省新余市高一上学期期末考试化学试卷(解析版) 题型:选择题
在FeCl3、CuCl2、FeCl2的混合溶液中,Fe3+、Cu2+和Fe2+的物质的量之比为3∶2∶1,现加入适量铁粉,使溶液中三种离子物质的量浓度之比变化为1∶2∶4,则参加反应的铁粉与原溶液Fe3+的物质的量之比为
A.2:1 B.1:2 C.1:3 D.1:4
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省六校高三3月联考理综化学试卷(解析版) 题型:填空题
(16分)CO是现代化工生产的基础原料,下列有关问题都和CO的使用有关。
(1)人们利用CO能与金属镍反应,生成四羰基镍,然后将四羰基镍分解从而实现镍的提纯,最后可以得到纯度达99.9%的高纯镍。具体反应为:
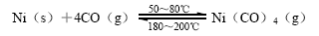
该正反应的ΔH 0(选填“>”或“=”或“<”)。
(2)工业上可利用CO生产乙醇:2CO(g)+4H2(g)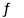 CH3CH2OH(g)+H2O(g) ΔH1
CH3CH2OH(g)+H2O(g) ΔH1
又已知:H2O(l)=== H2O(g) ΔH2
CO(g)+H2O(g)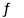 CO2(g)+H2(g) ΔH3
CO2(g)+H2(g) ΔH3
工业上也可利用CO2(g)与H2(g)为原料合成乙醇:
2CO2(g)+6H2(g) 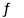 CH3CH2OH(g)+3H2O(l) ΔH
CH3CH2OH(g)+3H2O(l) ΔH
则:ΔH与ΔH1、ΔH2、ΔH3之间的关系是:ΔH=_______________________。
(3)一定条件下,H2、CO在体积固定的密闭容器中发生如下反应:
4H2(g)+2CO(g)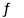 CH3OCH3(g)+H2O(g),
CH3OCH3(g)+H2O(g),
下列选项能判断该反应达到平衡状态的依据的有___ 。
A.2v(H2)= v(CO)
B.CO的消耗速率等于CH3OCH3的生成速率
C.容器内的压强保持不变
D.混合气体的密度保持不变
E.混合气体的平均相对分子质量不随时间而变化
(4)工业可采用CO与H2反应合成再生能源甲醇,反应:CO(g)+ 2H2(g)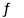 CH3OH(g)
CH3OH(g)
在一容积可变的密闭容器中充有10molCO和20mol H2,在催化剂作用下发生反应生成甲醇。CO的平衡转化率(α)与温度(T)、压强(p)的关系如(图28题-1)所示。
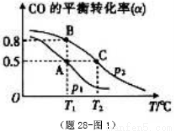
①合成甲醇的反应为__ __(填“放热”或“吸热”)反应。
②A、B、C三点的平衡常数KA、KB、KC的大小关系为___ 。
③若达到平衡状态A时,容器的体积为10L,则在平衡状态B时容器的体积为__ __L。
④(题28-图2)中虚线为该反应在使用催化剂条件下关于起始氢气与CO投料比和CO平衡转化率的关系图.当其条件完全相同时,用实线画出不使用催化剂情况下CO平衡转化率的示意图.
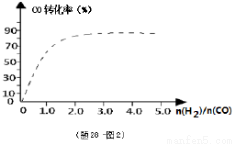
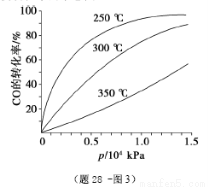
⑤CO的平衡转化率(α)与温度(T)、压强(p)的关系如(题28 -图3)所示,实际生产时条件控制在250 ℃、1.3×104 kPa左右,选择此压强的理由是________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省怀化市高三第一次模拟考试理综化学试卷(解析版) 题型:选择题
-C3H7和-C3H7O取代苯环上的氢原子,形成的有机物中能与金属钠反应的同分异构体有
A.10种 B.15种 C.30种 D.36种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com