
大气固氮(闪电时N2转化为NO)和工业固氮(合成氨)是固氮的重要形式。下表列举了不同温度下大气固氮和工业固氮的部分K值(K表示平衡常数):
| | N2+O2 2NO 2NO | N2+3H2 2NH3 2NH3 | ||
| 温度 | 25℃ | 2000℃ | 25℃ | 400℃ |
| K | 3.84×10-31 | 0.1 | 5×108 | 200 |
 氮的另一途径为 。
氮的另一途径为 。
 高温下,并用铁触媒作为催化剂。俄勒冈大学的化学家使用了一种名为trans-Fe(DMeOPrPE)的新催化剂,在常温下合成氨,反应的化学方程式为:N2 +3H2
高温下,并用铁触媒作为催化剂。俄勒冈大学的化学家使用了一种名为trans-Fe(DMeOPrPE)的新催化剂,在常温下合成氨,反应的化学方程式为:N2 +3H2 2NH3。有关说法正确的是 。
2NH3。有关说法正确的是 。科目:高中化学 来源: 题型:阅读理解
| N2+O2?2NO | N2+3H2?2NH3 | |||
| 温度 | 25℃ | 2000℃ | 25℃ | 400℃ |
| K | 3.84×10-31 | 0.1 | 5×108 | 200 |

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
大气固氮(闪电时N2转化为NO)和工业固氮(合成氨)是固氮的重要形式.下表列举了不同温度下大气固氮和工业固氮的部分K值(K表示平衡常数):
| N2+O2?2NO | N2+3H2?2NH3 | |||
| 温度 | 25℃ | 2000℃ | 25℃ | 400℃ |
| K | 3.84×10-31 | 0.1 | 5×108 | 200 |
(1)固氮是指______的过程,自然界固氮的另一途径为______.
(2)根据表中的数据,并结合所学知识分析,下列说法正确的是______.
a.人类大规模模拟大气固氮实际意义很小
b.常温下,大气固氮与工业固氮完成程度相差很大
c.两种固氮都是放热反应 d.在常温下,大气固氮几乎不可能,而工业固氮很容易进行
(3)为研究反应条件的改变对化学平衡移动的影响,将N2和H2在一固定体积的密闭容器中进行反应,得到如下的图象.下列有关条件改变(每次只改变一个条件)的说法,正确的是______.
a.t2可能是增加了原料的物质的量
b.t4可能是充入了He气
c.t5是从反应体系中分离出氨气
d.t7时可能是升高温度,使平衡向正反应方向移动
(4)目前工业固氮采用的是哈伯法,即在20~50MPa的高压和500℃左右的高温下,并用铁触媒作为催化剂.俄勒冈大学的化学家使用了一种名为trans-Fe(DMeOPrPE)的新催化剂,在常温下合成氨,反应的化学方程式为:N2+3H2?2NH3.有关说法正确的是______.
a.新法不需要高温条件,可节约大量能源
b.新法能在常温下进行是因为不需要断裂化学键
c.在相同温度下不同的催化剂其催化活性不同.
查看答案和解析>>
科目:高中化学 来源:期末题 题型:填空题
 2NO写出该反应的平衡常数表达式:_________
2NO写出该反应的平衡常数表达式:_________ 2NH3和②N2+O2
2NH3和②N2+O2  2NO的平衡常数(K)与温度的关系。根据图中的数据分析,下列说法正确的是( )。
2NO的平衡常数(K)与温度的关系。根据图中的数据分析,下列说法正确的是( )。 
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
大气固氮(闪电时N2转化为NO)和工业固氮(合成氨)是固氮的重要形式。下表列举了不同温度下大气固氮和工业固氮的部分K值(K表示平衡常数):
| N2+O2 | N2+3H2 | |||
| 温度 | 25℃ | 2000℃ | 25℃ | 400℃ |
| K | 3.84×10-31 | 0.1 | 5×108 | 200 |
(1)固氮是指 的过程,自然界固氮的另一途径为 。
(2)根据表中的数据,并结合所学知识分析,下列说法正确的是 。
a.人类大规模模拟大气固氮实际意义很小
b.常温下,大气固氮与工业固氮完成程度相差很大
c.两种固氮都是放热反应 d.在常温下,大气固氮几乎不可能,而工业固氮很容易进行
(3)为研究反应条件的改变对化学平衡移动的影响,将N2和H2在一固定体积的密闭容器中进行反应,得到如下的图像。下列有关条件改变(每次只改变一个条件)的说法,正确的是 。
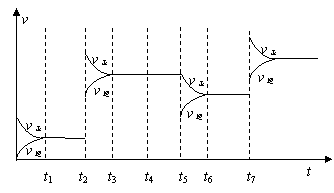 a.t2可能是增加了原料的物质的量
a.t2可能是增加了原料的物质的量
b.t4可能是充入了He气
c.t5是从反应体系中分离出氨气
d.t7时可能是升高温度,使平衡向
正反应方向移动
(4)目前工业固氮采用的是哈伯法,即在
20~50MPa的高压和500℃左右的高温下,并用铁触媒作为催化剂。俄勒冈大学的化学家使用了一种名为trans-Fe(DMeOPrPE)的新催化剂,在常温下合成氨,反应的化学方程式为:N2 +3H2![]() 2NH3 。有关说法正确的是 。
2NH3 。有关说法正确的是 。
a.新法不需要高温条件,可节约大量能源
b.新法能在常温下进行是因为不需要断裂化学键
c.在相同温度下不同的催化剂其催化活性不同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com