
| A. | 遇到苯酚显紫色的溶液:SCN-、Na+、SO32-、Cl- | |
| B. | 含有Na2CO3的溶液:Al3+、Ca2+、Cl-、NO3- | |
| C. | 通入足量CO2的溶液:K+、SiO32-、Cl-、NO3- | |
| D. | 25℃时pH<7的溶液:K+、Cu2+、Fe3+、NO3- |
分析 A.遇到苯酚显紫色的溶液中存在铁离子,铁离子能够与硫氰根离子、亚硫酸根离子反应;
B.钙离子、铝离子都与碳酸钠溶液发生反应;
C.硅酸根离子与二氧化碳反应生成硅酸沉淀;
D.25℃时pH<7的溶液的溶液呈酸性,四种离子之间不反应,都不与氢离子反应.
解答 解:A.遇到苯酚显紫色的溶液中含有Fe3+,Fe3+与SCN-、SO32-反应,在溶液中不能大量共存,故A错误;
B.Al3+、Ca2+与Na2CO3反应,在溶液中不能大量共存,故B错误;
C.SiO32-与CO2发生反应,通入足量CO2后不能大量共存,故C错误;
D.25℃时pH<7的溶液中存在大量H+,K+、Cu2+、Fe3+、NO3-之间不反应,都不与H+反应,在溶液中能够大量共存,故D正确;
故选D.
点评 本题考查离子共存的判断,为高考的高频题,题目难度不大,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间;能发生络合反应的离子之间(如 Fe3+和 SCN-)等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的具体反应条件,如“氧化还原反应”、“加入铝粉产生氢气”等;试题侧重对学生基础知识的训练和检验,有利于培养学生灵活运用基础知识解决实际问题的能力.


 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案科目:高中化学 来源: 题型:推断题
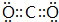 ;C 单质在高温下与B单质充分反应所得化合物的电子式为
;C 单质在高温下与B单质充分反应所得化合物的电子式为 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 8.12天津爆炸事件后,为处理现场散落的剧毒物NaCN,应喷洒双氧水 | |
| B. | 明矾和高铁酸盐都可用于饮用水的处理,因为它们均能杀菌消毒 | |
| C. | 向煤中加入适量石灰石,使煤燃烧产生的SO2最终生成CaSO3,可减少对大气的污染 | |
| D. | 氢氧化铝、碳酸钠都是常见的胃酸中和剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将过量NaOH溶液滴入Ca(HCO3)2溶液中:Ca2++HCO3-+OH-═CaCO3↓+H2O | |
| B. | Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+═Fe3++3H2O | |
| C. | 向硫酸铝铵[NH4Al(SO4)2]溶液中加入氢氧化钡溶液至SO42ˉ离子沉淀完全Al3++2SO42ˉ+2Ba2++4OHˉ═Al(OH)4ˉ+2BaSO4↓ | |
| D. | 向NH4HCO3溶液中加入过量的Ba(OH)2溶液并加热:Ba2++2OH-+NH4++HCO3-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+2H2O+BaCO3↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯元素在自然界中存在游离态,只是量极少 | |
| B. | 海水中的氯元素主要以NaCl等盐的形式存在 | |
| C. | 人体血液中含有NaCl,其浓度大约为0.9% | |
| D. | NaCl对维持人体的生理功能有着重要作用 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe3O4根据化合价规律可表示为FeO•Fe2O3,则Pb3O4也可表示为PbO•Pb2O3 | |
| B. | CaC2能水解:CaC2+2H2O=Ca(OH)2+C2H2↑,则Al4C3也能水解:Al4C3+12H2O=4A1(OH)3↓+3CH4↑ | |
| C. | Cl2与Fe加热生成FeCl3,则I2与Fe加热生成FeI3 | |
| D. | SO2通入BaCl2溶液不产生沉淀,则SO2通入Ba(NO3)2溶液也不产生沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硝酸铵自发地溶于水 | B. | CaO(s)+CO2(g)=CaCO3(s) | ||
| C. | HCl(g)+NH3(g)=NH4Cl(s) | D. | 2H2(g)+O2(g)=2H2O(l) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com