
有X、Y、Z、W、M五种短周期元素,其中X、Y、Z、W同周期, Z、M同主族; X+与M2-具有相同的电子层结构;离子半径:Z2->W-;Y的单质晶体熔点高、硬度大,是一种重要的半导体材料。下列说法中,正确的是
A.X、M两种元素只能形成X2M型化合物
B.元素W和M的某些单质可作为水处理中的消毒剂
C.元素Y、Z、W的单质晶体属于同种类型的晶体
D.由于W、Z、M元素的氢气化物相对分子质量依次减小,所以其沸点依次降低
科目:高中化学 来源: 题型:
镁是一种重要的金属资源,工业上制取镁单质主要是电解法.
(1)电解法制取镁单质的反应方程式是: .
(2)电解原料无水氯化镁可由海水制备.主要有以下步骤:①在一定条件下脱水干燥;②加熟石灰;③加盐酸;④过滤;⑤浓缩冷却结晶.
其步骤先后顺序是 ;(每步骤可重复使用)
(3)上述步骤①中“一定条件下”具体是指: ,其目的是 .
(4)已知某温度下Mg(OH)2的Ksp=6.4×l0﹣12,当溶液中c(Mg2+)≤1.0×10﹣5mol•L﹣1可视为沉淀完全,则此温度下应保持溶液中c(OH﹣)≥ mol•L﹣1.
(5)饱和NH4Cl溶液滴入少量的Mg(OH)2悬浊液中,看到的现象是 .反应原理可能有两方面,请分别用离子方程式表示:① ;② .
要验证①②谁是Mg(OH)2溶解的主要原因,可选取 代替NH4Cl溶液作对照实验.
A.NH4NO3 B.(NH4)2SO4 C.CH3COONH4 D.NH4HCO3
(6)镁电池是近年来科学技术研究的热点之一.一种“镁﹣次氯酸盐”电池的总反应为:
Mg+ClO﹣+H2O═Mg(OH)2+Cl﹣.其工作时正极的电极反应式: ClO﹣+2e﹣+H2O=Cl﹣+2OH﹣ ;用此镁电池给铅蓄电池充电,下列说法中正确的是 .
A.镁电池正极与铅蓄电池正极相连
B.电子从Pb电极转移到镁电池负极
C.充电后,铅蓄电池两极质量均减小,理论上镁电池消耗24g Mg,阴、阳极的质量变化之比为3:2
D.充电后,镁电池和铅蓄电池的pH均增大.
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上合成氨时一般采用700 K左右的温度,其原因是( )
①提高合成氨的速率 ②提高氢气的转化率 ③提高氨的产率 ④催化剂在700 K时活性最大
A.只有① B.①②
C.②③④ D.①④
查看答案和解析>>
科目:高中化学 来源: 题型:
某温度下,在一容积可变的容器中,反应2A(g)+B(g)2C(g)达到平衡时,A、B和C的物质的量分别为4 mol、2 mol和4 mol。保持温度和压强不变,对平衡混合物中三者的物质的量做如下调整,可使平衡右移的是( )
A.均减半 B.均加倍
C.均增加1 mol D.均减少1 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
樱桃是一种抗氧化的水果,对人体有很大的益处,樱桃中含有一种羟基酸
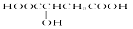 具有健脾作用。下列有关说法正确的是
具有健脾作用。下列有关说法正确的是
A.该羟基酸含有3种官能团
B.通常条件下,该羟基酸可以发生取代、氧化和加成反应
C.该羟基酸可以在Cu的催化下被O2氧化成醛
D.含1mol该羟基酸的溶液可与含2mol氢氧化钠的溶液恰好完全反应
查看答案和解析>>
科目:高中化学 来源: 题型:
有一未知的无色溶液,只可能含有以下离子中的若干种(忽略由水电离产生的H+、OH-):H+、NH4+、K+、Mg2+、Cu2+、Al3+、NO3-、CO32-、SO42-,现取三份100mL溶液进行如下实验:
①第一份加足量AgNO3溶液后,有白色沉淀产生。
②第二份加足量BaCl2溶液后,有白色沉淀产生,经洗涤、干燥后,沉淀质量为6.99 g。
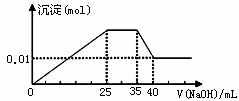
③第三份逐滴滴加NaOH溶液,测得沉淀与NaOH溶液的体积关系如图。根据上述实验,以下推测不正确的是
A.原溶液一定不存在H+、Cu2+、CO32-
B.不能确定原溶液是否含有K+、NO3-
C. 实验所加的NaOH的浓度为2mol·L-1
D. 原溶液确定含Mg2+、Al3+、NH4+,且n(Mg2+)n(Al3+)n( NH4+)=112
查看答案和解析>>
科目:高中化学 来源: 题型:
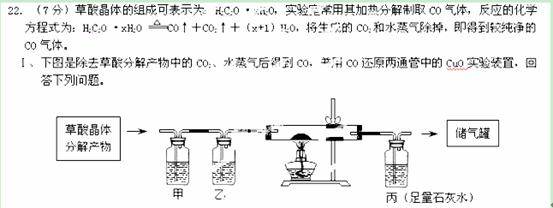
(1)在甲洗气瓶中所盛溶液是 ▲ 。
(2)CuO全部被还原后停止实验操作的步骤的有:①停止通气体,②熄灭酒精灯,③拆下实验装置, ④继续通气体到两通管冷却止。其正确的操作顺序是 ▲ 。
A.④②①③ B.①②③ C.②④①③ D.②④③
Ⅱ、为测定草酸晶体的x值,进行下列实验:
①取wg草酸晶体配成100mL水溶液;
②量取25.00mL草酸溶液置于锥形瓶中,加入适量稀H2SO4后,用浓度为c mol·L-1KMnO4溶液滴定。滴定时,所发生的反应为:
2KMnO4+5H2C2O4+3H2SO4=K2SO4+10CO2↑+2MnSO4+8H2O
请回答下列问题:
(1)实验②中,滴定时,KMnO4溶液应装在 ▲ (填“酸式滴定管”、“碱式滴定管”)中。
(2)判断滴定终点的方法是 ▲ 。若滴定时,前后两次读数分别为a mL和b mL,由此计算出该草酸晶体的x值是 ▲ 。
(3)下列操作会引起测得的x值偏大的是 ▲ (填选项)
A.滴定结束时俯视读数
B.滴定结束后滴定管尖嘴处还有一滴标准液悬而未滴
C.锥形瓶未干燥即装入草酸溶液
D.滴定管用蒸馏水洗净后即装入KMnO4溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:25°C时,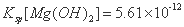 ,
,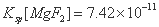 。下列说法正确的是
。下列说法正确的是
A.25°C时,饱和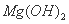 溶液与饱和
溶液与饱和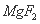 溶液相比,前者的
溶液相比,前者的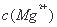 大
大
B.25°C时,在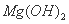 的悬浊液中加入少量的
的悬浊液中加入少量的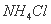 固体,
固体,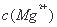 增大
增大
C.25°C时,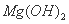 固体在20ml0.01 mol·
固体在20ml0.01 mol·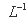 氨水中的Ksp比在20mL 0.01mol·
氨水中的Ksp比在20mL 0.01mol·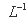
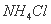 溶液中的Ksp小
溶液中的Ksp小
D.25°C时,在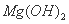 的悬浊液中加入NaF溶液后,不可能有
的悬浊液中加入NaF溶液后,不可能有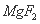 生成
生成
查看答案和解析>>
科目:高中化学 来源: 题型:
请你设计一个能证明铁的金属活动性比铜强的实验。要求:
①此方案能将化学能转化为电能;
②绘出实验装置图并注明所需的药品;
 ③写出实验过程中的主要实验现象。
③写出实验过程中的主要实验现象。
实验装置
实验现象:______________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com