
| A. | 2C2H2(g)+3O2(g)=4CO (g)+2H2O(l)△H=+1468 kJ•mol-1 | |
| B. | 在③反应时,若加入催化剂,可以使△H减小 | |
| C. | 若有3.2g CH4与足量水蒸汽按③反应,则放出热量是43.2 kJ | |
| D. | 若生成相同质量的CO2,则放出的热量C2H2大于CO |
分析 A.依据热化学方程式和盖斯定律计算,依据盖斯定律计算①-②×2得到的热化学方程式分析;
B.催化剂能改变反应速率,但无法改变反应的△H;
C.化学计量数与反应热成正比,根据热化学方程式分析解答;
D.生成相同质量的CO2,结合C2H2和CO燃烧的热化学方程式的反应热进行比较.
解答 解:A.①2C2H2(g)+5O2(g)=4CO2 (g)+2H2O(l)△H=-2600kJ•mol-1
②2CO(g)+O2(g)=2CO2(g)△H=-566kJ•mol-1
依据盖斯定律计算①-②×2得到,2C2H2(g)+3O2(g)=4CO (g)+2H2O(l)△H=-1468 kJ•mol-1故A错误;
B.焓变=反应物断裂化学键吸收的能量-生成物形成化学键放出的能量,在反应体系中加入催化剂,催化剂改变反应速率,不改变化学平衡,反应热不变,故B错误;
C.3.2g CH4的物质的量为n=$\frac{n}{M}$=$\frac{3.2g}{16g/mol}$=0.2mol,CH4(g)+H2O(g)═CO(g)+3H2(g)△H=+216kJ/mol,所以应吸收热量是43.2 kJ,故C错误;
D.假设都生成2molCO2,C2H2燃烧放出1300KJ热量,CO燃烧放出566kJ,前者大于后者,故D正确;
故选D.
点评 本题考查热化学方程式含义及反应热的大小比较,题目难度不大,关键是注意反应热的数值与单位,反应热的数值与化学方程式前面的系数成正比.


科目:高中化学 来源: 题型:选择题
| A. | 反应过程中不可能产生H2 | |
| B. | 剩余的金属粉末中一定有铜 | |
| C. | 往反应后的溶液中加入KSCN 溶液会变血红色 | |
| D. | 往反应后的溶液中加入足量的稀H2SO4,则金属粉末的质量一定会减少 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 ,
,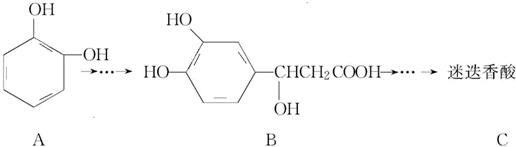
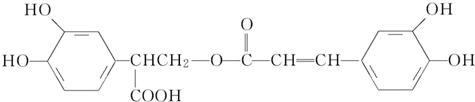
| A. | 有机物B可以发生取代、加成、消去、氧化反应 | |
| B. | 有机物A分子中所有原子一定在同一平面上 | |
| C. | 有机物C在浓硫酸催化下水解的一种产物是B | |
| D. | 1 mol B与足量的NaOH溶液反应,最多可消耗4 mol NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | X2YZ3 | B. | X2YZ4 | C. | X3YZ4 | D. | X4Y2Y7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| ① | ② | ③ | 实验结论 |  | |
| A | 硫酸 | 碳酸钠 | 硅酸钠溶液 | 非金属性:S>C>Si | |
| B | 硝酸 | 碳酸钠 | 苯酚钠溶液 | 酸性:硝酸>碳酸>苯酚 | |
| C | 盐酸 | 二氧化锰 | 溴化钾溶液 | 氧化性:二氧化锰>氯气>液溴 | |
| D | 溴的苯溶液 | 铁屑 | 硝酸银溶液 | 苯和溴单质在铁的催化剂作用下发生取代反应 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 最简式为C2H4O的有机物一定可以发生银镜反应 | |
| B. | 不粘锅表面的高分子涂层可以由四氟乙烯通过缩聚反应合成 | |
| C. | 分子结构中含有4个甲基、碳原子数最少的烷烃的系统命名为:2,2-二甲基丙烷 | |
| D. | 甘油和甲苯只有在物质的量之比1:1混合时,充分燃烧后生成的水,才与等质量的甘油充分燃烧后生成的水相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ①②④ | C. | ①③④ | D. | ②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | Fe2+、Na+、SCN-、Cl- | B. | Ca2+、Cu2+、NO3-、SO32- | ||
| C. | Na+、Ba2+、Cl-、HCO3- | D. | Al3+、Na+、SO42-、NO3- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com