
����Ŀ������þ��![]() ��Ҫ�ɷ�Ϊ
��Ҫ�ɷ�Ϊ![]() ��������
��������![]() ��
��![]() ��ȡ����Ĺ�������Ϊ��
��ȡ����Ĺ�������Ϊ��
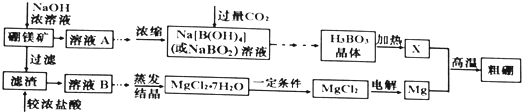
��֪��![]() ���������������ƣ�Ҳ��������������Һ��Ӧ��
���������������ƣ�Ҳ��������������Һ��Ӧ��
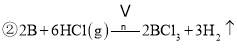
![]() ���۵�Ϊ
���۵�Ϊ![]() ���е�Ϊ
���е�Ϊ![]() ���ڳ�ʪ���������γɰ�����
���ڳ�ʪ���������γɰ�����
I.�ش��������⣺
![]() ֤����ҺB�к�����Ԫ�صķ����� ______
֤����ҺB�к�����Ԫ�صķ����� ______
![]() ��X��Ӧ��ȡ����Ļ�ѧ����ʽ ______
��X��Ӧ��ȡ����Ļ�ѧ����ʽ ______
![]() ��ͼ����ȡ
��ͼ����ȡ![]() ����һ����������ָ ______
����һ����������ָ ______
![]() ijͬѧ�����ͼ��ʾװ���Ʊ����Ȼ���
ijͬѧ�����ͼ��ʾװ���Ʊ����Ȼ���

�ش��������⣺
![]() װ�õ������� ______ ��
װ�õ������� ______ ��
![]() ���ȥ��Bװ�ã����ܵĺ���� ______ ��
���ȥ��Bװ�ã����ܵĺ���� ______ ��

![]() װ�ú��滹Ӧ���ӵ�һ��װ���� ______ ��
װ�ú��滹Ӧ���ӵ�һ��װ���� ______ ��
���𰸡�ȡ������ҺB���Թ��У��μӼ���KSCN��Һ����Һ���ɫ��˵������FeԪ�� 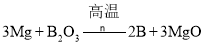 HCl��Χ������ ��ȴ���ռ�
HCl��Χ������ ��ȴ���ռ�![]() ����ʱB��HCl��Ӧ���ɵ��������������������ը d
����ʱB��HCl��Ӧ���ɵ��������������������ը d
��������
I.��þ����Ҫ�ɷ�Ϊ![]() �����Կ���
�����Կ���![]() ��������������
��������������![]() ��
��![]() ����Ũ����������Һ�ܽ⣬
����Ũ����������Һ�ܽ⣬![]() ��
��![]() ���������Ʒ�Ӧ�õ�
���������Ʒ�Ӧ�õ�![]() ��
��![]() ����MgO��
����MgO��![]() �����������Ʒ�Ӧ�����˵õ�����ΪMgO��
�����������Ʒ�Ӧ�����˵õ�����ΪMgO��![]() ����ҺA��Ϊ
����ҺA��Ϊ![]() ��
��![]() ��ʣ���NaOH��Ũ����ͨ������Ķ�����̼������ϵ�в����õ�
��ʣ���NaOH��Ũ����ͨ������Ķ�����̼������ϵ�в����õ�![]() �����ȵõ�
�����ȵõ�![]() ������Mg�����û���Ӧ��Ӧ�õ�B��MgO��
������Mg�����û���Ӧ��Ӧ�õ�B��MgO��
�����������Ũ���ᷴӦ�õ���ҺB����![]() ��
��![]() ��δ��Ӧ��HCl����������þ�ȵ�����ҺpH��ʹ��Һ��������ת��Ϊ���������������ٹ��˳�ȥ����Һ���������ᾧ�õ�
��δ��Ӧ��HCl����������þ�ȵ�����ҺpH��ʹ��Һ��������ת��Ϊ���������������ٹ��˳�ȥ����Һ���������ᾧ�õ�![]() ����HCl��Χ�¼��ȷֽ�õ�
����HCl��Χ�¼��ȷֽ�õ�![]() ���Է�ֹ�Ȼ�þˮ�⣬�ٵ�����ڵ�
���Է�ֹ�Ȼ�þˮ�⣬�ٵ�����ڵ�![]() �õ�����Mg��������
�õ�����Mg��������![]() ����ҺB�к��е���Ԫ����
����ҺB�к��е���Ԫ����![]() ��ʽ���ڣ���KSCN��Һ���м��飻
��ʽ���ڣ���KSCN��Һ���м��飻
��![]() �ڳ�ʪ���������γɰ�������ˮ����ˮ�ⷴӦ��Ӧ����ˮ�����½��У�װ��A�Ʊ��������Ʊ��������к��лӷ�����HCl������B��HCl���Է�����Ӧ��
�ڳ�ʪ���������γɰ�������ˮ����ˮ�ⷴӦ��Ӧ����ˮ�����½��У�װ��A�Ʊ��������Ʊ��������к��лӷ�����HCl������B��HCl���Է�����Ӧ��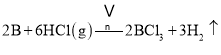 �����ɵ�����������������ը��Bװ������HCl��Cװ�����ڸ���������Dװ����B��������Ӧ����
�����ɵ�����������������ը��Bװ������HCl��Cװ�����ڸ���������Dװ����B��������Ӧ����![]() ������
������![]() �ķе�ϵͣ���Ӧ�õ�Ϊ��̬
�ķе�ϵͣ���Ӧ�õ�Ϊ��̬![]() ��Eװ�����ñ�ˮ��ȴ�ռ��õ�Һ��
��Eװ�����ñ�ˮ��ȴ�ռ��õ�Һ��![]() ������δ��Ӧ����������Ⱦ��������Ҫ��Eװ��֮��������������װ�ã�ͬʱ��ֹ�����е�ˮ��������D�У���ֹ
������δ��Ӧ����������Ⱦ��������Ҫ��Eװ��֮��������������װ�ã�ͬʱ��ֹ�����е�ˮ��������D�У���ֹ![]() ����ˮ�⡣
����ˮ�⡣
![]() ��þ����Ҫ�ɷ�Ϊ
��þ����Ҫ�ɷ�Ϊ![]() �����Կ���
�����Կ���![]() ��������������
��������������![]() ��
��![]() ����Ũ����������Һ�ܽ⣬
����Ũ����������Һ�ܽ⣬![]() ��
��![]() ���������Ʒ�Ӧ�õ�
���������Ʒ�Ӧ�õ�![]() ��
��![]() ����MgO��
����MgO��![]() �����������Ʒ�Ӧ�����˵õ�����ΪMgO��
�����������Ʒ�Ӧ�����˵õ�����ΪMgO��![]() ����ҺA��Ϊ
����ҺA��Ϊ![]() ��
��![]() ��ʣ���NaOH��Ũ����ͨ������Ķ�����̼������ϵ�в����õ�
��ʣ���NaOH��Ũ����ͨ������Ķ�����̼������ϵ�в����õ�![]() �����ȵõ�
�����ȵõ�![]() ������Mg�����û���Ӧ��Ӧ�õ�B��MgO��
������Mg�����û���Ӧ��Ӧ�õ�B��MgO��
�����������Ũ���ᷴӦ�õ���ҺB����![]() ��
��![]() ��δ��Ӧ��HCl����������þ�ȵ�����ҺpH��ʹ��Һ��������ת��Ϊ���������������ٹ��˳�ȥ����Һ���������ᾧ�õ�
��δ��Ӧ��HCl����������þ�ȵ�����ҺpH��ʹ��Һ��������ת��Ϊ���������������ٹ��˳�ȥ����Һ���������ᾧ�õ�![]() ����HCl��Χ�¼��ȷֽ�õ�
����HCl��Χ�¼��ȷֽ�õ�![]() ���Է�ֹ�Ȼ�þˮ�⣬�ٵ�����ڵ�
���Է�ֹ�Ȼ�þˮ�⣬�ٵ�����ڵ�![]() �õ�����Mg��������
�õ�����Mg��������
![]() ����ҺB�к��е���Ԫ����
����ҺB�к��е���Ԫ����![]() ��ʽ���ڣ���KSCN��Һ���м��飬�������Ϊ��ȡ������ҺB���Թ��У��μӼ���KSCN��Һ����Һ���ɫ��˵������FeԪ�أ�
��ʽ���ڣ���KSCN��Һ���м��飬�������Ϊ��ȡ������ҺB���Թ��У��μӼ���KSCN��Һ����Һ���ɫ��˵������FeԪ�أ�
�ʴ�Ϊ��ȡ������ҺB���Թ��У��μӼ���KSCN��Һ����Һ���ɫ��˵������FeԪ�أ�
![]() ��
��![]() �õ�B��MgO����Ӧ����ʽΪ��
�õ�B��MgO����Ӧ����ʽΪ��![]() ��
��
�ʴ�Ϊ��![]() ��
��
![]() ��HCl��Χ�¼��ȷֽ�õ�
��HCl��Χ�¼��ȷֽ�õ�![]() ���Է�ֹ�Ȼ�þˮ�⣬
���Է�ֹ�Ȼ�þˮ�⣬
�ʴ�Ϊ��HCl��Χ�����ȣ�
��![]() �ڳ�ʪ���������γɰ�������ˮ����ˮ�ⷴӦ��Ӧ����ˮ�����½��У�װ��A�Ʊ��������Ʊ��������к��лӷ�����HCl������B��HCl���Է�����Ӧ��
�ڳ�ʪ���������γɰ�������ˮ����ˮ�ⷴӦ��Ӧ����ˮ�����½��У�װ��A�Ʊ��������Ʊ��������к��лӷ�����HCl������B��HCl���Է�����Ӧ��![]() �����ɵ�����������������ը��Bװ������HCl��Cװ�����ڸ���������Dװ����B��������Ӧ����
�����ɵ�����������������ը��Bװ������HCl��Cװ�����ڸ���������Dװ����B��������Ӧ����![]() ������
������![]() �ķе�ϵͣ���Ӧ�õ�Ϊ��̬
�ķе�ϵͣ���Ӧ�õ�Ϊ��̬![]() ��Eװ�����ñ�ˮ��ȴ�ռ��õ�Һ��
��Eװ�����ñ�ˮ��ȴ�ռ��õ�Һ��![]() ������δ��Ӧ����������Ⱦ��������Ҫ��Eװ��֮��������������װ�ã�ͬʱ��ֹ�����е�ˮ��������D�У���ֹ
������δ��Ӧ����������Ⱦ��������Ҫ��Eװ��֮��������������װ�ã�ͬʱ��ֹ�����е�ˮ��������D�У���ֹ![]() ����ˮ�⣮
����ˮ�⣮
![]() ������������֪��Eװ�õ������ǣ���ȴ���ռ�
������������֪��Eװ�õ������ǣ���ȴ���ռ�![]() ���ʴ�Ϊ����ȴ���ռ�
���ʴ�Ϊ����ȴ���ռ�![]() ��
��
![]() װ������HCl����ȥ��Bװ�ã�B��HCl���Է�����Ӧ��
װ������HCl����ȥ��Bװ�ã�B��HCl���Է�����Ӧ��![]() �����ɵ�����������������ը��
�����ɵ�����������������ը��
�ʴ�Ϊ������ʱB��HCl���Է�����Ӧ��![]() �����ɵ��������������������ը��
�����ɵ��������������������ը��
�ʴ�Ϊ������ʱB��HCl��Ӧ���ɵ��������������������ը��
![]() ����δ��Ӧ����������Ⱦ������
����δ��Ӧ����������Ⱦ������![]() ��ˮ����ˮ�⣬����Ҫ��Eװ��֮��������������װ�ã�ͬʱ��ֹ�����е�ˮ��������D�У���ֹ
��ˮ����ˮ�⣬����Ҫ��Eװ��֮��������������װ�ã�ͬʱ��ֹ�����е�ˮ��������D�У���ֹ![]() ����ˮ�⣬
����ˮ�⣬
a��Ũ���������ʣ���������bc������ˮ��ˮ�������Խ���E�У�����![]() ����ˮ�⣬d�м�ʯ�ҿ������������������ˮ��������ѡ��d��
����ˮ�⣬d�м�ʯ�ҿ������������������ˮ��������ѡ��d��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ�ϳ��õ����������Һ��������������ռ���Һ��װ����ͼ��ʾ������������������Ϊ���Ե缫�����ͬ��ͬѹ�£�������������ҵ������ԼΪ2:1������˵����ȷ���� ( )
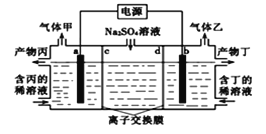
A. b�缫��Ӧʽ��2H2O+4e-=O2��+4H+
B. ���ӽ���ĤdΪ�����ӽ���Ĥ
C. ��Ϊ������Һ����Ϊ����������Һ
D. a�缫���ӵ�Դ������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ�����������ʯβ��(��Ҫ�ɷ�ΪMgO������FeO��Fe2O3��Al2O3��)�Ʊ������Ȼ�þ����(MgCl2��6H2O)��ʵ���������£�

��֪���ֽ����������γ������������ʱ��pH���±���
Fe2+ | Fe3+ | Al3+ | Mg2+ | |
��ʼ����ʱ | 7.6 | 2.7 | 4.2 | 9.6 |
������ȫʱ | 9.6 | 3.7 | 5.4 | 11.1 |
�ش��������⣺
(1)����ȡ�������У��ܼӿ��ȡ���ʵķ�����____________��__________(��д����)��
(2)����X�ĵ���ʽΪ________������1�������������Ƶ�һ�ָ�Ч�����߷��ӻ���������ˮ�����仯ѧʽΪ[Fe2(OH)n(SO4)(3��0.5n)]m�������������Ԫ�صĻ��ϼ�Ϊ________��
(3)����H2O2��Ŀ����______________________���������������е���H2O2������NaClO������Ҳ�ܴﵽͬ��Ŀ�ģ�������Ӧ�����ӷ���ʽΪ��________________________________��
(4)��һϵ�в�������Ҫ���������������ᣬȻ��____________________�����ˡ�ϴ�ӣ����õ��Ȼ�þ���塣
(5)ȷ��ȡ2.000 g�Ȼ�þ�����Ʒ��250 mL��ƿ�У���ˮ50 mLʹ����ȫ�ܽ⣬����100 mL���Ի���Һ����������Tָʾ������Һ�Ծƺ�ɫ���ڲ������£���0.5000 mol/L��EDTA����Һ���еζ����䷴Ӧԭ��ΪMg2+��Y4- ==MgY2-���ζ��յ�ʱ����EDTA����Һ�����19.00 mL��
�����Ʒ��MgCl2��6H2O����������Ϊ________(���������λ��Ч����)��
�����еζ������ᵼ�²������ƫ�ߵ���________(����ĸ)��
a���ζ��յ�ʱ���Ӷ��� b����ƿϴ�Ӻ�û�и���
c���ζ�ʱ��ƿ����Һ�彦�� d���ζ��ܵζ�ǰ�����ݣ��ζ���������ʧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���о�������FeCl3��Һ����ɫ��Ӧ��ʵ�����¡�����˵������ȷ����
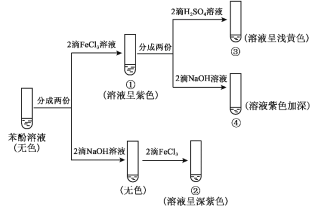
A.�ԱȢ٢��е�����˵���μ�ϡ�����c(Fe3+)��С
B.���Թܢ��еμ���������������Һ��ɫ��Ϊdz��ɫ
C.�ԱȢ٢ڡ��٢��е�����˵����ɫ���ʵ���������Һ�� c(C6H5O)���
D.�ԱȢ٢ڡ��٢��е�����˵�����C6H5O��������H+��Fe3+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����õ������Һ��Ũ�ȶԵ缫���Ƶ�Ӱ�죬�����Ũ���ء�ij������Ũ���ع���ԭ����ͼ��ʾ��ͨ��NH3ʱ��ؿ�ʼ���������缫�������٣��Ҳ�缫�������ӣ��м�AΪ�����ӽ���Ĥ���ŵ������÷��Ƚ��г����������֪��Cu2+��4NH3![]()
![]() ������˵������ȷ����
������˵������ȷ����
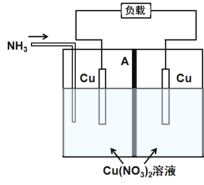
A.�ŵ�ʱ�����缫����������Ӧ��Cu��4NH3-2e��![]()
B.�ŵ�ʱ����ص��ܷ�ӦΪCu2����4NH3![]()
![]() ����H��0
����H��0
C.�ŵ�ʱ��![]() �����ӽ���Ĥ���Ҳ������Ǩ��
�����ӽ���Ĥ���Ҳ������Ǩ��
D.����ԭ��ص��γ�˵������ͬ�����£�![]() �������Ա�Cu2������������
�������Ա�Cu2������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ˮ��һ����Ҫ����Ȼ��Դ��ˮ������ֱ��Ӱ�����彡����ˮ����������������������Ӧ�ù㷺���ۺ�������(PFS)��ˮ��������Ҫ�����������Ի����������(��Ҫ�ɷ�ΪFe2O3��FeO��SiO2��)�ͷ���мΪԭ����ȡ�ۺ�������([Fe2(OH)x(SO4)3-![]() ]m)�Ĺ���������ͼ��
]m)�Ĺ���������ͼ��
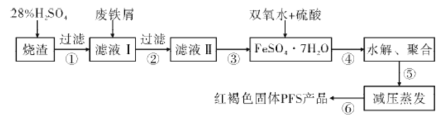
(1)��98%����������28%�����ᣬ����IJ�����������Ͳ�⣬����______(���ţ���
a.����ƿ b.�ձ� c.������ d.��Һ©��
(2)����м���渽�����⣬�������Ҫ�ɷ�Ϊ______������۵ľ���ʵ�������____��
(3)ˮ�⡢�ۺ�Ҫ�Ͽ�pH���¶ȡ�pHƫСʱFe3+ˮ��̶�����pHƫ��ʱ��______��д��ˮ�⡢�ۺϷ�Ӧ����PFS�Ļ�ѧ����ʽ��_________��
(4)���������ڳ�ѹ��������ѹ�������ŵ���_________��
(5)��ˮ����һ����������������������Cu2+��Hg2+��Pb2+���ؽ������ӣ��ɼ��������ʹ�������������������Ϊ����������_______�����ţ���
a.��ˮ b.�������� c.��������Һ d.������Һ
(6)Ӳ��Ϊ1����ˮ��ָÿ��ˮ��10mgCaO����֮�൱������(��7.1mgMgO)����ij��Ȼˮ��c(Ca2+)=1.5��10-3mol/L��c(Mg2+)=6.4��10-4mol/L�����ˮ��Ӳ��Ϊ______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ȼҵ��ԭ��ʾ��ͼ��ͼ������˵����ȷ����
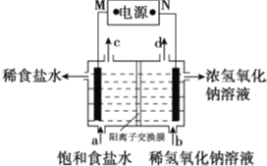
A. M����
B. ͨ��ʹ�Ȼ��Ʒ�������
C. ����c�ռ���������������
D. ͨ��һ��ʱ���������pH����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������������п�̸ɵ�صĻ������ϡ���ҵ�������̿�Ϊԭ�ϣ��������������Ʊ��ߴ��ȶ������̵�������ͼ1��
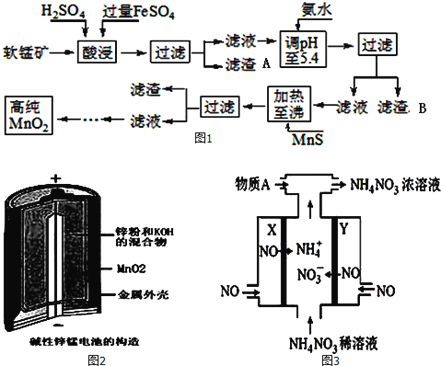
ij���̿����Ҫ�ɷ�ΪMnO2��������Si��16.27%����Fe��5.86%����Al��3.42%����Zn��2.68%����Cu��0.86%����Ԫ�صĻ��������������������������������ʽ��ȫ����ʱ��Һ��pH������ش���������
������ | Al��OH��3 | Fe��OH��3 | Fe��OH��2 | Mn��OH��2 | Cu��OH��2 | Zn��OH��2 | CuS | ZnS | MnS | FeS |
pH | 5.2 | 3.2 | 9.7 | 10.4 | 6.7 | 8.0 | ��-0.42 | ��2.5 | ��7 | ��7 |
��1���������������������½�MnO2��ԭΪMnSO4�����ʱ��������Ҫ��Ӧ�Ļ�ѧ����ʽΪ__________��
��2������A����Ҫ�ɷ���____________������B����Ҫ�ɷ���__________________��
��3������MnS��Ŀ���dz�ȥCu2+��Zn2+���ʣ�����ԭ����_________________��
��4������п�̵����һ��һ���Ե�أ���ṹ��ͼ2��ʾ���õ�طŵ���̲���MnOOH���õ�ص�������ӦʽΪ________________������ܷ�Ӧ�ķ���ʽΪ_______________________��
��5�����øü���п�̵�ص��NO�Ʊ�NH4NO3���乤��ԭ����ͼ3��ʾ��X�缫__________�������ʱ�����ĵ缫��ӦΪ________________��ʹ������ȫ��ת��ΪNH4NO3���貹������A��A��__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���״���Ϊȼ�ϣ��ڻ�ʯ��Դ�Ϳ�������Դʱ�ھ��й㷺��Ӧ��ǰ����
I. �״�����������ͺͲ�����Ϊ��ȼ��ȼ�ϡ�
��1�����͵���Ҫ�ɷ�֮һ������[C8H18(l)]����֪��25�桢101 kPaʱ��1 mol C8H18(l)��ȫȼ��������̬������̼��Һ̬ˮ���ų�5518 kJ�������÷�Ӧ���Ȼ�ѧ����ʽΪ______��
��2����֪��25�桢101 kPaʱ��CH3OH(l) + 3/2 O2(g) ==== CO2 (g) + 2H2O(l) �� H��-726.5 kJ/mol����ͬ�����ļ״�������ֱ���ȫȼ��ʱ���ų������϶����______��
��3��ij�о��߷ֱ��Լ״���������ȼ�ϣ�ʵ�����ڷ������߸��ɹ�������£�����β����CO�İٷֺ����������ļ������ܵĹ�ϵ������ʾ��
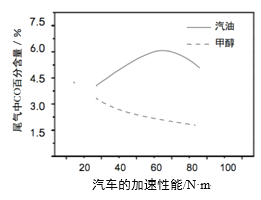
����ͼ��Ϣ��������������ȣ��״���Ϊȼ�ϵ��ŵ���______��
II. �״��ĺϳ�
��4����CO2(g)��H2(g)Ϊԭ�Ϻϳɼ״�����Ӧ�������仯����ͼ��ʾ��

�� ��ȫ��ͼ��ͼ��A��Ӧ����______��
�� �÷�Ӧ��Ҫ����ͭ��п����������������÷�Ӧ�Ħ�H______��������С�����䡱����
��5����֪�� CO(g)��1/2 O2(g) ==== CO2(g) ��H1��-283 kJ/mol
H2(g)��1/2 O2(g) ==== H2O(g) ��H2��-242 kJ/mol
CH3OH(g) + 3/2 O2(g) ==== CO2 (g) + 2H2O(g) ��H3��-676 kJ/mol
��CO(g)��H2(g)Ϊԭ�Ϻϳɼ״��ķ�ӦΪCO(g) + 2H2(g) ==== CH3OH(g) ���÷�Ӧ�Ħ�HΪ_____ kJ/mol��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com