
��֪A(g)+B(g)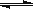 C(g)+D(g)��Ӧ��ƽ�ⳣ�����¶ȵĹ�ϵ���£�
C(g)+D(g)��Ӧ��ƽ�ⳣ�����¶ȵĹ�ϵ���£�
| |�¶�/�� | 700 | 900 | 830 | 1000 | 1200 |
| ƽ�ⳣ�� | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
�ش��������⣺
(1)�÷�Ӧ��ƽ�ⳣ������ʽK=������������������ ������H���������� 0���<���� >���� =��)��
(2) 830��ʱ����һ�� 5 L���ܱ������г���0.20mol��A��0.80mol��B���練Ӧ��ʼ6s��A��ƽ����Ӧ����v(A)=0��003mol��L-1��s-1������6sʱc(A)= �� ��������mol��L-1��C�����ʵ���Ϊ�������� mol����Ӧ��һ��ʱ���ﵽƽ��,��ʱA��ת����Ϊ���� �������������������ʱ����ܱ��������ٳ���1 mol�����ƽ��ʱA��ת����Ϊ���������������� ��������
(3)�жϸ÷�Ӧ�Ƿ�ﵽƽ�������Ϊ�������������� (����ȷѡ��ǰ����ĸ)��������
����a��ѹǿ����ʱ��ı䡡���� b.������ܶȲ���ʱ��ı�
����c. c(A)����ʱ��ı䡡������ d.��λʱ��������C��A�����ʵ�����ȡ�����
(4)1200��ʱ��ӦC(g)+D(g)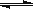 A(g)+B(g)��ƽ�ⳣ����ֵΪ������������ ����������
A(g)+B(g)��ƽ�ⳣ����ֵΪ������������ ����������

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
������ʵ��������ɳ����ԭ�����͵���( )
A����H2��I2������HI��ɵ�ƽ����ϵ��ѹ����ɫ����
B������ѹǿ��������SO2��O2��Ӧ����SO3
C�����ű���ʳ��ˮ���ռ�Cl2
D����ҵ��ȡ������Na(l)+ KCl(l)  NaCl(l)+ K(g)ѡ���˵��¶ȣ�ʹK�������ӷ�Ӧ������з������
NaCl(l)+ K(g)ѡ���˵��¶ȣ�ʹK�������ӷ�Ӧ������з������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�������ӷ���ʽ����ȷ����
A��̼�������Һ�����ᷴӦ��Ca(HCO3)2 + 2H+ = Ca2+ + 2H2O + 2CO2��
B��Ca(HCO3)2��Һ������NaOH��Һ��Ӧ��HCO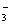 + Ca2��+ OH��= CaCO3��+ H2O
+ Ca2��+ OH��= CaCO3��+ H2O
C��������������Һ�м�������Һ��Ba2����SO42- + H+ + OH- === BaSO4��+ H2O
D����NaHSO4��Һ�еμ�������Ba(OH)2��Һ: Ba2+ + OH- + H+ + SO42- = BaSO4��+ H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���ܱ�����,��ӦaA(g)  bB(g)��ƽ���,�����¶Ȳ���,�������������һ��,�ﵽ��ƽ��ʱ,BŨ����ԭ����60%,��������
bB(g)��ƽ���,�����¶Ȳ���,�������������һ��,�ﵽ��ƽ��ʱ,BŨ����ԭ����60%,��������
A.ƽ��������Ӧ�����ƶ��� B.����A��ת���ʼ�����
C.����B���������������� D. a>b
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�ں��º�ѹ���ܱ������У����� 4L X�� 3L Y�Ļ�����壬��һ�������·������з�Ӧ��
4X��g���� 3Y��g��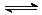 2Q��g���� nR��g���ﵽƽ��ʱ��� X��ת����Ϊ 25������ʱ���
2Q��g���� nR��g���ﵽƽ��ʱ��� X��ת����Ϊ 25������ʱ���
��������Ϊ6.5L����÷�Ӧ����ʽ�е�nֵΪ�� �� ��
A��8 B��6 C��5 D��3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���й���ͬ���칹�塢ͬϵ�ͬ�������塢ͬλ�ص�˵���д������
A����������������Ϊͬ���칹�� B.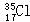 ��
��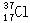 ��Ϊͬλ��
��Ϊͬλ��
B�������������Ϊͬ�������� D. ��ϩ�����ϩ��Ϊͬϵ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��һ����������ͨ��30 mLŨ��Ϊ10.00 mol/L����������Ũ��Һ�У���������ʱ�����Һ���γ�NaCl��NaClO��NaClO3������ϵ�������ж���ȷ����
A����NaOH��Ӧ������һ��Ϊ0.3 mol
B������Ӧ��ת�Ƶĵ���Ϊn mol����0.15��n��0.25
C��n��Na+����n��Cl-������Ϊ7��3
D��n��NaCl����n��NaClO����n��NaClO3������Ϊ8��2��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���л�ѧʵ��ʱ����ע�ⰲȫ������˵������ȷ���ǣ�������
�ٲ������ὦ�����У�Ӧ�����ô���ˮ��ϴ����ϴ��գ�۾���
�ڲ�����Ũ����Һմ��Ƥ���ϣ�Ҫ�����ô���ˮ��ϴ��Ȼ��Ϳ��������Һ��
�۲�����Ũ�������������ϣ�Ӧ������Ũ����������Һ��ϴ��
������ϡ����ʱ����������Ͳ�м���һ�������ˮ�����ڽ�������������Ũ���
�ݾƾ����Ż�ʱ����ˮ����
A���٢ڢ� B���ڢۢ� C���ۢܢ� D��ȫ����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com