
(1)配平化学方程式:![]() 氧化剂是____①____;还原剂是____②____.
氧化剂是____①____;还原剂是____②____.
(2)设X、Y、Z代表3种元素.已知:①X+和Y-两种离子具有相同的电子层结构;②Z元素原子核内质子数比Y元素原子核内质子数少9个;③Y和Z两元素可以形成四核42个电子的负一价阴离子.据此,请填空:
(Ⅰ)Y元素是________,Z元素是________.
(Ⅱ)由X、Y、Z三元素所形成的含68个电子的盐类化合物之分子式(即化学式)是________.
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:志鸿系列全优设计必修一化学人教版 人教版 题型:043
焊接金属时常用的焊接液为氯化铵,其作用是消除焊接金属表面的铁锈.
(1)配平化学方程式:
![]() Fe2O3+
Fe2O3+![]() NH4Cl→
NH4Cl→![]() Fe+
Fe+![]() FeCl3+
FeCl3+![]() N2↑+
N2↑+![]() H2O
H2O
(2)上述反应中________被氧化,当生成2.24 L氮气(标准状况)时,发生转移的电子数目是________.
(3)有同学认为,该反应产物中不可能有Fe生成,其原因是________.
查看答案和解析>>
科目:高中化学 来源:上海市南汇中学2012届高三第一次考试化学试题 题型:022
为了防止枪支生锈,常将枪支的钢铁零件放在NaNO2和NaOH的混合液中进行化学处理经处理后钢铁零件表面生成Fe3SO4的致密的保护层——“发蓝”.主要反应如①②③:
①3Fe+NaNO2+5NaOH→3NaFeO2+NH3+H2O
②________Na2FeO2+________NaNO2+________H2O→________Na2Fe2O4+________NH3+________NaOH
③Na2FeO2+Na2Fe2O4+2H2O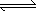 Fe3O4+4NaOH
Fe3O4+4NaOH
(1)配平化学方程式②,标出电子转移方向和数目.
(2)上述反应②中还原剂为________,被还原物质是________.若有1 mol Na2Fe2O4生成,则反应中有________mol电子转移.
(3)当NaOH溶液浓度过大,“发蓝”的厚度会变小,其原因是:________.
查看答案和解析>>
科目:高中化学 来源:黑龙江省哈师大附中2010届高三上学期第一次月考化学试题 题型:022
KClO3和浓盐酸在一定温度下反应会生成黄绿色的易爆物二氧化氯.其变化可
表述为:
□KClO3+□HCl(浓)-□KCl+□Cl2↑+□ClO2↑+□________
(1)配平化学方程式并标出电子转移的方向和数目(未知物化学式和系数填入框内)
(2)浓盐酸在反应中显示出来的性质是________(填写编号,多选倒扣).
①只有还原性
②还原性和酸性
③只有氧化性
④氧化性和酸性
(3)产生0.1 mol Cl2,则转移的电子的物质的量为________.
(4)ClO2具有很强的氧化性.因此,常被用作消毒剂,其消毒的效率(以单位物质的量得到的电子数表示)是Cl2的________倍.
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)配平化学方程式:?
Fe2O3+ NH4Cl→ Fe+ FeCl3+ N2↑+ H2O
(2)上述反应中_______被氧化,当生成2.24 L氮气(标准状况)时,发生转移的电子数目是_______。?
(3)有同学认为,该反应产物中不可能有Fe生成,其原因是________________。?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com