
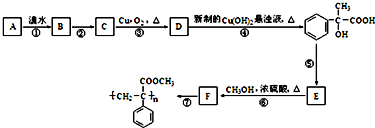
 .
.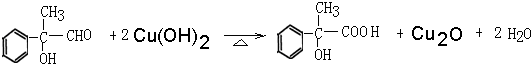 .
.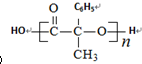 .
. .
.分析 D与新制备氢氧化铜反应产物可知D应为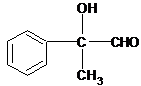

 ,则A为
,则A为

 ,A发生加成得B,B水解得C,C氧化得D,D氧化得
,A发生加成得B,B水解得C,C氧化得D,D氧化得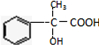 ,
, 发生消去得E,E发生酯化得F,F发生加聚得最终产物,结合有机物的结构和性质解答该题.
发生消去得E,E发生酯化得F,F发生加聚得最终产物,结合有机物的结构和性质解答该题.
解答 解:D与新制备氢氧化铜反应产物可知D应为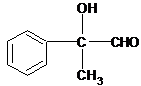

 ,则A为
,则A为

 ,A发生加成得B,B水解得C,C氧化得D,D氧化得
,A发生加成得B,B水解得C,C氧化得D,D氧化得 ,
, 发生消去得E,E发生酯化得F,F发生加聚得最终产物,
发生消去得E,E发生酯化得F,F发生加聚得最终产物,
(1)根据上面的分析可知,反应①到⑥中消去反应是⑤,
故答案为:⑤;
(2)反应②为 的碱性水解,所以反应②的条件为NaOH水溶液,加热,
的碱性水解,所以反应②的条件为NaOH水溶液,加热,
故答案为:NaOH水溶液,加热;
(3)根据上面的分析可知,A为
故答案为:
(4)反应④为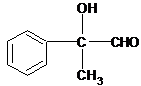
 ,
,
故答案为: ;
;
(5) 发生消去得E,
发生消去得E, 也可以发生缩聚反应生成
也可以发生缩聚反应生成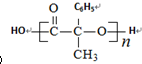 ,故在E的粗产物中,经检测含有高分子聚合物杂质为
,故在E的粗产物中,经检测含有高分子聚合物杂质为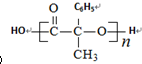 ,
,
故答案为: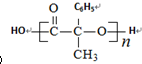 ;
;
(6)E为 ,根据条件Ⅰ.苯环上的一元取代物只有两种结构,说明有两个不同的基团位于苯环的对位;Ⅱ.能发生银镜反应,说明有醛基;Ⅲ.与氯化铁溶液发生显色反应,说明有酚羟基,所以符合条件的E的一种同分异构体的结构简式为
,根据条件Ⅰ.苯环上的一元取代物只有两种结构,说明有两个不同的基团位于苯环的对位;Ⅱ.能发生银镜反应,说明有醛基;Ⅲ.与氯化铁溶液发生显色反应,说明有酚羟基,所以符合条件的E的一种同分异构体的结构简式为 ,
,
故答案为: .
.
点评 本题考查有机物的推断,题目难度中等,解答本题的关键是以 为突破口进行推断,注意官能团的变化和反应的条件.
为突破口进行推断,注意官能团的变化和反应的条件.


科目:高中化学 来源: 题型:选择题
| A. | 工业生产硫酸的过程中使用过量的氧气,以提高二氧化硫的转化率 | |
| B. | 合成氨工厂通常采用20MPa~50MPa压强,以提高原料的利用率 | |
| C. | 实验室用排饱和食盐水的方法收集氯气 | |
| D. | 用铁触媒作催化剂加快化学反应速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
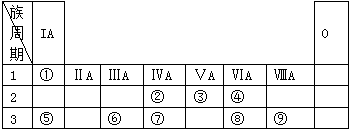
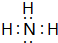 ;W与④的单质在催化剂、加热条件下发生的反应是工业制取Z的基础,写出该反应的化学方程式:4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O.
;W与④的单质在催化剂、加热条件下发生的反应是工业制取Z的基础,写出该反应的化学方程式:4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O.查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 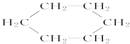 属于环状化合物 属于环状化合物 | B. |  属于卤代烃 属于卤代烃 | ||
| C. |  属于链状化合物 属于链状化合物 | D. | 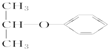 属于醚 属于醚 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | N、P、As的电负性随原子序数的增大而增大 | |
| B. | 价电子排布为4s24p3的元素位于第四周期第ⅤA族,是p区元素 | |
| C. | 2p和3p轨道形状均为哑铃形,能量也相等 | |
| D. | 镁原子由1s22s22p63s2→1s22s22p63p2时,原子释放能量,由基态转化成激发态 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 向甲、乙、丙三个密闭容器中充入一定量的A和B,发生反应:A(g)+xB(g)?2C(g).各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别如表和如图表示:下列说法正确的是( )
向甲、乙、丙三个密闭容器中充入一定量的A和B,发生反应:A(g)+xB(g)?2C(g).各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别如表和如图表示:下列说法正确的是( )| 容器 | 甲 | 乙 | 丙 |
| 容积 | 0.5L | 0.5L | 1.0L |
| 温度/℃ | T1 | T2 | T2 |
| 反应物 起始量 | 1.5molA 0.5molB | 1.5molA 0.5molB | 6.0molA 2.0molB |
| A. | 10min内甲容器中反应的平均速率v(A)=0.025mol/(L•min) | |
| B. | 由图可知:T1<T2,且该反应为吸热反应 | |
| C. | x=1,若平衡时保持温度不变,改变容器体积平衡移动 | |
| D. | T1℃,起始时甲容器中充入0.5molA、1.5molB,平衡时A的转化率为75% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸钙跟稀盐酸反应CO32-+2H+=CO2↑+H2O | |
| B. | 向碳酸钠溶液中加入过量醋酸溶液CO32-+2H+=CO2↑+H2O | |
| C. | 氯气与水反应Cl2+H2O=2H++Cl-+ClO- | |
| D. | 三氯化铝溶液与氨水Al3++3NH3•H2O=Al(OH)3↓+3NH4 + |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com