
【题目】实验室用高锰酸钾和浓盐酸制取氯气,反应方程式如下:
[___]KMnO4+[___]HCl(浓)→[___]KCl+[___]MnCl2+[___]Cl2+[___]H2O
(1)配平上述反应的化学方程式,并用单线桥标出电子转移方向和数目。__________
(2)反应中,HCl 体现的化学性质为____。
(3)若反应消耗 2molHCl,转移电子数目为_____个。
(4)将SO2气体通入KMnO4溶液中,溶液褪色,生成Mn2+.写出发生反应的离子方程式________。
【答案】2 16 2 2 5 8 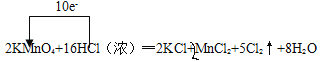 酸性和还原性 1.25NA 5SO2+2MnO4﹣+2H2O=2Mn2++5SO42﹣+4H+
酸性和还原性 1.25NA 5SO2+2MnO4﹣+2H2O=2Mn2++5SO42﹣+4H+
【解析】
(1)反应中KMnO4→MnCl2,Mn元素化合价由+7降低为+2,共降低5价,HCl(浓)→Cl2,Cl元素化合价由﹣1价升高为0价,共升高为2价,化合价升降最小公倍数为10,故KMnO4的系数为2,Cl2的系数为5,再根据原子守恒配平其它物质的系数,根据化合价变化标出电子转移的方向和数目;
(2)反应中盐酸中部分Cl化合价升高表现还原性,部分Cl化合价不变得到盐,表现酸性;
(3)根据化合价升降进行电子转移的计算;
(4)酸性高锰酸钾具有强氧化性,被还原为锰离子,二氧化硫可以被还原为硫酸根离子,据此书写。
(1)反应中Mn元素化合价由+7降低为+2,共降低5价,HCl(浓)→Cl2,Cl元素化合价由﹣1价升高为0价,共升高为2价,化合价升降最小公倍数为10,故KMnO4的系数为2,Cl2的系数为5,再根据原子守恒配平其它物质的系数,配平后的方程式为2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O,电子转移情况如下: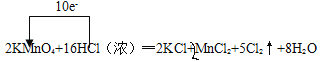 ,故答案为:2;16;2;2;5;8;
,故答案为:2;16;2;2;5;8;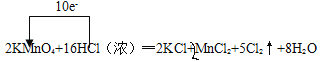 。
。
(2)反应中盐酸中部分Cl化合价升高表现还原性,部分Cl化合价不变得到盐,表现酸性;故答案为:酸性和还原性;
(3)如反应中转移了10mol电子,则消耗盐酸是16mol,若反应消耗2molHCl,转移电子数目为1.25NA,故答案为:1.25NA;
(4)酸性高锰酸钾具有强氧化性,被还原为锰离子,二氧化硫可以被氧化为硫酸根离子,反应为:5SO2+2MnO4﹣+2H2O=2Mn2++5SO42﹣+4H+,故答案为:5SO2+2MnO4﹣+2H2O=2Mn2++5SO42﹣+4H+。


科目:高中化学 来源: 题型:
【题目】A、B、C、W均为中学常见的纯净物,它们之间有如下转化关系(其它产物及反应条件已略去,反应可以在水溶液中进行)。![]()
(1)若A为有刺激性气味的气体,溶液呈碱性;C为红棕色气体,与水反应生成一元强酸D,D具有强氧化性。
①实验室制取气体A的化学方程式_____________;
②写出A→B的化学方程式为_____________;
③写出Cu与D稀溶液反应生成B的离子方程式_____________;
(2)若A、B、C 三种物质的溶液均显碱性,焰色反应均为黄色;C常作面包和糕点的发袍剂,受热分解可生成B。
①写出A溶液与C溶液反应的离子方程式为_____________;
②向两份30mL同浓度的A溶液中通入不同体积的W气体,得到溶液M、N。向M、N溶液中逐滴加入浓度为0.25mol/L盐酸,如图所示I和II分别为加入V(盐酸)与产生V(W)的关系。则A溶液的物质的量浓度为_____________,M、N 两溶液中相同溶质的物质的量之比为_____________;

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应中的能量变化是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同引起的。如图为N2(g)和O2(g)反应生成NO(g)过程中的能量变化,下列说法中正确的是

A. 1 mol N2(g)和1 mol O2(g)反应放出的能量为180 kJ
B. NO是一种酸性氧化物,能与NaOH溶液反应生成盐和水
C. 在1 L的容器中发生反应,10 min内 N2减少了1 mol,因此10 min内的平均反应速率为v(NO)=0.1 mol·![]()
![]()
D. 1 mol N2(g)和1 mol O2(g)具有的总能量小于2 mol NO(g)具有的总能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知 3A(g)+2B(g) ![]() C(s)+4D(g) △H <0。 图中a、b表示在一定条件下,A的体积分数随时间t的变化。若使曲线b变为曲线a,可采取的措施是
C(s)+4D(g) △H <0。 图中a、b表示在一定条件下,A的体积分数随时间t的变化。若使曲线b变为曲线a,可采取的措施是

A. 增大A的浓度 B. 升高温度 C. 加催化剂 D. 缩小容器体积
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知pCa=-lgc(Ca2+),Ksp(CaSO4)=9.0×10-6,Ksp(CaCO3)=2.8×10-9,向10 mL CaCl2溶液中滴加0.1mol/L的Na2SO4溶液时,溶液中pCa与Na2SO4溶液体积(V)的关系如图所示(实线),下列有关说法正确的是(已知1g3=0.48)
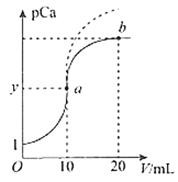
A. y值为3.48
B. a与b两点c(Ca2+)之比为50:3
C. 原CaCl2溶液浓度为1mol/L
D. 若把0.1mol/L的Na2SO4溶液换成0.1mol/L的Na2CO3溶液则图象在终点后变为虚线部分
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将a L NH3通入某恒压的密闭容器中,在一定条件下让其分解,达到平衡后气体体积增大到b L(气体体积在相同条件下测定)。下列说法中正确的是
A. 平衡后氨气的分解率为![]() ×100% B. 平衡混合气体中H2的体积分数为
×100% B. 平衡混合气体中H2的体积分数为![]() ×100%
×100%
C. 反应前后气体的密度比为a/b D. 平衡后气体的平均摩尔质量为17a/b g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关“未来金属”钛的信息有:①硬度大②熔点高③常温下耐酸碱、耐腐蚀,由钛铁矿钛的一种工业流程为:

(1)钛铁矿的主要成分是FeTiO3(钛酸亚铁),其中钛的化合价___价,反应①化学方程式为___。
(2)反应②的化学方程式为TiO2+C+Cl![]() TiCl4+CO(未配平),该反应中每消耗12gC,理论上可制备TiCl4___g。
TiCl4+CO(未配平),该反应中每消耗12gC,理论上可制备TiCl4___g。
(3)TiCl4在高温下与足量Mg反应生成金属Ti,反应③化学方程式___,该反应属于___(填基本反应类型)
(4)上述冶炼方法得到的金属钛中会混有少量金属单质是___(填名称),由前面提供的信息可知,除去它的试剂可以是以下剂中的___(填序号)
A HCl BNaOH CNaCl DH2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从海水中提取镁可按如下步骤进行:①把贝壳(主要成分是碳酸钙)煅烧成生石灰;②在引有海水的渠中加入生石灰,经过沉降,然后过滤得沉淀物;③将沉淀物与稀盐酸反应,然后结晶、过滤、干燥;④电解获得产物。根据上述提取镁的全过程,没有涉及的反应类型是( )
A.分解反应B.化合反应
C.置换反应D.复分解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25 ℃,两种酸的电离平衡常数如下表,下列叙述正确的是( )
Ka1 | Ka2 | |
H2A | 1.3×10-2 | 6.3×10-6 |
H2B | 4.2×10-7 | 5.6×10-11 |
A. H2A的电离方程式:H2A 2H++A2-
B. 常温下,在水中Na2B的水解平衡常数为:![]()
C. 相同pH的Na2A、Na2B溶液中物质的量浓度:c(Na2A)>c(Na2B)
D. 向Na2B溶液中加入少量H2A溶液,可发生反应:B2-+H2AA2-+H2B
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com