
分析 根据H原子守恒计算乙醇的物质的量,根据碳原子守恒计算CO、CO2的总的物质的量,结合二者质量之和列方程计算各自物质的量,根据m=nM计算CO2的质量.
解答 解:n(H2O)=16.2g÷18g/mol=0.9mol,
根据H原子守恒,可知乙醇的物质的量=$\frac{0.9mol×2}{6}$=0.3mol,
根据C原子守恒,可知CO和CO2的总的物质的量=0.3mol×2=0.6mol,
一氧化碳和二氧化碳的质量为:41g-16.2g=24.8g;
令CO、CO2的物质的量分别为xmol、ymol,则:
$\left\{\begin{array}{l}{x+y=0.6}\\{28x+44y=24.8}\end{array}\right.$
解得x=0.1,y=0.5,
所以CO2的质量为0.5mol×44g/mol=22g,
答:CO2的质量为22g.
点评 本题考查有机物燃烧反应的计算,关键是抓住化学反应前后原子守恒守恒解答,侧重考查学生分析计算能力.


科目:高中化学 来源: 题型:选择题
| A. | 4 mol | B. | 3 mol | C. | 2.5mol | D. | 1.2 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2c(H+)═2c(HS-)+c(S2-)+2c(OH-)? | B. | c(H+)═c(HS-)+2c(S2-)+c(OH-) | ||
| C. | c(H+)═c(HS-)+2c(S2-)? | D. | c(H+)═2c(S2-)+c(OH-)? |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
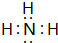 ,请用电子式表示A与C形成化合物的过程
,请用电子式表示A与C形成化合物的过程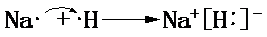 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 古剑“沈卢”“以剂钢为刃,柔铁为茎干,不尔则多断折”,剂钢指的是铁的合金 | |
| B. | 某种验钞笔中含有碘酒溶液,遇假钞呈现蓝色,其中遇碘变蓝的是葡萄糖 | |
| C. | “熬胆矾铁釜,久之亦化为铜”,该过程发生了置换反应 | |
| D. | 制造新版人民币所用的棉花、优质针叶木等原料的主要成分是纤维素 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
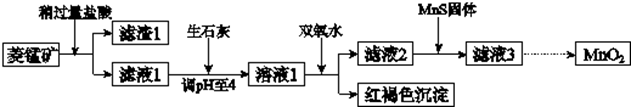
| Mn(OH)2 | Fe(OH)2 | Fe(OH)3 | Cu(OH)2 | |
| 开始沉淀时 | 8.3 | 6.3 | 2.7 | 4.7 |
| 完全沉淀时 | 9.8 | 8.3 | 3.7 | 6.7 |
| 化学式 | FeS | CuS | MnS |
| 溶度积 | 6.3×10-18 | 1.3×10-36 | 2.5×10-13 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | B | C | D |
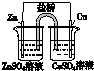 | 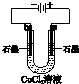 | 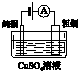 |  |
| 盐桥中的Cl-移向ZnSO4溶液 | a极附近产生的气体能使湿润的淀粉碘化钾试纸变蓝 | 粗铜的电极反应式为: Cu2++2e-═Cu | 正极反应式为: O2+4e-+2H2O═4OH- |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 化学式 | CH3COOH | HClO | H2CO3 |
| Ka | 1.8×10-5 | 3.0×10-8 | Ka1=4.1×10-7Ka2=5.6×10-11 |
| A. | 相同浓度CH3COONa和NaClO的混合液中,各离子浓度的大小关系是c(Na+)>c(ClO-)>c(CH3COO-)>c(OH-)>c(H+) | |
| B. | 向0.1mol•L-1CH3COOH溶液中滴加NaOH溶液至溶液pH=5,此时c(CH3COOH):c(CH3COO-)=9:5 | |
| C. | 少量碳酸氢钠固体加入到新制的氯水中,c(HClO)增大 | |
| D. | 等体积等物质的量浓度的CH3COONa(aq)与NaClO(aq)中离子总数大小:N前<N后 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com