
����Ŀ���л���G�Ǻϳ�ij�����Ⱦۺ���ĵ��壬��ϳɷ������£� 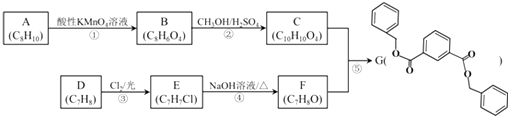
��֪��R1COOR2+R3OH ![]() RCOOR3+R2OH
RCOOR3+R2OH
��1������ϵͳ��������A������Ϊ ��
��2�����������е�ȡ����Ӧ���ڡ������������ţ����ڢݲ���Ӧ�У���ʹ�ú���18O��F����֮��C��Ӧ������������18O�ķֲ�������Ӷ��ƶϷ�Ӧ�����������о�������Ϊ ��
��3��������E�ĺ˴Ź�������ͼ�й��ж�����շ壬����ķ������Ϊ ��
��4�������кϳ�·�߿ɵõ�F��ͬ���칹��H����ɼ���H��F���Լ��� �� 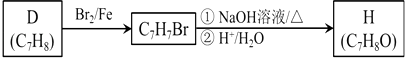
��5��C������NaOH��Һ��Ӧ�Ļ�ѧ����ʽΪ ��
��6��J��C��Ϊͬ���칹�壬������������ʣ�����Ҫ����л������֣������������칹��
������NaOH��Һ��Ӧ����1mol J��ȫ��Ӧ����4mol NaOH
���ܷ���������Ӧ����1mol J��������������Һ��Ӧ����4mol Ag
�۷����б����ϵ�һ��ȡ����ֻ��һ�֣�
���𰸡�
��1��1��3�����ױ�
��2���ܡ��ݣ�ͬλ��ʾ�ٷ�
��3��2��2��2��1
��4��FeCl3��Һ
��5��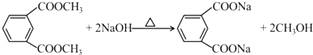
��6��6
���������⣺����G�Ľṹ��ʽ��C��F�ķ���ʽ��֪��һ���ӵ�C�������ӵ�F����������Ӧ����G�����Կ���֪FΪ ![]() ����Ӧ��ΪB��״�����������Ӧ����C������CΪ
����Ӧ��ΪB��״�����������Ӧ����C������CΪ 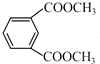 ��BΪ
��BΪ 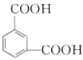 ��A����������Ӧ����B������AΪ
��A����������Ӧ����B������AΪ  ��D����������ȡ������E��E��������ˮ���F������DΪ
��D����������ȡ������E��E��������ˮ���F������DΪ ![]() ��EΪ
��EΪ ![]() ����1��AΪ
����1��AΪ  ������ϵͳ��������A������Ϊ 1��3�����ױ������Դ��ǣ�1��3�����ױ��� ��2����������ķ�����֪�����������е�ȡ����Ӧ�Тڡ��ۡ��ܡ��ݣ��ڢݲ���Ӧ�У���ʹ�ú���18O��F����֮��C��Ӧ������������18O�ķֲ�������Ӷ��ƶϷ�Ӧ�����������о�������Ϊ ͬλ��ʾ�ٷ������Դ��ǣ��ܡ��ݣ�ͬλ��ʾ�ٷ��� ��3��EΪ
������ϵͳ��������A������Ϊ 1��3�����ױ������Դ��ǣ�1��3�����ױ��� ��2����������ķ�����֪�����������е�ȡ����Ӧ�Тڡ��ۡ��ܡ��ݣ��ڢݲ���Ӧ�У���ʹ�ú���18O��F����֮��C��Ӧ������������18O�ķֲ�������Ӷ��ƶϷ�Ӧ�����������о�������Ϊ ͬλ��ʾ�ٷ������Դ��ǣ��ܡ��ݣ�ͬλ��ʾ�ٷ��� ��3��EΪ ![]() ��E�ĺ˴Ź�������ͼ�и���ķ������Ϊ2��2��2��1��
��E�ĺ˴Ź�������ͼ�и���ķ������Ϊ2��2��2��1��
���Դ��ǣ�2��2��2��1�� ��4��DΪ ![]() ��D���������������������·���������ȡ������ˮ���ữ�ɵ÷ӣ�����HΪ�ӣ���FΪ�������Լ���H��F���Լ���FeCl3��Һ��
��D���������������������·���������ȡ������ˮ���ữ�ɵ÷ӣ�����HΪ�ӣ���FΪ�������Լ���H��F���Լ���FeCl3��Һ��
���Դ��ǣ�FeCl3��Һ�� ��5��CΪ ![]() ��C������NaOH��Һ��Ӧ�Ļ�ѧ����ʽΪ
��C������NaOH��Һ��Ӧ�Ļ�ѧ����ʽΪ  ��
��
���Դ��ǣ� 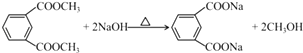 �� ��6��CΪ
�� ��6��CΪ 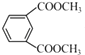 ��J��C��Ϊͬ���칹�壬����������������NaOH��Һ��Ӧ����1mol J��ȫ��Ӧ����4mol NaOH��˵��J�������������������ܷ���������Ӧ����1mol J��������������Һ��Ӧ����4mol Ag��˵������ȩ���������ij�����۷����б����ϵ�һ��ȡ����ֻ��һ�֣�˵��������ȡ���ֲ��Գƣ������������J�ĽṹΪ����������������OOCH��������CH3 �� �ֲ��Գƣ�����6�ֽṹ��
��J��C��Ϊͬ���칹�壬����������������NaOH��Һ��Ӧ����1mol J��ȫ��Ӧ����4mol NaOH��˵��J�������������������ܷ���������Ӧ����1mol J��������������Һ��Ӧ����4mol Ag��˵������ȩ���������ij�����۷����б����ϵ�һ��ȡ����ֻ��һ�֣�˵��������ȡ���ֲ��Գƣ������������J�ĽṹΪ����������������OOCH��������CH3 �� �ֲ��Գƣ�����6�ֽṹ��
���Դ��ǣ�6��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й����У���Ҫ�����������ǣ� ��
A.I2��I+I
B.H+Cl=HCl
C.H+H=H2
D.S+O2=SO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ֹ�����ĸ�ʴ�����缶���⣬ÿ��ȫ����ֲ������ķ�֮һ��ʴ����ʧ
��1��������ʴ��Ҫ��������ʴ���ø�ʴ�����еĵ缫��ӦʽΪ����
��2��Ϊ����ijˮ�����բ�ŵı���ʴ���ʣ����Բ���ͼ���������к�������բ���ϵĹ������R���Բ���________��
A.ͭ
B.��
C.п
D.ʯī
��3��ͼ����ʾ����Ҳ�ɽ�����բ�ŵı���ʴ���ʣ�������բ��Ӧ��������ֱ����Դ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������Ϣ��ҵ����Ҫ�Ļ������ϡ�ͨ���ý�̿�ڸ����»�ԭ���������Ƶôֹ�(������������������)���ֹ���������Ӧ�������Ȼ���(��Ӧ�¶�450��500��)�����Ȼ��辭�ᴿ����������ԭ�ɵøߴ��衣������ʵ�����Ʊ����Ȼ����װ��ʾ��ͼ��
�����Ϣ���£�
a�����Ȼ�����ˮ����ˮ�⣻
b���������������ڸ����¾���������ֱ�ӷ�Ӧ������Ӧ���Ȼ��
c���й����ʵ������������±���
�� �� | SiCl4 | BCl3 | AlCl3 | FeCl3 | PCl5 |
�е�/�� | 57.7 | 12.8 | �� | 315 | �� |
�۵�/�� | ��70.0 | ��107.2 | �� | �� | �� |
�����¶�/�� | �� | �� | 180 | 300 | 162 |
��ش��������⣺
��1��д��װ��A�з�����Ӧ�����ӷ���ʽ��
��2��װ��A��g�ܵ���������װ��C�е��Լ�����װ��E�е�hƿ��Ҫ��ȴ����������
��3��װ��E��hƿ�ռ����Ĵֲ����ͨ������(���ƶ������)�õ��ߴ������Ȼ��裬�����IJ������У�����Ԫ������ܻ����е�����Ԫ����(��дԪ�ط���)��
��4��Ϊ�˷�������������Ԫ�صĺ������Ƚ�������Ԥ������ʹ��Ԫ�ػ�ԭ��
Fe2�� �� ����KMnO4����Һ�����������½���������ԭ�ζ�����Ӧ�����ӷ���ʽ�ǣ�5Fe2����MnO4����8H��=5Fe3����Mn2����4H2O
���ζ�ǰ�Ƿ�Ҫ�μ�ָʾ����(��ǡ���)����˵��������
��ijͬѧ��ȡ5.000g�������Ԥ������������ƿ�����Ƴ�100mL��Һ����ȡ25.00mL������Һ����1.000��10��2mol��L��1KMnO4����Һ�ζ����ﵽ�ζ��յ�ʱ�����ı���Һ20.00mL�������������Ԫ�ص�������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������β����Ⱦ���ѱ������˹�ע��������ȼ���У������������������һ��������Ͻ������ף��������õ��ȼ��ȼ��ʹ�������¶�Ѹ�����ߣ���������������ͣ��ɴ˲�����ѹ���ƶ������˶���ȼ��ʱ�������к�����ͨ��β���ų�����ɴ�����Ⱦ��Ϊ�����ۣ�������(C8H18)�������͵ijɷ֣����������O2ռ1/5�������ش��������⣺
��1����������������������(��ͬ������)Ϊa��Ҫʹ������ȫȼ�գ�a����СֵΪ(��С����ʾ�������СֵΪa��)��
��2���������������������ȴ���a����β��������Ⱦ�������к���������Ժ������������(д����ʽ)��
��3����������������������С��a�䣬��β��������Ⱦ�������к���������Ժ������������(д����ʽ) �� ������������ķ�Ӧ����ʽ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����[Cu(NH3)4]2��������NH3����������Cu2����ϵĻ�ѧ����(����)
A.���Ӽ�B.�Ǽ��Լ�C.���Լ�D.��λ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й������������������ⲻ��ȷ���ǣ� ��
A.�����ܵ����γɣ�������һ�����ܵ����γ�
B.���������Ƽ�����ת������һ�������Ƽ�����ת
C.HCl �����е���������һ��ԭ�ӵ�s�������һ��ԭ�ӵ�p�������ͷ��ͷ����ʽ�ص��������ɵ�
D.���嵥����һ���������������ܴ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£�50mL pH=1��ϡH2SO4������Ļ��Һ��50mL Ba��OH��2��Һ���ϣ���ַ�Ӧ����ˣ���0.466g��������Һ��pHֵ��Ϊ13����
��1��ԭ���Һ��SO42�� ��Cl�������ʵ�����
��2��Ba��OH��2��Һ�����ʵ���Ũ�ȣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и��������У��ɰ��ܽ⡢���ˡ������IJ���˳��������
A������ͭ��̿�� B������غ��Ȼ���
C��ˮ�;ƾ� D��̼���ƺ����ᱵ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com