
在实验室中,通常将金属钠保存在( )
|
| A. | 水中 | B. | 煤油中 | C. | 四氯化碳中 | D. | 汽油中 |
考点:
钠的化学性质.
专题:
几种重要的金属及其化合物.
分析:
根据钠的保存需要考虑钠的性质,如钠与空气和水发生反应,与四氯化碳、汽油、煤油不反应,钠的密度比四氯化碳小、比煤油、汽油的密度大以及汽油的沸点低于煤油,易挥发.
解答:
解:A、金属钠和水之间能反应,所以不能保存在水中,故A错误;
B、金属钠与煤油不反应,且密度比煤油大,沉于煤油底部,隔开了空气,所以钠能保存在煤油中,故B正确;
C、金属钠与四氯化碳不反应,但密度比四氯化碳小,浮于煤油,能接触到空气,所以钠不能保存四氯化碳中,故C错误;
D、金属钠与汽油中不反应,密度比汽油大,沉于煤油液面,但汽油的沸点低于煤油,易挥发,所以钠不能保存汽油中,故D错误;
故选:B.
点评:
金属的保存需要考虑金属的物理性质和化学性质.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
下列说法不正确的是()
A. 0.1mol/L硫酸铵溶液中各离子的浓度由大到小的顺序是:c (NH4+)>c(SO42﹣)>c(H+)>c(OH﹣)
B. 在苏打与小苏打的混合溶液中存在:c(Na+)+c(H+)=c(OH ﹣)+2c(CO32﹣)+c(HCO3﹣)
C. 在滴有酚酞的Na2CO3溶液中,加入BaCl2溶液后红色褪去,证明Na2CO3溶液中存在水解平衡
D. 常温常压下能自发进行的反应,一定都是放热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
有三种不同质量比的氧化铜与炭粉的混合物样品①、②、③.甲、乙、丙三同学各取一种样品,加强热充分反应,测定各样品中氧化铜的量.
(1)甲取样品①强热,若所得固体为金属铜,将其置于足量的稀硝酸中微热,产生1.12L气体(标准状况),则样品①中氧化铜的质量为 g.
(2)乙取样品②ag强热,生成的气体不能使澄清的石灰水变浑浊.再将反应后的固体与足量的稀硝酸微热,充分反应后,有bg固体剩余,该剩余固体的化学式为C.样品②中氧化铜质量为 g
(以含a、b的代数式表示).
(3)丙称量样品③强热后剩余的固体,质量比原样品减小了cg,若该固体为金属铜,则样品③中氧化铜物质的量(n)的取值范围为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
我国科学家在世界上第一次为一种名为“钴酞菁”的分子(直径为1.3nm)恢复了磁性.“钴酞菁”分子的结构和性质与人体内的血红素及植物体内的叶绿素非常相似.下列说法中不正确的是( )
|
| A. | “钴酞菁”分子分散在水中所形成的分散系不具有丁达尔效应 |
|
| B. | “钴酞菁”分子能透过滤纸 |
|
| C. | 此项工作可以用来改变分子的某些物理性质 |
|
| D. | 此项工作可广泛应用于光电器件、生物技术等方面 |
查看答案和解析>>
科目:高中化学 来源: 题型:
同温同压下,同体积的氨气和硫化氢气体(H2S)的质量比为 ;同质量的氨和硫化氢气体的体积比为 ,其中含有的氢的原子个数比为 ;若二者氢原子数相等,它们的体积比为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
Na2O2与水反应能够产生O2,这一反应在呼吸面具、潜水艇及太空飞船中可为人体提供呼吸所用的O2.下面对该反应的说法中正确的是( )
|
| A. | 这是一个氧化还原反应,Na2O2既是氧化剂,又是还原剂 |
|
| B. | 这是一个氧化还原反应,Na2O2是氧化剂,水是还原剂 |
|
| C. | 这是一个氧化还原反应,Na2O2是还原剂,水是氧化剂 |
|
| D. | 这是一个置换反应,有单质O2产生 |
查看答案和解析>>
科目:高中化学 来源: 题型:
将氯化钠、氯化铝、氯化亚铁、氯化铁、氯化镁五种溶液,通过一步实验就能加以区别,并只用一种试剂,这种试剂是( )
|
| A. | KSCN | B. | BaCl2 | C. | NaOH | D. | HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:
研究物质性质的基本程序之一就是“预测物质的性质”.下列对物质性质的预测不正确的是()
A. 乙烯双键中的一个键容易断裂,所以容易发生加成反应和取代反应
B. CH3CH3为乙烷,该物质可以看作是甲烷分子中的一个氢原子被﹣CH3取代的结果,该物质能与氯气发生取代反应
C. 某有机化合物可以表示为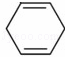 ,该物质能够使溴的四氯化碳溶液褪色
,该物质能够使溴的四氯化碳溶液褪色
D. 乙炔与苯具有相同的最简式,故等质量的苯和乙炔完全燃烧,消耗O2的质量相同
查看答案和解析>>
科目:高中化学 来源: 题型:
高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压.高铁电池的总反应为:3Zn+2K2O4+8H2O 3Zn(OH)2+2Fe(OH)3+2Fe(OH)3+4KOH下列叙述不正确的是()
3Zn(OH)2+2Fe(OH)3+2Fe(OH)3+4KOH下列叙述不正确的是()
A. 放电时负极反应为:3Zn﹣6e﹣+6OH﹣═3Zn(OH)2
B. 放电时正极反应为:2FeO42﹣+6e﹣+8H2O═2Fe(OH)3+10OH﹣
C. 放电时每转移3mol电子,正极有1mol K2FeO4被氧化
D. 放电时正极附近溶液的碱性增强
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com