
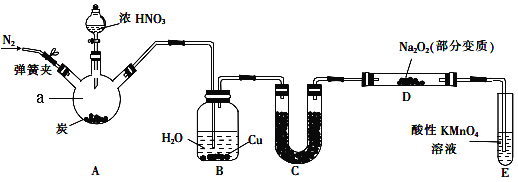
【题目】亚硝酸钠(NaNO2)是一种常见的食品添加剂。某兴趣小组用如图所示装罝制备NaNO2并对其性质作如下探究(A中加热装罝已略去)。
查阅资料可知:
① 2NO+Na2O2![]() 2NaNO2;2NO2+Na2O2
2NaNO2;2NO2+Na2O2![]() 2NaNO3。
2NaNO3。
② NO能被酸性KMnO4氧化成NO3。
(1)装置中仪器a的名称为____________,A中反应的化学方程式是______________________。
(2)装置B中观察到的主要现象是____________________________________________________。
(3)装置C中盛放的试剂是__________________________。
(4)装置E的作用是_______________。
(5)A中滴入浓硝酸之前,应先通入N2一段时间,原因是__________________________________。
(6)写出NO被酸性KMnO4氧化的离子反应方程式_______________________________________。
【答案】 三颈烧瓶(或三颈瓶) C+4HNO3![]() CO2↑+4NO2↑+2H2O 溶液变蓝,铜片溶解,有无色气体冒出 碱石灰(或生石灰或氢氧化钠固体) 吸收有毒气体NO,防止空气污染 排尽装置中的空气,防止对后续实验有干扰 5NO+3MnO4-+4 H+===5NO3+3Mn2+ + 2H2O
CO2↑+4NO2↑+2H2O 溶液变蓝,铜片溶解,有无色气体冒出 碱石灰(或生石灰或氢氧化钠固体) 吸收有毒气体NO,防止空气污染 排尽装置中的空气,防止对后续实验有干扰 5NO+3MnO4-+4 H+===5NO3+3Mn2+ + 2H2O
【解析】(1). 仪器a的名称为三颈烧瓶(或三颈瓶),碳与浓硝酸在加热条件下反应生成CO2、NO2和H2O,化学方程式为:C+4HNO3![]() CO2↑+4NO2↑+2H2O,故答案为:三颈烧瓶(或三颈瓶);C+4HNO3
CO2↑+4NO2↑+2H2O,故答案为:三颈烧瓶(或三颈瓶);C+4HNO3![]() CO2↑+4NO2↑+2H2O;
CO2↑+4NO2↑+2H2O;
(2). B装置中的水和混合气体中的NO2反应生成HNO3和NO,Cu与稀硝酸反应生成Cu(NO3)2、NO和水,所以装置B中观察到的主要现象是:溶液变蓝,铜片溶解,有无色气体冒出,故答案为:溶液变蓝,铜片溶解,有无色气体冒出;
(3). B中得到的NO气体中含有二氧化碳和水蒸气,二氧化碳或水蒸气都能与D装置中的过氧化钠反应,所以为保证制得的亚硝酸钠的纯度,应该除去二氧化碳和水蒸气,所以C中盛放的试剂可以是碱石灰(或生石灰或氢氧化钠固体),故答案为:碱石灰(或生石灰或氢氧化钠固体);
(4). 装置E中盛放的是酸性高锰酸钾溶液,由题中信息可知,酸性高锰酸钾溶液可以吸收多余的有毒气体NO,防止污染空气,故答案为:吸收有毒气体NO,防止空气污染;
(5). 因NO可以和空气中的氧气反应生成二氧化氮,所以A中滴入浓硝酸之前,应先通入N2一段时间,以排尽装置中的空气,防止对后续实验产生干扰,故答案为:排尽装置中的空气,防止对后续实验有干扰;
(6). 由题中信息可知,NO能被酸性KMnO4氧化成NO3,MnO4体现氧化性生成Mn2+,根据得失电子守恒和原子守恒,该反应的离子方程式为:5NO+3MnO4-+4 H+=5NO3+3Mn2+ + 2H2O,故答案为:5NO+3MnO4-+4 H+=5NO3+3Mn2+ + 2H2O。


 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案科目:高中化学 来源: 题型:
【题目】在下列溶液中,能大量共存的一组离子是( )
A.pH=1的溶液中:NH4+、Fe2+、SO ![]() 、Cl﹣
、Cl﹣
B.通入过量SO2气体的溶液中:Fe3+、NO3﹣、Ba2+、H+
C.c(Al3+)=0.1 mol/L的溶液中:Na+、K+、AlO ![]() 、SO
、SO ![]()
D.由水电离出的c(H+)=1×10﹣13 mol/L的溶液中:Na+、HCO ![]() 、Cl﹣、Br﹣
、Cl﹣、Br﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学与技术]水处理技术在生产、生活中应用广泛.
(1)含有较多离子的水称为硬水.硬水加热后产生碳酸盐沉淀的离子方程式为(写出一个即可)
(2)将RH型阳离子交换树脂和ROH型阴离子交换树脂串接来软化天然硬水,应首先使硬水通过(填“RH”或“ROH”)型离子交换树脂,原因是 .
(3)通过施加一定压力使水分子通过半透膜而将大分子或离子截留,从而获得纯净水的方法称为 . 电渗析法净化水时,使离子通过半透膜的推动力是 .
(4)检验蒸馏水的纯度时,最简单易行的方法是测定水的 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某密闭容器中,有A.B两种气体,反应按下式进行A(g)+B(g)═2C(g)反应经过2S后浓度不再发生变化时,测得容器中各物质的浓度分别为c(A)=0.5mol/L,c(B)=0.75mol/L,c(C)=0.5mol/L.
(1)B物质的起始浓度为
(2)2S时A的转化率
(3)用物质A表示反应的平均速率 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将4mol SO2与2molO2放入4L的密闭容器中,在一定条件下反应达到平衡:2SO2+O22SO3测得平衡时混合物总的物质的量为5mol,求:
(1)平衡时各物质的浓度;
(2)平衡时SO2的转化率.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】除去下列物质中的杂质(括号中为杂质),采用的试剂和除杂方法错误的是( )
选项 | 含杂质的物质 | 试剂 | 除杂方法 |
A | C2H4(SO2) | NaOH溶液 | 洗气 |
B | C6H6(苯酚) | 浓Br2水 | 过滤 |
C | C6H5NO2(HNO3) | NaOH溶液 | 分液 |
D | C2H2(H2S) | CuSO4溶液 | 洗气 |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】a、b、c、d为短周期元素,a的原子中只有1个电子,b2-和c+离子的电子层结构相同,d与b同族。下列叙述错误的是
A. a与其他三种元素形成的元化合物中其化合价均为+1
B. b与其他三种元素均可形成至少两种二元化合物
C. d和a形成的化合物的溶液呈弱酸性
D. C的原子半径是这些元素中最大的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列电化学有关说法中正确的是( )
A.将钢闸门与直流电源的正极相连,可降低钢闸门腐蚀速率
B.镀锌铁制品镀层受损后,铁制品仍不易生锈
C.粗铜精炼时,电镀液中的c(Cu2+)保持不变
D.纯银在空气中久置变黑发生的是电化学腐蚀
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com