
 请按要求回答下列问题.
请按要求回答下列问题.分析 (1)①若打开K2,合并K1,形成原电池反应,Zn为负极,被氧化,Cu为正极,发生还原反应生成铜;
②若打开K1,合并K2,为电镀池,Cu为阳极,被氧化,Zn为阴极,发生还原反应生成铜;
(2)铝片和铜片插入浓HNO3溶液中,金属铝会钝化,金属铜和浓硝酸之间会发生自发的氧化还原反应;插入稀NaOH溶液中,金属铜和它不反应,金属铝能和氢氧化钠发生自发的氧化还原反应,在原电池中,自发氧化还原反应中的失电子的金属为负极,另一种金属或非金属是正极.
解答 解:(1)①若打开K2,合并K1,形成原电池反应,Zn为负极,被氧化而锌不断溶解,Cu为正极,发生还原反应生成铜,电极方程式为Cu2++2e-═Cu,
故答案为:锌不断溶解;Cu2++2e-═Cu;
②若打开K1,合并K2,为电镀池,Cu为阳极,被氧化,发生Cu-2e-═Cu2+,Zn为阴极,发生还原反应,锌极镀上一层红色的铜,
故答案为:电极表面有红色固体附着;Cu-2e-═Cu2+;
(2)铝片和铜片插入浓HNO3溶液中,金属铝会钝化,金属铜和浓硝酸之间会发生自发的氧化还原反应,此时金属铜时负极,金属铝是正极,
插入稀NaOH溶液中,金属铜和它不反应,金属铝能和氢氧化钠发生自发的氧化还原反应,此时金属铝是负极,金属铜是正极,
故答案为:铜片;铝片.
点评 本题综合考查原电池和电解池知识,为高频考点,注意把握原电池、电解池的工作原理以及电极方程式的书写,在判断原电池正负极时注意电解质溶液的性质,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 18 g D2O所含的电子数为10NA | |
| B. | 12 g金刚石中含C-C键数为4NA | |
| C. | 标况下11.2 L二氯甲烷所含分子数为0.5NA | |
| D. | 现有乙烯、丙烯的混合气体共14 g,其原子数为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铝片与稀H2SO4反应 | B. | 灼热的炭与CO2反应 | ||
| C. | 高温煅烧石灰石 | D. | 甲烷在O2中的燃烧反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  $\stackrel{催化剂}{→}$ $\stackrel{催化剂}{→}$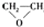 +HOCH2═O═CH2OH+2H2O +HOCH2═O═CH2OH+2H2O | B. | CH2═CH2+Cl2+Ca(OH)2? +CaCl2+H2O +CaCl2+H2O | ||
| C. | CH2═CH2+ (过氧乙酸)? (过氧乙酸)?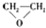 +C3HCOCH +C3HCOCH | D. | 2CH2═CH2+O2$\stackrel{催化剂}{→}$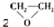 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 油脂、淀粉、蔗糖和蛋白质在一定条件能发生水解反应 | |
| B. | 甲烷和苯都不能与溴水、酸性高锰酸钾溶液发生反应,但苯不属于饱和烃 | |
| C. | 甲烷与氯气制备一氯甲烷符合绿色原子经济要求 | |
| D. | 乙烯聚合为聚乙烯高分子材料符合绿色原子经济要求 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
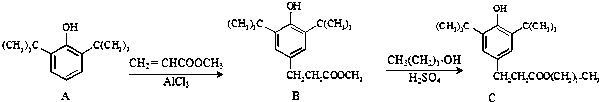
| A. | 物质A中所有碳原子有可能位于同一平面 | |
| B. | 物质B可与4molH2发生加成反应 | |
| C. | 用酸性KMnO4溶液鉴别抗氧化剂C中是否含有CH3(CH2)17OH | |
| D. | B生成C的反应类型为取代反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
| 元素 | 有关信息 |
| X | 元素主要化合价-2,原子半径为0.0074nm |
| Y | 所在主族序数与所在周期序数之差为4 |
| Z | 单质在X的单质中燃烧,产物是造成酸雨的罪魁祸首之一 |
| D | 最高价氧化物对应的水化物能电离出电子数相等的阴、阳离子 |
| E | 单质是生活中的常见金属,其制品在潮湿空气中易被腐蚀或损坏 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
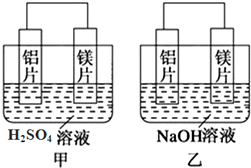
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com