
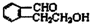 ;
;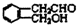 .
. ;此A对应的B生成C的反应:
;此A对应的B生成C的反应: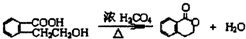 .
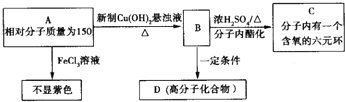
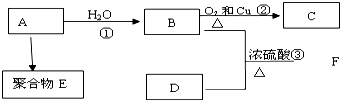
. 分析 A为芳香烃衍生物,只含C、H、O三种元素,能与新制氢氧化铜悬浊液反应生成B,则A含有-CHO,B能发生分子内酯化反应生成C,则B含有-COOH、-OH,故A中还含有-OH,A不能与氯化铁溶液发生显色反应,故A含有的羟基为醇羟基,A在Cu作催化剂条件下与氧气发生氧化反应生成E,且E具有相同的官能团,可以确定A含有1个-CHO、1个-OH,且-OH相连的C原子上有2个H原子,A的相对分子质量为150,去掉1个-CHO、1个-OH后剩余基团式量为150-46=104,剩余基团中C原子最大数目为$\frac{104}{12}$=8…8,应为C8H8,故A含有1故苯环,结合C中含有1个含有O原子的六元环,则A的结构为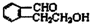 或
或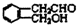 ,B的结构为
,B的结构为 或
或 ,(4)中A在浓硫酸条件下生成F,F能使溴水褪色,则A为
,(4)中A在浓硫酸条件下生成F,F能使溴水褪色,则A为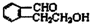 ,F为
,F为 ,E为
,E为 ,B的结构为
,B的结构为 ,C为
,C为 ,B发生缩聚反应得到D,据此解答.
,B发生缩聚反应得到D,据此解答.
解答 解:A为芳香烃衍生物,只含C、H、O三种元素,能与新制氢氧化铜悬浊液反应生成B,则A含有-CHO,B能发生分子内酯化反应生成C,则B含有-COOH、-OH,故A中还含有-OH,A不能与氯化铁溶液发生显色反应,故A含有的羟基为醇羟基,A在Cu作催化剂条件下与氧气发生氧化反应生成E,且E具有相同的官能团,可以确定A含有1个-CHO、1个-OH,且-OH相连的C原子上有2个H原子,A的相对分子质量为150,去掉1个-CHO、1个-OH后剩余基团式量为150-46=104,剩余基团中C原子最大数目为$\frac{104}{12}$=8…8,应为C8H8,故A含有1故苯环,结合C中含有1个含有O原子的六元环,则A的结构为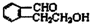 或
或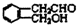 ,B的结构为
,B的结构为 或
或 ,(4)中A在浓硫酸条件下生成F,F能使溴水褪色,则A为
,(4)中A在浓硫酸条件下生成F,F能使溴水褪色,则A为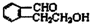 ,F为
,F为 ,E为
,E为 ,B的结构为
,B的结构为 ,C为
,C为 ,B发生缩聚反应得到D,
,B发生缩聚反应得到D,
(1)B为 或
或 ,分子中含氧官能团为:羧基、羟基,
,分子中含氧官能团为:羧基、羟基,
故答案为:羧基、羟基;
(2)由上述分析可知,符合上述条件的A的两种可能的结构为: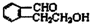 、
、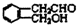 ,
,
故答案为: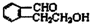 ;
;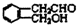 ;
;
(3)B为 或
或 ,1molB分别与Na,NaOH,NaHC03反应时,消耗2molNa、1molNaOH、1molNaHC03,消耗三者物质的量之比为:2:1:1,
,1molB分别与Na,NaOH,NaHC03反应时,消耗2molNa、1molNaOH、1molNaHC03,消耗三者物质的量之比为:2:1:1,
故答案为:2:1:1;
(4)A在浓硫酸条件下生成F,F能使溴水褪色,则A为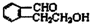 ,F为
,F为 ,E为
,E为 ,B的结构为
,B的结构为 ,C为
,C为 ,B发生缩聚反应得到D,
,B发生缩聚反应得到D,
①A→F的反应类型为消去反应,
故答案为:消去反应;
②此A与新制Cu(OH)2悬浊液的反应的方程式为: ,
,
此A对应的B生成C的反应方程式为: ,
,
故答案为: ;
; .
.
点评 本题考查有机物推断,题目难度较大,注意利用残余法计算确定A的结构是解题关键,再结合转化关系推断,需要学生熟练掌握官能团性质,对学生的逻辑推理有一定的要求.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
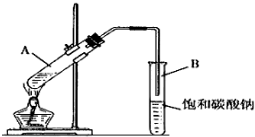 (1)写出制取乙酸乙酯的化学反应方程式CH3COOH+CH3CH2OH
(1)写出制取乙酸乙酯的化学反应方程式CH3COOH+CH3CH2OH CH3COOC2H5+H2O;
CH3COOC2H5+H2O;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
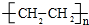 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
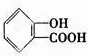 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原电池中电子流出的极为负极,发生氧化反应 | |
| B. | 原电池中阴离子向正极移动 | |
| C. | 原电池是将电能转化为化学能的装置 | |
| D. | 原电池正极上发生氧化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
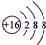
 ,属于离子化合物.
,属于离子化合物.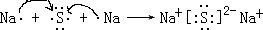 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
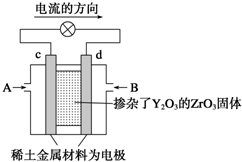 科学家制造出一种使用固体电解质的燃料电池,其效率更高,可用于航天航空.如下图所示装置中,以稀土金属材料作惰性电极,在两极上分别通入丙烷和空气,其中固体电解质是掺杂了Y2O3的ZrO3固体,它在高温下能传导正极生成的O2-.
科学家制造出一种使用固体电解质的燃料电池,其效率更高,可用于航天航空.如下图所示装置中,以稀土金属材料作惰性电极,在两极上分别通入丙烷和空气,其中固体电解质是掺杂了Y2O3的ZrO3固体,它在高温下能传导正极生成的O2-.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
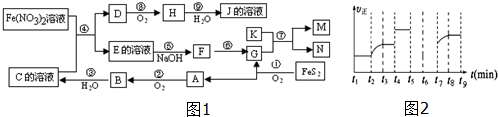
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com