
下列叙述正确的是
A.糖类、蛋白质都属于天然高分子化合物
B.强紫外线灼伤人体皮肤属于皮肤蛋白质的变性
C.纤维素和淀粉的组成都可用(C6H10O5)n表示,它们互为同分异构体
D.向鸡蛋清溶液中分别加入饱和(NH4)2SO4和CuSO4溶液都能使之聚沉,其原理相同
科目:高中化学 来源:2014-2015江苏省高二上学期期中化学(必修)试卷(解析版) 题型:选择题
对于某些离子的检验及结论一定正确的是
A.加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有CO32?
B.加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42?
C.加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,一定有NH4+
D.加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+
查看答案和解析>>
科目:高中化学 来源:2013-2014广东省越秀区高一下学期学业水平测试调研化学试卷(解析版) 题型:选择题
下列物质中不能使酸性KMnO4溶液褪色的是( )
①乙烯 ②苯 ③乙醇 ④甲烷 ⑤乙酸 ⑥二氧化硫
A.①②③④⑤ B.②④⑤ C.②④⑤⑥ D.①③⑥
查看答案和解析>>
科目:高中化学 来源:2013-2014广东省肇庆市第二学期高二期末统测化学试卷(解析版) 题型:填空题
电解原理在化学工业中有广泛应用。下图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。 请回答以下问题:
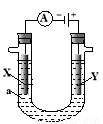
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则
①在X极附近观察到的现象是 。
②Y电极上的电极反应式是 ;把湿润的碘
化钾淀粉试纸放在Y电极附近,现象是 。
(2)要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则:X电极的材料是 ,
Y电极上发生的电极反应式为 。(说明:杂质发生的电极反应不必写出)
查看答案和解析>>
科目:高中化学 来源:2013-2014广东省肇庆市第二学期高二期末统测化学试卷(解析版) 题型:选择题
某有机物A用质谱仪测定如图①,核磁共振氢谱示意图如图②,则A的结构简式可能为

A.HCOOH B.CH3CHO C.CH3CH2OH D.CH3CH2CH2COOH
查看答案和解析>>
科目:高中化学 来源:2013-2014广东省珠海市高三学业质量监测二模理综化学试卷(解析版) 题型:填空题
(16分)
I.制取三氧化硫反应的化学方程式为:2SO2(g)十O2(g) 2SO3(g)
2SO3(g)
(1)此反应是工业上生产 的重要步骤。
(2)能够说明在恒温恒容条件下,上述反应已经达到化学平衡状态的是 (填序号).
a.每生成1mol SO3的同时生成0.5mol O2
b.容器中混合气体的密度不变
c.SO2、O2、SO3的物质的量之比为2:1:2
d.容器中气体总压强不变
(3)在400℃时,常压下,容积为1.0L的密闭容器中充入1.00mol SO2(g)和0.96mol O2(g),充分反应后,测得还有0.04mol SO2剩余,并放出190.08KJ的热量。
① 根据有关数据,请分析在工业生产中选择常压反应器的原因:
。
②写出此反应的热化学方程式:
2SO2(g)十O2(g) 2SO3(g) △H= 。
2SO3(g) △H= 。
Ⅱ.(1)在某温度下,把1.00 mol NH3溶于水中配成1.00 L溶液,测得溶液中OH-浓度和时间的图像如下:

① 求该温度时,氨水的电离平衡常数K= 。
② 在t1时刻再加入H2O配成2L溶液,于t2时刻重新达到平衡,请在坐标系中画出t1 ~t2时间内OH-浓度随时间变化的曲线。
(2)将a mol/L的盐酸和b mol/L氨水等体积混合,混合后体积为混合前体积之和,充分反应后所得溶液显中性。
① a b (填“<”、“=”或“>”)
② 根据物料守恒原理,求混合后溶液中剩余氨水浓度:c(NH3·H2O)= 。
(用含有a、b的式子表示)
查看答案和解析>>
科目:高中化学 来源:2013-2014广东省珠海市高三学业质量监测二模理综化学试卷(解析版) 题型:选择题
下列有关物质的性质或应用正确的是
A.单质硅用于制造芯片和光导纤维
B.浓硫酸能干燥SO2、NO2等气体,说明浓硫酸具有吸水性
C.SO2具有漂白性,通入紫色石蕊溶液中能使溶液先变红后褪色
D.30%的H2O2溶液中加入MnO2可制得O2,MnO2做氧化剂
查看答案和解析>>
科目:高中化学 来源:2013-2014广东省高一下学期期末考试化学试卷(解析版) 题型:填空题
利用“化学蒸气转移法”制备TaS2晶体,某温度下的2L恒容密闭容器中加入一定量 的 I2(g)和TaS2(s)发生如下反应
TaS2(s)+2I2(g) TaI4(g)+S2(g)△H=a kJ·mol-1 (I)
TaI4(g)+S2(g)△H=a kJ·mol-1 (I)
达平衡时,TaS2(s)、I2(g)、TaI4(g)、、S2(g)的物质的量分别为3 mol 、2mol、2mol、2mol。
(1)反应(I)的平衡常数表达式K=
(2)若该温度下该容器中某时刻TaS2(s)、I2(g)、TaI4(g)、、S2(g)的物质的量分别为2mol、2mol、4mol、4mol,则该时刻平衡向 (填“正反应”或“逆反应”)移动,v正 v逆(填“>”、“=”或“<”)。
(3)在不同温度下,该反应的平衡常数K如下表:
温度/℃ | 40 | 80 | 200 |
平衡常数K | 1 | 1.5 | 4 |
该反应的△H 0(填“>”、“=”或“<”)。
(4)40℃时,向该恒容密闭容器中加入2mol I2(g)和4mol TaS2(s),I2(g)的平衡转化率为 (写出计算过程,结果保留小数点后1位)
查看答案和解析>>
科目:高中化学 来源:2013-2014广东省第一学期期终考试高一级化学科试卷甲卷(解析版) 题型:选择题
某学生配制0.5mol/L的氯化钠溶液,实际浓度偏低,原因可能是
A.天平空摆时,指针偏向标尺右边 B.溶解后烧杯未经洗涤
C.容量瓶中原有少量蒸馏水 D.定容时腑视刻度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com