
【题目】甲、乙为两种不同介质的乙醇燃料电池(如下图所示)。下列说法正确的是
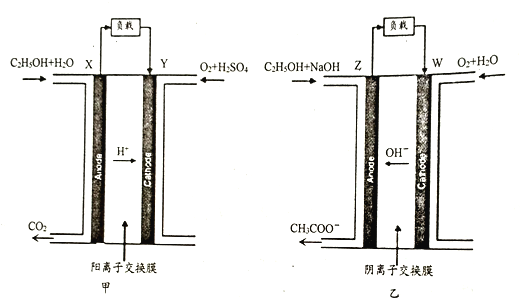
A. 装置甲和乙均是电能转化为化学能
B. X、Z极上分别消耗等物质的量乙醇时,流过甲、乙负载的电子数相同
C. Y、W极消耗氧气物质的量相同时,X、Z极消耗乙醇的物质的量也相同
D. Z极上发生的电极反应为:CH3CH2OH+5OH--4e-=CH3COO-+4H2O
 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案科目:高中化学 来源: 题型:
【题目】能够鉴定氯乙烷中氯元素的存在的操作是( )
A. 在氯乙烷中直接加入AgNO3溶液
B. 加入NaOH溶液,加热后加入稀硝酸酸化,然后加入AgNO3溶液
C. 加蒸馏水,充分搅拌后,加入AgNO3溶液
D. 加入NaOH的乙醇溶液,加热后加入AgNO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丰富多彩的颜色变化增添了化学的魅力。下列颜色变化过程中气体被氧化的是( )
A.水蒸气使淡黄色过氧化钠变白色
B.CuSO4蓝色溶液吸收H2S后有黑色沉淀
C.SO2能使溴水褪色
D.C12使湿润的淀粉碘化钾试纸变蓝
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列数据记录合理的是
A. 用托盘天平称取5.85 g食盐
B. 用10 mL量筒量取8.36 mL稀硫酸
C. 用广泛pH试纸测得某溶液pH值为5.5
D. 用酸式滴定管移取高锰酸钾溶液19.10 mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】漂白粉来源广泛、价格低康用其脱除烟气中SO2和NOx是目前研究的热点之一:
(1)脱除姻气中的SO2和NOx实验示意装置如图所示:图中N2和O2的作用______;装置A的作用是________。
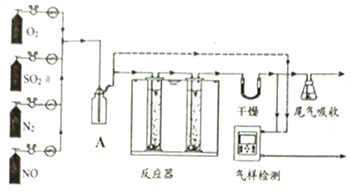
(2)工业上用氯气与熟石灰制取漂白粉的化学方程式为________。
(3)用漂白粉溶液同时脱硫脱硝时,测得相同条件下SO2和NO的脱除率随时间变化如图所示:
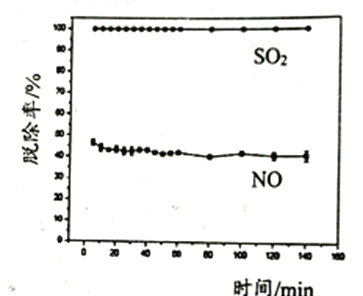
①SO2的脱除率总是比NO的大,除因为脱除NO的活化能较高外,另一原因是__________。
②漂白粉溶液与过量SO2反应(同时有沉淀生成)的离子方程式为___。
(4)脱硝过程中包含一系列反应:2NO+O2=2NO2,2NO2+H2O![]() HNO2+HNO3,NO+HClO
HNO2+HNO3,NO+HClO![]() NO2+HCl等。
NO2+HCl等。
①实验测得吸收液初始pH与NO脱除率的关系如图所示:
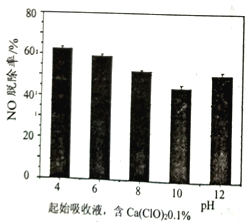
i)在4<pH<10时,pH越小,NO脱除率越大,是因为________;
ii)当pH=12时,NO脱除率又增大,是因为________。
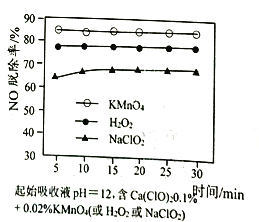
②为提高NO脱除率,在其他条件相同时,漂白粉溶液中分别添加三种不同添加剂,测得其对NO脱除率的影响如图所示。NO脱除率不同的原因是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用蛋白质的变性可以为我们日常生活和医疗卫生服务。下列实例与蛋白质变性无关的是( )
A. 利用高温、紫外线对医疗器械进行消毒 B. 将鸡蛋蒸煮后食用
C. 给重金属中毒的病人服用蛋白质 D. 胃蛋白酶帮助人体消化食物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D和E是原子序数依次增大前20号元素。A原子价电子层p轨道中只有1个电子;B、C、D元素的基态原子具有相同的能层数,B、D元素原子的p能级上都有1个未成对电子,D原子得一个电子填入3p轨道后,3p轨道已充满,C原子的p轨道中有3个未成对电子;E是同周期第一电离能最小的元素。回答下列问题:
(1)A的元素符号为 ___________、 B3+的结构示意图为___________、C的最高价氧化物对应水化物为____________;E的价电子排布式为______________。
(2)上述五种元素中最高价氧化物对应水化物酸性最强的是___________,(填写化学式)碱性最强物质的电子式为_____________; D所在周期(除稀有气体元素外)第一电离能最小的元素是_________;在AD3分子中A元素原子的杂化方式是__________,分子空间构型为_______________;
(3)准晶是一种无平移周期序但有严格准周期位置序的独特晶体,可通过____________方法区分晶体、准晶体和非晶体。
(4)C单质为面心立方晶体,其晶胞参数a=0.405nm,晶胞中铝原子的配位数为_____,列式表示Al单质的密度____________________g·cm﹣3(不必计算出结果)。
(5)石墨具有平面层状结构,同一层中的原子构成许许多多的正六边形,它与熔融的E单质相互作用,形成某种青铜色的物质(其中的元素E用“●”表示),原子分布如图所示,该物质的化学式为_______________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一密闭容器中,等物质的量的A和B发生反应:A(g)+2B(g) ![]() 2C(g),反应达平衡时,若混合气体中A和B的物质的量之和与C的物质的量相等,则这时A的转化率为( )
2C(g),反应达平衡时,若混合气体中A和B的物质的量之和与C的物质的量相等,则这时A的转化率为( )
A. 40% B. 50% C. 60% D. 70%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com