
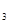 +H
+H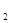 O
O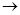 Al(OH)
Al(OH)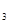 +N
+N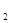 ↑+NaAlO
↑+NaAlO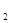 ,有关叙述正确的是( )
,有关叙述正确的是( )| A.上述反应中水是氧化剂 |
B.若反应过程中转移5 mol e 则生成标准状况下N 则生成标准状况下N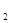 的体积为11.2L 的体积为11.2L |
C.该反应的氧化产物是N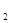 |
D.当消耗1 mol Al时,生成标况下N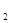 的体积为22.4L 的体积为22.4L |
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.升高 | B.降低 | C.不变 | D.不能确定 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.+2 价 | B.+3 价 | C.+4价 | D.+5价 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 的硝酸溶液中充分反应,产生NO气体,所得澄清溶液成分可看做是Fe(NO3)3、H2SO4的混合液,则反应中未被还原的硝酸可能为
的硝酸溶液中充分反应,产生NO气体,所得澄清溶液成分可看做是Fe(NO3)3、H2SO4的混合液,则反应中未被还原的硝酸可能为 mol
mol| A.①④ | B.②③ | C.①③ | D.②④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1/5 mol | B.2/5 mol |
| C.3/5mol | D.11/5 mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 2SO3,在一密闭容器中一定时间内达到平衡.
2SO3,在一密闭容器中一定时间内达到平衡.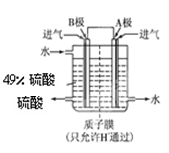
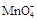 + —— Fe3++ Mn2++
+ —— Fe3++ Mn2++ 查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.氧化性由强到弱的顺序为KBrO3 > KClO3 > Cl2 > Br2 |
| B.①中KCl是氧化产物,KBr 发生还原反应 |
| C.③中1mol氧化剂参加反应得到电子的物质的量为2mol |
| D.反应②中氧化剂与还原剂的物质的量之比为1:6 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com