
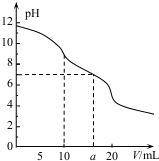
 常温下,用 0.1mol•L HCl溶液滴定10.0mL浓度为0.1mol•L-1 Na2CO3溶液,所得滴定曲线如图所示.下列说法正确的是( )
常温下,用 0.1mol•L HCl溶液滴定10.0mL浓度为0.1mol•L-1 Na2CO3溶液,所得滴定曲线如图所示.下列说法正确的是( )| A. | 当V=0时:c(H+)+c(H2CO3)+c(HCO3-)=c(OH-) | |
| B. | 当V=5时:c(Na+ )>c(HCO3-)>c(CO32- )>c(Cl- ) | |
| C. | 当V=a时:c(Na +)>c(Cl- )>c(H+ )=c(OH- ) | |
| D. | 当V=10时:c(H+ )+c(H2CO3)=c(OH- )+c(CO32-) |
分析 A.根据碳酸钠溶液中物料守恒和电荷守恒进行判断;
B.当V=5时,得到等浓度的NaHCO3、NaCl、Na2CO3混合溶液,CO32-、HCO3-溶液呈碱性,HCO3-的水解程度小于CO32-的水解程度;
C.根据V=a时,溶液的pH=7,则c(H+)=c(OH-),再根据电荷守恒判断溶液中钠离子与氯离子浓度关系;
D.当V=10时,反应恰好等浓度的NaHCO3、NaCl混合溶液,溶液中碳酸氢根离子既发生水解又发生电离,结合水电离的氢离子与氢氧根离子相等.
解答 解:A.当V=0时为碳酸钠溶液,根据电荷守恒可知:c(H+)+c(Na+)=c(OH-)+2c(CO32-)+c(HCO3-),根据物料守恒可得:c(Na+)=2c(HCO3-)+2c(H2CO3)+2c(CO32-),联立可得:c(H+)+c(HCO3-)+2c(H2CO3)=c(OH-),故A错误;
B.当V=5时,得到等浓度的NaHCO3、NaCl、Na2CO3混合溶液,CO32-、HCO3-溶液呈碱性,HCO3-的水解程度小于CO32-的水解程度,故溶液中:c(Na+ )>c(HCO3-)>c(Cl- )>c(CO32- ),故B错误;
C.v=a时,溶液的pH=7,溶液为中性,则c(H+)=c(OH-),根据电荷守恒可得:c(H+)+c(Na+)=c(OH-)+2c(CO32-)+c(Cl-)+c(HCO3-),联立可得c(Na+)=2c(CO32-)+c(HCO3-)+c(Cl-),所以c(Na+)>c(Cl-)>c(H+)=c(OH-),故C正确;
D.当V=10时,反应恰好等浓度的NaHCO3、NaCl混合溶液,由于水电离的氢离子与氢氧根离子相等,部分氢离子结合与碳酸氢根结合为碳酸分子,部分碳酸氢根电离产生碳酸根离子与氢离子,则c(H+ )+c(H2CO3)=c(OH- )+c(CO32-),故D正确.
故选:CD.
点评 本题考查了溶液中离子浓度大小比较、盐的水解原理,题目难度中等,注意理解掌握电荷守恒、物料守恒、质子恒等式在离子浓度大小比较中应用,A选项即可用运用质子恒等式判断.


 全能练考卷系列答案
全能练考卷系列答案 一课一练课时达标系列答案
一课一练课时达标系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
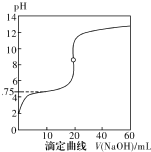 25℃时,用0.1000mol•L-1NaOH溶液滴定20mL0.1000mol•L-1一元酸HA(pKa=-lgKa=4.75)溶液,其滴定曲线如右图所示.下列说法正确的是( )
25℃时,用0.1000mol•L-1NaOH溶液滴定20mL0.1000mol•L-1一元酸HA(pKa=-lgKa=4.75)溶液,其滴定曲线如右图所示.下列说法正确的是( )| A. | 当滴人40mLNaOH溶液时,溶液中:c(Na+)>c(A-)>c(OH-)>c(H+) | |
| B. | 当溶液中c(H+)+c(OH-)=2×10-7时:c(Na+)>c(A-)>c(OH-)=c(H+) | |
| C. | 当滴人NaOH溶液20mL时c(OH-)>c(H+)+c(HA) | |
| D. | 当滴定到pH=4.75时,c(A-)=c(HA) |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | pH=2的HA溶液与pH=12的MOH溶液任意比混合:c(H+)+c(M+)=c(OH-)+c(A-) | |
| B. | B氨水和盐酸混合后溶液呈酸性,溶液中可能存在:c(NH4+)>c(Cl-) | |
| C. | 在一定温度下,相同pH的硫酸和硫酸铁溶液中水电离出来的c(H+)分别是1.0×0×10-amol/L和是1.0×10-bmol/L,在此温度时,水的离子积为1.0×10-(a+b) | |
| D. | 常温下,0.1mol/L酸HA pH=3,0.1mol/L 碱BOH pH=13,则盐BA溶液的pH<7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 坩埚的质量 | 坩埚的质量+晶体质量 | 失水后坩埚的质量+固体质量 |
| 11.70g | 14.2g | 13.2g |
| A. | 晶体中含有不分解的杂质 | B. | 没有放在干燥器中冷却 | ||
| C. | 实验前,晶体表面吸附水 | D. | 没有进行恒重操作 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 酸 | 电离方程式 | 电离常数 K/mol•L-1 |
| CH3COOH | CH3COOH?CH3COO-+H+ | 1.26×10-5 |
| H2CO3 | H2CO3?H++HCO3- HCO3-?CO32-+H+ | K1=4.31×10-7 K2=5.61×10-11 |
| H2S | H2S?H++HS- HS-?H++S2- | K1=9.1×10-8 K2=1.1×10-12 |
| H3PO4 | H3PO4?H++H2PO4- H2PO4-?H++HPO42- HPO42-?H++PO43- | K1=7.52×10-3 K2=6.23×10-8 K3=2.20×10-13 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氟酸的电离方程式及热效应可表示为:HF(aq)?H+(aq)+F-(aq)△H=+10.4kJ/mol | |
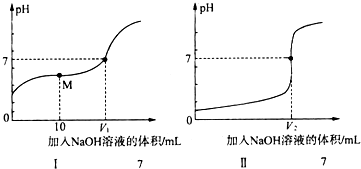
| B. | 当V=20 mL时,溶液中:c(OH-)=c(HF)+c(H+) | |
| C. | 当V=20 mL时,溶液中:c(F-)=c(Na+)=0.1mol/L | |
| D. | 当v>0时,溶液中一定存在c(Na+)>c(F-)>c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 操作步骤 | 现象 |
| 步骤1:向20mL0.05mol•L-1AgNO3溶液中加入20mL0.05mol•L-1KSCN溶液,充分反应后过滤 | 出现白色沉淀 |
| 步骤2:向滤液中滴加少量2mol•L-1Fe(NO3)3溶液 | 溶液变红色 |
| 步骤3:向步骤2所得溶液中,加入少量3mol•L-1AgNO3溶液 | 现象a |
| 步骤4:取步骤1所得少量滤渣加入到适量的3mol•L-1KI溶液中 | 出现黄色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | A2B3是三氧化二铝 | B. | A3+与B2-最外层上的电子数相同 | ||
| C. | A是第2周期第ⅢA族的元素 | D. | B是第3周期第ⅥA族的元素 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com