
 £®
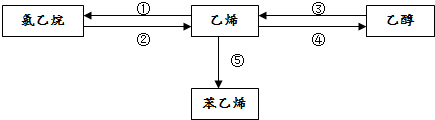
£®·ÖĪö £Ø1£©ĀČŅŅĶéŌŚĒāŃõ»ÆÄĘ“¼ČÜŅŗÖŠ·¢ÉśĻūČ„·“Ӧɜ³ÉŅŅĻ©£»ŅŅĻ©ÓėĖ®·¢Éś¼Ó³É·“Ӧɜ³ÉŅŅ“¼£»
£Ø2£©Āȱ½ŗĶŅŅĻ©ŌŚ“߻ƼĮ×÷ÓĆĻĀ·¢ÉśČ”“ś·“Ó¦±½ŅŅĻ©ŗĶĀČ»ÆĒā£»
£Ø3£©±ūĻ©ŌŚŅ»¶ØĢõ¼žĻĀÄÜÓėHCl·¢Éś¼Ó³É·“Ӧɜ³É1-ĀȱūĻ©»ņ2-ĀȱūĻ©£®
½ā“š ½ā£ŗ£Ø1£©ĀČŅŅĶéŌŚĒāŃõ»ÆÄĘ“¼ČÜŅŗÖŠ·¢ÉśĻūČ„·“Ӧɜ³ÉŅŅĻ©£¬·“Ó¦µÄ·½³ĢŹ½ĪŖCH3CH2Cl+NaOH$”ś_{”÷}^{ŅŅ“¼}$CH2=CH2”ü+NaCl£¬ŅŅĻ©ÓėĖ®·¢Éś¼Ó³É·“Ӧɜ³ÉŅŅ“¼£¬·“Ó¦µÄ·½³ĢŹ½ĪŖCH2=CH2+H2O$\stackrel{“߻ƼĮ}{”ś}$CH3CH2OH£¬¹Ź“š°øĪŖ£ŗCH3CH2Cl+NaOH$”ś_{”÷}^{ŅŅ“¼}$CH2=CH2”ü+NaCl£»CH2=CH2+H2O$\stackrel{“߻ƼĮ}{”ś}$CH3CH2OH£»
£Ø2£©Āȱ½ŗĶŅŅĻ©ŌŚ“߻ƼĮ×÷ÓĆĻĀ·¢ÉśČ”“ś·“Ó¦±½ŅŅĻ©ŗĶĀČ»ÆĒā£¬·“Ó¦µÄ·½³ĢŹ½ĪŖ £¬
£¬
¹Ź“š°øĪŖ£ŗ £»
£»
£Ø3£©±ūĻ©ŌŚŅ»¶ØĢõ¼žĻĀÄÜÓėHCl·¢Éś¼Ó³É·“Ӧɜ³É1-ĀȱūĻ©»ņ2-ĀȱūĻ©£¬½į¹¹¼ņŹ½ĪŖCH3CH2CH2Cl”¢CH3CHClCH3£¬¹Ź“š°øĪŖ£ŗCH3CH2CH2Cl£»CH3CHClCH3£®
µćĘĄ ±¾Ģāæ¼²éÓŠ»śĪļµÄŗĻ³É£¬ĪŖøßĘµæ¼µć£¬²ąÖŲӌѧɜµÄ·ÖĪöÄÜĮ¦µÄ漲飬±¾ĢāÉę¼°Ļ©”¢“¼”¢ĀČ“śĢžÖ®¼äµÄ×Ŗ»Æ¹ŲĻµµČ£¬ÄŃ¶Č²»“ó£¬×¢Ņā»ł“”ÖŖŹ¶µÄĄķ½āÕĘĪÕ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
| t/s | 0 | 120 | 180 | 240 | 330 | 530 | 600 | 700 | 800 |
| c/mol•L-1 | 0 | 0.036 | 0.030 | 0.026 | 0.022 | 0.017 | 0.016 | 0.015 | 0.015 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ķ¬ĪĀĶ¬Ń¹ĻĀ£¬ĻąĶ¬Ģå»żµÄĪļÖŹ£¬ĖüĆĒµÄĪļÖŹµÄĮæ±ŲĻąµČ | |
| B£® | ČĪŗĪĢõ¼žĻĀ£¬µČĪļÖŹµÄĮæµÄN2ŗĶCOĖłŗ¬µÄ·Ö×ÓŹż±ŲĻąµČ | |
| C£® | 1LŅ»Ńõ»ÆĢ¼ĘųĢåŅ»¶Ø±Č1LŃõĘųµÄÖŹĮ抔 | |
| D£® | ĢśµÄĦ¶ūÖŹĮæŌŚŹżÖµÉĻµČÓŚĢśŌ×ÓµÄĻą¶ŌŌ×ÓÖŹĮæ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | $\frac{n£ØA-N+8£©}{A+16}$mol | B£® | $\frac{n£ØA-N+2£©}{A}$ mol | C£® | $\frac{n£ØA-N+8£©}{A+8}$mol | D£® | $\frac{n£ØA-N-2£©}{A}$ mol |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | CH3CH3£¬C2H6 | B£® | -NO2£¬NO2 | C£® |  £¬OH- £¬OH- | D£® |  £¬ £¬ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | -128.1kJ/mol | B£® | -1295.3kJ/mol | C£® | -157.7kJ/mol | D£® | +157.7kJ/mol |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 Čē±ķÖŠµÄŹż¾ŻŹĒĘĘ»µ1molĪļÖŹµÄ»Æѧ¼üĖłĻūŗĵÄÄÜĮæ£ŗ
Čē±ķÖŠµÄŹż¾ŻŹĒĘĘ»µ1molĪļÖŹµÄ»Æѧ¼üĖłĻūŗĵÄÄÜĮæ£ŗ| ĪļÖŹ | Cl2 | Br2 | I2 | HCl | HBr | HI | H2 |
| ÄÜĮæ£ØkJ£© | 243 | 193 | 151 | 431 | 366 | 298 | 436 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ²Ł ×÷ | ĻÖĻó | ½įĀŪ |
| ȔɣĮæ³ż¾”Ag+ŗóµÄČÜŅŗÓŚŹŌ¹ÜÖŠ£¬¼ÓČĖKSCNČÜŅŗ£¬Õńµ“ | £Ø1£© | “ęŌŚFe3+ |
| ȔɣĮæ³ż¾”Ag+ŗóµÄČÜŅŗÓŚŹŌ¹ÜÖŠ£¬¼ÓČė £Ø2£©£¬Õńµ“ | £Ø3£© | “ęŌŚFe2+ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 °±ĘųŅ×Ņŗ»Æ£¬±ćÓŚ“¢ŌĖ£¬æÉĄūÓĆNH3×÷“¢Ēā²ÄĮĻ
°±ĘųŅ×Ņŗ»Æ£¬±ćÓŚ“¢ŌĖ£¬æÉĄūÓĆNH3×÷“¢Ēā²ÄĮĻ²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com