
”¾ĢāÄæ”æ100mL2mol/LµÄĮņĖįŗĶ¹żĮæµÄŠæʬ·“Ó¦£¬ĪŖĮĖ¼Óæģ·“Ó¦ĖŁĀŹ,µ«ÓÖ²»Ó°ĻģÉś³ÉĒāĘųµÄ×ÜĮ棬²»ŅĖ²ÉČ”µÄ“ėŹ©ŹĒ
A. øÄÓĆŠæ·Ū B. ÉżĪĀ·“Ó¦ĢåĻµµÄĪĀ¶Č
C. ¼ÓČėÉŁĮæµÄCuSO4ČÜŅŗ D. øÄÓĆ200mLlmol/LµÄĮņĖį
”¾“š°ø”æD
”¾½āĪö”æĢāÄæÖŠŅŖĒó²»Ó°ĻģÉś³ÉĒāĘųµÄĮ棬Ņņ“ĖĖł¼ÓĪļÖŹ²»ÄÜĻūŗÄĒāĄė×Ó£¬ĢįøßĖŁĀŹµÄ°ģ·ØÓŠÉżøßĪĀ¶Č£¬Ōö“óÅØ¶Č£¬Ōö“ó½Ó“„Ć껿£¬ŠĪ³ÉŌµē³ŲµČ”£A”¢øÄÓĆŠæ·Ū£¬Ōö“óĮĖĆ껿£¬æÉŅŌ¼Óæģ·“Ó¦ĖŁĀŹ”£ÕżČ·£»B”¢ÉżĪĀ·“Ó¦ĢåĻµµÄĪĀ¶ČæÉŌö¼Ó·“Ó¦ĖŁĀŹ”£ÕżČ·£»C”¢¼ÓČėÉŁĮæµÄCuSO4ČÜŅŗÓŠÉŁĮæĶ±»ÖĆ»»£¬ÓėŠæŠĪ³ÉŌµē³Ų£¬¼ÓĖŁ·“Ó¦”£ÕżČ·£»D”¢ĖäČ»ĒāĄė×ÓµÄ×ÜĮæĆ»±ä£¬µ«ÅØ¶Č¼õŠ”ĮĖ£¬·“Ó¦ĖŁĀŹ¼õŠ””£“ķĪó£»¹ŹŃ”D



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æČÜŅŗXæÉÄÜŗ¬ÓŠNa+”¢Fe3+”¢Ca2+”¢SO42-”¢ CO32- ”¢Cl-”¢I-ÖŠµÄ¼øÖÖĄė×Ó”£ĪŖČ·¶ØĘä×é³É£¬Éč¼Ę²¢Ķź³ÉŅŌĻĀŹµŃé£ŗ

øł¾ŻÉĻŹöŹµŃ飬ŅŌĻĀĶĘ²āŗĻĄķµÄŹĒ
A. ČÜŅŗXÖŠŹĒ·ń“ęŌŚNa+»¹ŠčŅŖĶعżŃęÉ«·“Ó¦½ųŅ»²½Č·ČĻ
B. ČÜŅŗXÖŠŅ»¶Ø²»ŗ¬Fe3+”¢Ca2+”¢SO42-
C. ĪŖČ·¶ØČÜŅŗXÖŠŹĒ·ńŗ¬ÓŠCl-£¬æÉČ”ČÜŅŗ2¼ÓČėCCl4³ä·ÖŻĶČ”ŗó£¬ŌŁČ”ÉĻ²ćŅŗĢå¼ÓČėAgNO3ČÜŅŗ
D. ČÜŅŗXµÄČÜÖŹĪŖNa2CO3ŗĶNaI
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻÖÓŠĮ½ÖÖµķ·ŪĆøAÓėB£¬Ä³ÉśĪļŠĖȤŠ”×éĪŖĢ½¾æ²»Ķ¬ĪĀ¶ČĢõ¼žĻĀÕāĮ½ÖÖµķ·ŪĆøµÄ»īŠŌ£¬Éč¼ĘČēĻĀĢ½¾æŹµŃé:
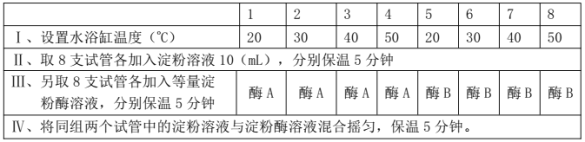
ŹµŃé½į¹ū£ŗ¶Ōø÷×éµķ·ŪŹ£ÓąĮæ½ųŠŠ¼ģ²ā£¬½į¹ūČēĻĀĶ¼ĖłŹ¾”£
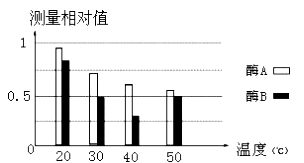
£Ø1£©øĆŹµŃéµÄ×Ō±äĮæŹĒ ŗĶ ”£
£Ø2£©øł¾ŻŹµŃé½į¹ū·ÖĪö£¬ĆøBŌŚ ”ęĢõ¼žŹ±»īŠŌ½Ļøß”£
£Ø3£©±¾ŹµŃéÄܲ»ÄÜÓĆģ³ĮÖŹŌ¼Į¼ģ²āÉś³ÉĪļĀóŃæĢĒµÄŗ¬ĮæĄ“±ķŹ¾£æ £¬ĄķÓÉŹĒ ”£
£Ø4£©ČōŅŖ½ųŅ»²½Ģ½¾æĆøBµÄ×īŹŹĪĀ¶Č£¬ŹµŃéÉč¼ĘµÄÖ÷ŅŖĖ¼Ā·Ó¦ŹĒŌŚ ”ęÖ®¼äÉčĮ¢½ĻŠ”µČĪĀ¶Č”õĢŻ¶ČµÄ·Ö×鏵Ń飬°“ÉĻŹö²½Öč½ųŠŠŹµŃ飬·ÖĪö½į¹ūµĆ³ö½įĀŪ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”潚Źō¼ŲµÄŅ±Į¶æɲÉÓĆČēĻĀ·½·Ø£ŗ2KF+CaC21237”«1423CCaF2+2K”ü+2C£¬ĻĀĮŠÓŠ¹ŲĖµ·ØŗĻĄķŹĒ
A£®øĆ·“Ó¦µÄŃõ»Æ¼ĮŹĒKF£¬Ńõ»Æ²śĪļŹĒK
B£®øĆ·“Ó¦ÄÜĖµĆ÷CµÄ»¹ŌŠŌ“óÓŚK
C£®µē½āKFČÜŅŗ²»æÉÄÜÖʱø½šŹō¼Ų
D£®CaC2”¢CaF2¾łĪŖĄė×Ó»ÆŗĻĪļ£¬ĒŅŅõ”¢ŃōĄė×ÓøöŹż±Č¾łĪŖ2”Ć1
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĶéĢžµÄŅ»ĀČČ”“śĪļ֊ƻӊĶ¬·ÖŅģ¹¹ĢåµÄŹĒ(””””)
A.2”Ŗ¼×»ł±ūĶéB.±ūĶéC.¶”ĶéD.ŅŅĶé
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ£Ø1£©KClO3æÉÓĆÓŚŹµŃéŹŅÖĘO2£¬Čō²»¼Ó“߻ƼĮ£¬400 ”ꏱ·Ö½āֻɜ³ÉĮ½ÖÖŃĪ£¬ĘäÖŠŅ»ÖÖŹĒĪŽŃõĖįŃĪ£¬ĮķŅ»ÖÖŃĪµÄŅõŃōĄė×ÓøöŹż±ČĪŖ1”Ć1”£Š“³öøĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½£ŗ ____________________”£
£Ø2£©ŌŚÄ³ĒæĖįŠŌ»ģŗĻĻ”ĶĮČÜŅŗÖŠ¼ÓČėH2O2£¬µ÷½ŚpH”Ö3£¬Ce3£«ĶعżĻĀĮŠ·“Ó¦ŠĪ³ÉCe(OH)4³ĮµķµĆŅŌ·ÖĄė”£Ķź³É·“Ó¦µÄĄė×Ó·½³ĢŹ½£ŗ______________________
![]() Ce3£«£«
Ce3£«£«![]() H2O2£«
H2O2£«![]() H2O===
H2O===![]() Ce(OH)4”ż£«
Ce(OH)4”ż£«![]() ________
________
£Ø3£©AsæÉŅŌÓėNaClOµÄĖ®ČÜŅŗ·“Ó¦£¬Éś³ÉĘä×īøß¼Ūŗ¬ŃõĖį(H3AsO4)£¬Š“³öøĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½ £ŗ _____”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æijŠ£»ÆѧŠĖȤŠ”×éĪŖĢ½¾æĢśÓėÅØĮņĖį·“Ó¦£¬Éč¼ĘĮĖĶ¼1”¢Ķ¼2ĖłŹ¾×°ÖĆ½ųŠŠŹµŃ锣

£Ø1£©±Č½ĻĮ½ŹµŃé×°ÖĆ£¬Ķ¼2ĖłŹ¾×°ÖƵÄÓŵćŹĒ£ŗ
¢ŁÄÜøüŗƵŲĪüŹÕÓŠ¶¾ĘųĢåSO2£¬·ĄÖ¹ĘäĪŪČ¾»·¾³£»
¢Ś_________________________________________________”£
£Ø2£©ÄÜĖµĆ÷ÓŠSO2ĘųĢå²śÉśµÄŹµŃéĻÖĻóŹĒ_________________________”£
£Ø3£©·“Ó¦Ņ»¶ĪŹ±¼äŗó£¬ÓƵĪ¹ÜĪüČ”AŹŌ¹ÜÖŠµÄČÜŅŗµĪČĖŹŹĮæĖ®ÖŠĪŖŹŌŃł£¬ŹŌŃłÖŠĖłŗ¬½šŹōĄė×ӵijɷÖÓŠŅŌĻĀČżÖÖæÉÄÜ£ŗ
I£®Ö»ŗ¬ÓŠFe3+£»II£®Ö»ŗ¬ÓŠFe2+£»III£®¼ČÓŠFe3+ÓÖÓŠFe2+”£
ĪŖŃéÖ¤¢ņ”¢¢óµÄæÉÄÜŠŌ£¬Ń”ÓĆČēĻĀŹŌ¼Į£¬ĢīŠ“ĻĀĮŠæÕøń£ŗ
A£®Ļ”ŃĪĖįČÜŅŗ B£®Ļ”ĮņĖįČÜŅŗ C£®KSCNČÜŅŗ D£®KMnO4ČÜŅŗ
E£®NaOHČÜŅŗ F£®µķ·Ū”ŖKIČÜŅŗ G£®H2O2ČÜŅŗ
ŃéÖ¤¢ņ£ŗČ”ŹŌŃł£¬ĻȵĪ¼ÓÉŁĮæµÄ____________(ĢīŹŌ¼ĮŠņŗÅ£¬ĻĀĶ¬)£¬Õńµ“£¬ŌŁµĪ¼ÓÉŁĮæµÄ___________£¬øł¾ŻČÜŅŗŃÕÉ«µÄ±ä»ÆæÉČ·¶Ø¼ŁÉč¢ņŹĒ·ńÕżČ·”£
ŃéÖ¤¢ó£ŗ²½Öčl Č”ŹŌŃł£¬µĪ¼ÓÉŁĮæµÄ______________(ĢīŹŌ¼ĮŠņŗÅ)£¬ČÜŅŗµÄŃÕÉ«±ä____É«£¬ŌņŹŌŃłÖŠŗ¬ÓŠFe3+£¬·¢Éś·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ________”£
²½Öč2 ŌŁČ”ŹŹĮæµÄŹŌŃłµĪ¼ÓÉŁĮæµÄ_______________________ (ĢīŹŌ¼ĮŠņŗÅ)£¬ČÜŅŗµÄŃÕÉ«±äĪŖ_____________£¬ŌņŹŌŃłÖŠŗ¬ÓŠFe2+”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅ»¶ØĢõ¼žĻĀ£¬Ņ»ÖÖ·“Ó¦Īļ¹żĮ棬ĮķŅ»ÖÖ·“Ó¦ĪļČŌ²»ÄÜĶźČ«·“Ó¦µÄŹĒ£Ø £©
A. ¹żĮæµÄĒāĘųÓėµŖĘų B. ¹żĮæµÄÅØŃĪĖįÓė¶žŃõ»ÆĆĢ
C. ¹żĮæµÄĶÓėÅØĮņĖį D. ¹żĮæµÄŠæÓė18 mol/LĮņĖį
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĮ¬¶žŃĒĮņĖįÄĘ£ØNa2S2O4£©ÓÖ³Ę±£ĻÕ·Ū£¬ŹĒ°×ɫɰד»ņµ»ĘÉ«·ŪÄ©¹ĢĢ壬¼ŗÖŖĮ¬¶žŅµĮņĖįÄĘŌŚ¼īŠŌĢõ¼žĻĀ½ĻĪČ¶Ø£¬Ņ×±»æÕĘųŃõ»Æ£¬²»ČÜÓŚ¼×“¼£¬ÓöĖ®ŃøĖŁ·Ö½ā£¬Ä³Ķ¬Ń§Éč¼ĘĄūÓĆČēĻĀĶ¼ĖłŹ¾µÄŹµŃé×°ÖĆÖʱøŅ»¶ØĮæµÄĮ¬¶žŃĒĮņĖįÄĘ£¬×°ÖĆCÖŠµÄŹŌ¼ĮĪŖ¼×ĖįÄĘ£ØHCOONa£©”¢NaOH µÄ¼×“¼ČÜŅŗ£¬»Ų“šĻĀĮŠĪŹĢā£ŗ
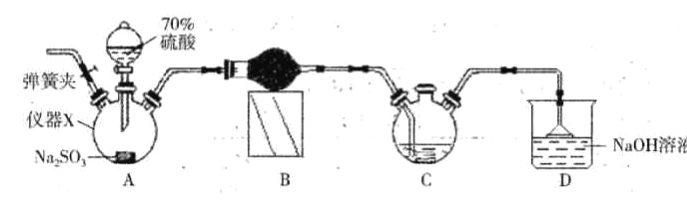
£Ø1£©ŅĒĘ÷XµÄĆū³ĘŹĒ_____”£×°ÖĆBÖŠµÄĒņŠĪøÉŌļ¹ÜÖŠŹ¢×°µÄŹŌ¼ĮŹĒ_______”£
£Ø2£©×°ÖĆDµÄ×÷ÓĆŹĒ___________”£ŹµŃ鏱ŠčŅŖ½«CÖŠĪĀ¶ČæŲÖĘŌŚ70-75”ę£¬×īŗƵÄæŲÖĘ·½·ØŹĒ__________”£
£Ø3£©ŹµŃéæŖŹ¼Ź±ĻČ“ņæŖ×°ÖĆAÖŠµÄµÆ»É¼ŠĶØČėŅ»¶ĪŹ±¼äN2µÄÄæµÄŹĒ______”£ŹµŃé¹ż³Ģ֊װÖĆC ÖŠ³żÓŠĘųĢå²śÉśĶā£¬»¹ÄܹŪ²ģµ½µÄŹµŃéĻÖĻóĪŖ____________”£
£Ø4£©ÓŠĶ¬Ń§Ķعż×ŠĻøĖ¼æ¼ŗóČĻĪŖ£¬»¹Ó¦ŌŚC”¢D Ö®¼äĢķ¼ÓŅ»øö×°ÖĆ£¬²ÅÄÜČ·±£CÖŠÉś³ÉÄÜĪČ¶Ø“ęŌŚµÄĮ¬¶žŃĒĮņĖįÄĘ£¬ŌņøĆ×°ÖĆÓ¦¾ßÓŠµÄ¹¦ÄÜŹĒ______”£ĪŖµĆµ½½Ļ“æµÄĮ¬¶žŃĒĮņĖįÄĘ£¬ŠčŅŖ¶ŌŌŚ¹żĀĖŹ±µĆµ½µÄĮ¬¶žŃĒĮņĖįÄĘ½ųŠŠĻ“µÓ£¬Ļ“µÓµÄ·½·ØŹĒ_________”£
£Ø5£©ČōŹµŃéÖŠĖłÓĆNa2SO3µÄÖŹĮæĪŖ12.6g £ØĮņĖįŹĒ¹żĮæµÄ£©£¬×īÖÕµĆµ½m gøÉŌļµÄĮ¬¶žŃĒĮņĖįÄĘ£¬ŌņĮ¬¶žŃĒĮņĖįÄĘµÄ²śĀŹĪŖ_____________”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com