
 碳是地球上含量丰富的元素,其氧化物的研究有着重要意义.
碳是地球上含量丰富的元素,其氧化物的研究有着重要意义.分析 (1)由图可知,1mol NO2和1mol CO反应生成CO2和NO放出热量368-134=234kJ,根据热化学方程式书写原则进行书写;
(2)加入催化剂,降低反应物的活化能,反应速率加快;
(3)依据盖斯定律和热化学方程式计算得到所需热化学方程式,注意燃烧热是1mol可燃物完全燃烧生成稳定氧化物放出的热量;
(4)依据反应自发碱性的判断依据分析判断,△H-T△S<0反应自发进行.
解答 解:(1)由图可知,1mol NO2和1mol CO反应生成CO2和NO放出热量368-134=234kJ,反应热化学方程式为NO2(g)+CO(g)=NO(g)+CO2(g)△H=-234 kJ/mol,
故答案为:NO2(g)+CO(g)=NO(g)+CO2(g)△H=-234 kJ/mol;
(2)加入催化剂,降低反应物的活化能,反应速率加快,图象应为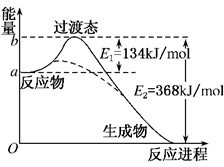 ,
,
故答案为:
(3)①N2(g)+O2(g)=2NO(g)△H=+180kJ/mol
②2NO(g)+2CO(g)=N2(g)+2CO2(g)△H=-746kJ/mol
依据盖斯定律①+②得到2CO(g)+O2(g)=2CO2(g)△H=-566KJ/mol,
燃烧热是1mol可燃物完全燃烧生成稳定氧化物放出的热量,则一氧化碳燃烧热的热化学方程式为:CO(g)+$\frac{1}{2}$O2(g)=CO2(g)△H=-283kJ•mol-1,
故答案为:CO(g)+$\frac{1}{2}$O2(g)=CO2(g)△H=-283kJ•mol-1;
(4)2CO(g)=2C(s,石墨)+O2(g)△H>0,△S<0,△G=△H-T△S>0,反应不能自发进行,不能实现此反应,
故答案为:否,该反应△G始终大于0,是非自发反应;
点评 本题考查反应热的有关计算以及催化剂对反应活化能的影响,反应自发进行的判断依据,题目难度中等,注意热化学方程式的计算以及加入催化剂,降低反应物的活化能.


科目:高中化学 来源: 题型:选择题
| A. | 稀盐酸,Na2CO3溶液 | B. | 硫酸铝溶液,氨水 | ||
| C. | 碳酸氢钠溶液,澄清石灰水 | D. | 二氧化碳,氢氧化钠溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②④⑥⑦ | B. | ①④⑤⑦ | C. | ①④⑦ | D. | ②③⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C2H4O和C3H6O均满足饱和一元醛的通式,因此它们一定互为同系物 | |
| B. | 乙烯和苯均可使溴水褪色,但是其褪色原理不同 | |
| C. | 乙烯和苯分子中各原子都在同一平面 | |
| D. | 检验乙烷中是否含有乙烯,试剂为酸性高锰酸钾溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 烃CnH2n+2 | B. | 醇CnH2n+2O | C. | 醛CnH2nO | D. | 羧酸CnH2nO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com