
| A. | 同温度、同浓度的NaCl溶液和氨水的导电能力 | |
| B. | 25℃时.pH均为2的盐酸和CH3COOH溶液中溶质的物质的量浓度 | |
| C. | 25℃时,pH均为2的H2SO4溶液和盐酸中氢离子的物质的量浓度 | |
| D. | 25℃时.pH均为3的盐酸和FeCI3溶液中水的电离程度 |
分析 A.氯化钠是强电解质完全电离,氨水是弱电解质部分电离;
B.盐酸是强酸完全电离,乙酸是弱酸部分电离;
C.pH均为2,C〔H+〕=1×10-2mol/L;
D.盐酸是强电解质完全电离,三氯化铁是强酸弱碱盐水解.
解答 解:A.同温度、同浓度的NaCl溶液和氨水,氯化钠是强电解质完全电离NaCl=Na++Cl-,电离出的离子浓度等于氯化钠浓度的两倍,而氨水是弱电解质,部分电离,所以电离出的离子小于其浓度的了两倍,离子浓度大导电能力强,所以,导电能力前者比后者大,故A正确;
B.根据pH=-lgC〔H+〕公式,pH均为2,H2SO4溶液和盐酸中氢离子的物质的量浓度C〔H+〕=1×10-2mol/L,盐酸是强酸完全电离,所以,盐酸的物质的量浓度等于1×10-2mol/L,乙酸是弱酸部分电离,它的物质的量的浓度大于1×10-2mol/L,前者小,后者大,故B错误;
C.根据pH=-lgC〔H+〕公式,pH均为2,H2SO4溶液和盐酸中氢离子的物质的量浓度C〔H+〕=1×10-2mol/L,两者相等,故C错误;
D.水的电离方程式:H2O?H++OH-,加入酸或碱抑制水的电离,加入能水解的盐促进水的电离,盐酸是强电解质完全电离,三氯化铁是强酸弱碱盐水解,所以前者抑制水的电离,后者促进水的电离,前者小于后者,故D错误;
故选A.
点评 本题考查了水的电离和强弱电解质的电离,注意pH=-lgC〔H+〕公式与氢离子浓度间的关系,题目不难.


 华东师大版一课一练系列答案
华东师大版一课一练系列答案科目:高中化学 来源: 题型:选择题
| A. | v(Fe)=0.5 mol•L-1•min-1 | B. | v(H2SO4)=1 mol•L-1•min-1 | ||
| C. | v(H2)=0.05 mol•L-1•min-1 | D. | v(FeSO4)=0.5 mol•L-1•min-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 蒸发 | B. | 蒸馏 | C. | 过滤 | D. | 分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 物质类别 | 酸 | 碱 | 盐 | 氧化物 | 氢化物 |
| 化学式 | ①HCl ②H2SO4 | ③NaOH ④Ba(OH)2 | ⑤Na2CO3 ⑥K2SO4 | ⑦CO2 ⑧Na2O | ⑨NH3 ⑩H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol•L-1的NaCl溶液是指由1mol NaCl和1000mL水配制成的溶液 | |
| B. | 从1L 0.5mol•L-1的NaCl溶液中取出100mL,剩余溶液物质的量浓度为0.45mol•L-1 | |
| C. | 标准状况下,18克H2O所含的氧原子数目为NA | |
| D. | 0℃时,2mol Cl2的体积不可能为22.4L |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
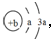 ,Y、Z为同周期金属元素,其中Y为短周期元素中原子半径最大的元素,Z为地壳中含量最高的金属元素,W的最高价氧化物对应水化物可以与其气态氢化物反应生成盐G,盐G溶液呈酸性,回答下列问题:
,Y、Z为同周期金属元素,其中Y为短周期元素中原子半径最大的元素,Z为地壳中含量最高的金属元素,W的最高价氧化物对应水化物可以与其气态氢化物反应生成盐G,盐G溶液呈酸性,回答下列问题: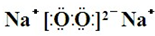 ,所含有的化学键类型为离子键和共价键.
,所含有的化学键类型为离子键和共价键.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com