
已知同周期两种非金属元素X、Y,电负性X>Y,下列说法错误的是
| A.含氧酸的酸性:X对应的强于Y对应的 | B.气态氢化物的稳定性:HmX强于HnY |
| C.第一电离能可能Y大于X | D.X与Y形成化合物时,X显负价,Y显正价 |
【答案】C
【解析】本题考查了电负性的知识。同周期元素,自左而右元素的电负性增强,电负性X>Y,故非金属性X>Y。非金属性越强,最高价含氧酸的酸性越强,非金属性X>Y,所以最高价含氧酸的酸性:X强于Y,故A正确,不选。非金属性越强,气态氢化物越稳定,非金属性X>Y,所以氢化物的稳定性:HmX强于HnY,故B正确,不选。若Y的第一电离能失去的电子所处能级为半满稳定状态,其第一电离能可能高于X的第一电离能,如第一电离能P>S,故C错,选C。电负性表示原子对键合电子吸引力的大小,电负性越大的原子,对键合电子的吸引力越大,电负性X>Y,键合电子偏向X原子,偏离Y原子,则X与Y形成化合物中,X显负价,Y显正价,故D正确,不选。


科目:高中化学 来源: 题型:
根据下表的数据,H2(g)+Cl2(g)=2HCl(g)的反应热为:( )
| H2 | Cl2 | HCl | |
| 键能/(KJ/mol) | 436 | 243 | 431 |
|
| A. | +183.0 KJ/mol | B. | ﹣366.0 KJ/mol |
|
| C. | +211.0 KJ/mol | D. | ﹣183.0 KJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
有四种混和溶液,分别由0.1mol/L CH3COONa溶液与等体积、等浓度的四种溶液混和而成:①HCl,②NaOH,③NaCl,④NaHCO3.关于混和后的溶液下列各项排序正确的是( )
|
| A. | pH:②>③>④>① | B. | c(CH3COO﹣):②>④>③>① |
|
| C. | c(H+):①>③>②>④ | D. | c(CH3COOH):①>④>③>② |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列对难溶电解质的溶解平衡的叙述,错误的是
A.难溶电解质的溶解平衡是一种动态平衡
B.达到溶解平衡时,沉淀的速率和溶解的速率相等,溶液中离子的浓度保持不变
C.达到溶解平衡时,溶液中各种离子的浓度不一定相等
D.达到溶解平衡时,再加入该难溶电解质,将促进其溶解
查看答案和解析>>
科目:高中化学 来源: 题型:
我国是个钢铁大国,钢铁产量为世界第一,高炉炼铁是最为普遍的炼铁方法。
I.已知反应Fe2O3(s)+ CO(g)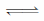 Fe(s)+ CO2(g) ΔH=-23.5kJ·mol-1,该反应在1000℃的平衡常数等于4。在一个容积为10L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0mol,应经过l0min后达到平衡。
Fe(s)+ CO2(g) ΔH=-23.5kJ·mol-1,该反应在1000℃的平衡常数等于4。在一个容积为10L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0mol,应经过l0min后达到平衡。
(1)CO的平衡转化率=____________
(2)欲提高CO的平衡转化率,促进Fe2O3的转化,可采取的措施是________。
a.提高反应温度
b.增大反应体系的压强
c.选取合适的催化剂
d.及时吸收或移出部分CO2
e.粉碎矿石,使其与平衡混合气体充分接触
Ⅱ.高炉炼铁产生的废气中的CO可进行回收,使其在一定条件下和H2反应制备甲醇:CO(g)+ 2H2(g) 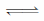 CH3OH(g)。请根据图示回答下列问题:
CH3OH(g)。请根据图示回答下列问题:
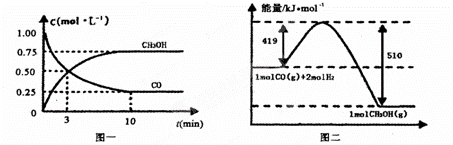
(3)从反应开始到平衡,用H2浓度变化表示平均反应速率v(H2)=________。
(4)已知氢气的燃烧热286kJ/mol,请写出甲醇气体不充分燃烧的热化学方程式____________________________________________________________________。
(5)若在温度和容器相同的三个密闭容器中,按不同方式投入反应物,测得反应达到平衡吋的有关数据如下表:
| 容器 | 反应物投入的量 | 反应物的 转化率 | CH3OH的浓度 | 能量变化 (Q1、Q2、Q3均大于0) |
| 甲 | 1mol CO和2mol H2 | α1 | c1 | 放出Q1kJ热量 |
| 乙 | 1mol CH3OH | α2 | c2 | 吸收Q2kJ热量 |
| 丙 | 2mol CO和4mol H2 | α3 | c3 | 放出Q3kJ热量 |
则下列关系正确的是________
A.c1=c2
B.2Q1=Q3
C.2α1=α3
D.α1+α2 =1
E.该反应若生成1mol CH3OH,则放出(Q1+Q2)kJ热量
Ⅲ.以甲烷为燃料的新型电池,其成本大大低于以氢为燃料的传统燃料电池,目前得到广泛的研究,如图是目前研究较多的一类固体氧化物燃料电池工作原理示意图。回答下列问题:
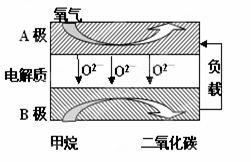
(6) B极上的电极反应式为 。
(7)若用该燃料电池做电源,用石墨做电极电解100mL 1mol/L的硫酸铜溶液,当两极收集到的气体体积相等时,理论上消耗的甲烷的体积为 (标况下)。
查看答案和解析>>
科目:高中化学 来源: 题型:
化学用语是学习化学的工具和基础。下列有关化学用语的使用正确的是
A.食醋呈酸性的原因是:CH3COOH+H2O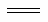 CH3COO-+H3O+
CH3COO-+H3O+
B.纯碱溶液呈碱性的原因是: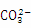 +2H2O
+2H2O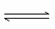 H2CO3+2OH-
H2CO3+2OH-
C.用铁作阳极,电解饱和食盐水的离子方程式:Fe+2H2O Fe(OH)2+H2↑
Fe(OH)2+H2↑
D.表示氢气燃烧热的热化学方程式为:2H2(g)+O2(g)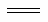 2H2O(l);
2H2O(l); H=-571.6kJ·mol-1
H=-571.6kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
部分氧化的FeCu合金样品(氧化产物为Fe2O3、CuO)共5.76 g,经如下处理:

下列说法正确的是
| A.V=44.8 | B.原样品中Fe元素的质量分数为38.89% |
| C.滤液A中的阳离子为Fe2+、Fe3+、H+ | D.样品中CuO的质量为4.0 g |
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,有下列四种溶液:①pH=2的CH3COOH溶液;②pH=2的HCl溶液;③pH=12的氨水;④pH=12的NaOH溶液.下列有关说法正确的是( )
|
| A. | 四种溶液的KW相同,由水电离的c(H+):①=③>②=④ |
|
| B. | 向等体积的四种溶液中分别加入100 mL水后,溶液的pH:③>④>②>① |
|
| C. | ②、④溶液分别与足量铝粉反应,生成H2的量:②最大 |
|
| D. | 将②、③两种溶液混合后,若pH=7,消耗溶液的体积为:③>② |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知磷酸分子中的三个氢原子都可以跟重水分子(D2O)中的D原子发生氢交换.又知次磷酸(H3PO2)也可跟D2O进行氢交换,但次磷酸钠(NaH2PO2)却不能跟D2O发生氢交换.由此可推断出H3PO2的分子结构是( )

|
| A. |
| B. |
| C. |
| D. |
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com