


分析 (1)已知UF6在常温常压下是固体,在56.4℃升华成气体,其沸点低,所以UF6是分子晶体;
(2)甲基上的碳是sp3杂化,其它碳是sp2杂化;Cu元素为29号元素,原子核外有29个电子,所以核外电子排布式为:1s22s22p63s23p63d104s1;
(3)①在该离子内部含有的化学键类型有碳氢和碳氮极性共价键,碳碳非极性共价键,以及铜与氮之间形成的配位键;
②根据形成氢键的条件分析;
③利用判断σ键的规律来分析σ键数目和π键的数目;
(4)外界电离,内界不电离,以及Ag++Cl-=AgCl↓,来分析求解.
解答 解:(1)已知UF6在常温常压下是固体,在56.4℃升华成气体,其沸点低,所以UF6是分子晶体,故答案为:分子;
(2)甲基上的碳是sp3杂化,其它碳是sp2杂化,Cu元素为29号元素,原子核外有29个电子,所以核外电子排布式为:1s22s22p63s23p63d104s1,所以外围电子排布式为:3d104s1,故答案为:sp3、sp2;3d104s1;
(3)某铜的配合物在煤的液化中起催化作用,其阳离子结构如下图.
①在该离子内部含有的化学键类型有碳氢和碳氮极性共价键,碳碳非极性共价键,以及铜与氮之间形成的配位键,故选:bcd;
②电负性较强的元素如N、O、F与H形成共价键时,能形成氢键,而C的电负性较弱,与H形成共价键后,不能形成氢键,
故答案为:甲醛分子中氢原子与碳原子形成共价键,碳的电负性较小,不构成形成氢键的条件;
③甲醛中含有一个C=O,C=O由1个π键和1个σ键构成和2个碳氢σ键构成,所以σ键和π键的个数比为3:1,故答案为:3:1;
(4)1mol该配合物与足量AgNO3溶液反应生成2mol AgCl沉淀,说明3-n=2,所以n=1,又因为具有6 配位所以m=5,故答案为:5;1.
点评 本题考查了分子的类型的判断和原子的杂化方式,涉及电子排布式、晶体的判断、氢键、化学键的判断等,考查的知识点较多,综合性较强.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| t℃ | 700 | 800 | 830 | 1 000 | 1 200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 吸热反应中,反应物的总能量大于生成物的总能量 | |
| B. | 形成化学键的过程会释放能量 | |
| C. | 加热才能发生的反应一定是吸热反应 | |
| D. | 氧化反应均为吸热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 既能发生取代反应,也能发生加成反应 | |
| B. | 在浓硫酸催化下加热脱水,可以生成不止一种四烯烃 | |
| C. | 1mol橙花醇与浓氢溴酸反应,最多消耗3mol HBr | |
| D. | 1mol橙花醇在室温下与溴的四氯化碳溶液反应,最多消耗 480g Br2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 对比实验 | 试管A | 试管B |
| 加入试剂 | 1ml0.05mol/l KMnO4 2ml0.1mol/l H2C2O4 | 1ml0.05mol/lKMnO4 2ml0.1mol/lH2C2O4 少量MnSO4 |
| (预期)实验现象 (褪色时间) | 褪色较慢 | 褪色很快 |
| 结论 | 猜想Ⅱ正确 | |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 冰熔化时,分子中H-O键发生断裂 | |
| B. | HI比HF易分解,是因为HI分子间不存在氢键 | |
| C. | 非极性键不可能存在于离子化合物中,由非金属元素组成的化合物中一定不存在离子键 | |
| D. | 含有阴离子的物质一定含有阳离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
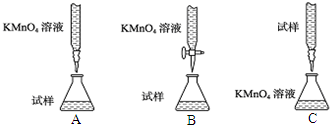
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在Na2CO3的水溶液中存在:2c(Na+)=c(CO32-)+c(HCO3-)+2c(H2CO3) | |
| B. | pH=3盐酸与pH=11氨水等体积混合时有:c(NH4+)=c(Cl-)>>c(H+)=c(OH-) | |
| C. | pH均为9的Na2CO3和CH3COONa溶液,二者的水解程度相同 | |
| D. | 在氨水中加水稀释,溶液中$\frac{c(N{H}_{4}^{+})}{c(N{H}_{3}•{H}_{2}O)}$ 增大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com