分析:A、根据在离子化合物中,相同的离子要分开写,并且要对称;
B、根据共价化合物中没有括号和所带电荷数;
C、根据共价化合物中氧原子形成2对共用电子对,氢原子形成1对共用电子对;
D、根据氮气中氮原子形成3对共用电子对,每个原子还剩余2个电子;
解答:解:A、氧化钠为离子化合物,由钠离子与氧离子构成,钠离子不能合并,电子式为

,故A错误;
B、硫化氢为共价化合物,不存在离子键,硫原子与氢原子之间形成1对共用电子对,电子式为
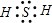
,故B错误;
C、双氧水是氧原子和氢原子之间通过共价键形成的共价化合物,其电子式为
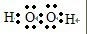
,故C正确;
D、氮原子最外层有5个电子,要达到稳定结构得形成三对共用电子对,电子式为

,故D错误;
故选:C.
点评:本题考查电子式的书写,难度不大,注意未成键的孤对电子对容易忽略.掌握电子式的书写方法即可解答.


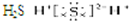

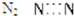
 ,故A错误;
,故A错误;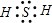 ,故B错误;
,故B错误;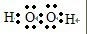 ,故C正确;
,故C正确; ,故D错误;
,故D错误;
