
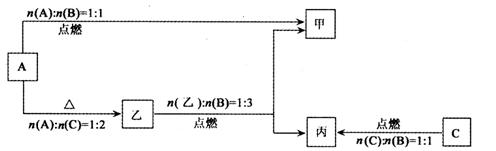
写出C转化为丙的化学方程式__________________________________________________。
(2)在常温下,按下图装配好装置,待内外气体压强不变时,水银柱液面在M处,取下橡皮塞,在玻璃燃烧匙中加入乙,乙在B中充分燃烧,水银柱推向左管。简要回答下列问题:
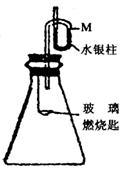
①写出乙燃烧的化学方程式:____________________________________________________。
②水银柱推向左管的原因是:____________________________________________________。
③火焰熄灭后,静置一段时间恢复到原温度,右管水银的位置应该是__________________。
A.仍在M处 B.高于M处 C.低于M处
做出选择后,简要说明理由______________________________________________________。
④用下图所示装置检验乙燃烧的产物
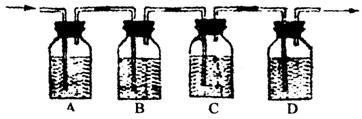
Ⅰ.A、B、C、D中所盛放的药品名称是:
A______________________
B______________________
C______________________
D______________________
Ⅱ.确认产物气体中含丙的现象是________,确认产物中含甲的现象是:_______________。
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源: 题型:
已知:mA=mB+mC,nA(HCl)=nB(HCl)+nC(HCl)。请完成下列问题:
(1)写出短周期ⅠA与ⅡA族元素形成的所有碳酸盐的名称:_______________________。
(2)若以MA、MB和MC分别表示A、B、C的相对分子质量,试写出MA、MB和MC三者的相互关系式________________________________________。
(3)A的正确选择有____________种,其化学式为________________、______________。
(4)若A和B为ⅡA族元素的碳酸盐,C为ⅠA族元素的碳酸盐,则A、B、C的化学式依次是_________________________,mB∶mC=1∶___________(保留2位小数)。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年江苏省苏北三市高三第二次调研测试化学试卷(解析版) 题型:推断题
A、B、C是短周期非金属元素,核电荷数依次增大。A原子外围电子排布为ns2np2,C是地壳中含量最多的元素。D、E是第四周期元素,其中E元素的核电荷数为29。D原子核外未成对电子数在同周期中最多。请用对应的元素符号或化学式填空:
(1)A、B、C的第一电离能由小到大的顺序为 。
(2)分子(AB)2中键与键之间的夹角为180°,并有对称性,每个原子最外层电子数均满足八电子,其结构式为 ,1mol该分子中含有 键的数目为 。
键的数目为 。
(3)基态D原子的外围电子排布式为 。DO2Cl2熔点:-96 .5℃,沸点:117℃,则固态DO2Cl2属于 晶体。
(4)E的氢化物的晶胞结构如图所示,其化学式是 。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com