
”¾ĢāÄæ”æŅŃÖŖA”¢EĪŖ½šŹōµ„ÖŹ£¬BŹĒµ»ĘÉ«·ŪÄ©ĒŅ³£ÓĆÓŚ·Ą¶¾Ćę¾ßÖŠ£¬»Ų“šĻĀĢā”£
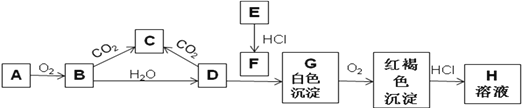
(1)ŹµŃéŹŅÖŠA³£³£±£“ęŌŚŹ¢·Å__________µÄ¹ćæŚĘæÖŠ£¬AŃęÉ«·“Ó¦ĪŖ__________É«”£
(2)Š“³öB×Ŗ±ä³ÉCµÄ»Æѧ·½³ĢŹ½_______________________”£øĆ·“Ó¦ÖŠŃõ»Æ¼ĮŹĒ_________£¬»¹Ō¼ĮŹĒ___________£¬0.1molB²ĪÓėøĆ·“Ó¦£¬×ŖŅʵē×ÓµÄøöŹżĪŖ_________ ”£
(3)Š“³öDÓėF·“Ӧɜ³ÉGµÄĄė×Ó·½³ĢŹ½£ŗ____________________________________________”£
(4)ĆčŹöHČÜŅŗÖŠ½šŹōŃōĄė×ӵďµŃéŹŅ¼ģŃé·½·Ø______________________________________£»ĘäÉę¼°µ½µÄĄė×Ó·“Ó¦·½³ĢŹ½ĪŖ£ŗ_________________________________”£
”¾“š°ø”æ ĆŗÓĶ »Ę 2Na2O2 + 2CO2 = 2Na2CO3 + O2 Na2O2 Na2O2 0.1NA Fe2++2OH-=Fe(OH)2”ż Č”ŹŹĮæ“ż¼ģČÜŅŗÉŁŠķÓŚŹŌ¹ÜÖŠ£¬µĪ¼Ó¼øµĪKSCNČÜŅŗ£¬ČōČÜŅŗ³Ź£ØŃŖ£©ŗģÉ«£¬ŌņÖ¤Ć÷ŗ¬Fe3+ Fe3+ + 3SCN- = Fe(SCN)3£Ø»ņÕߣŗČ”ŹŹĮæ“ż¼ģČÜŅŗÉŁŠķÓŚŹŌ¹ÜÖŠ£¬µĪ¼Ó¼øµĪNaOHČÜŅŗ£¬Čō³öĻÖŗģŗÖÉ«³Įµķ£¬ŌņÖ¤Ć÷ŗ¬Fe3+£¬Fe3+ + 3OH- = Fe(OH)3”ż£©
”¾½āĪö”æŅŃÖŖA”¢EĪŖ½šŹōµ„ÖŹ£¬BŹĒµ»ĘÉ«·ŪÄ©ĒŅ³£ÓĆÓŚ·Ą¶¾Ćę¾ßÖŠ£¬Ņņ“ĖBŹĒ¹żŃõ»ÆÄĘ£¬AŹĒÄĘ£¬¹żŃõ»ÆÄĘÓėCO2·“Ӧɜ³ÉĢ¼ĖįÄĘŗĶŃõĘų£¬ŌņCŹĒĢ¼ĖįÄĘ£¬¹żŃõ»ÆÄĘŗĶĖ®·“Ӧɜ³ÉĒāŃõ»ÆÄĘŗĶŃõĘų£¬ŌņDŹĒĒāŃõ»ÆÄĘ”£°×É«³ĮµķGÄÜ×Ŗ»ÆĪŖŗģŗÖÉ«³Įµķ£¬ŌņGŹĒĒāŃõ»ÆŃĒĢś£¬ĖłŅŌEŹĒĢś£¬FŹĒĀČ»ÆŃĒĢś£¬HŹĒĀČ»ÆĢś”£
£Ø1£©ŹµŃéŹŅÖŠÄĘ³£³£±£“ęŌŚŹ¢·ÅĆŗÓĶµÄ¹ćæŚĘæÖŠ£¬ÄĘŃęÉ«·“Ó¦ĪŖ»ĘÉ«”££Ø2£©¹żŃõ»ÆÄĘÓėCO2·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ2Na2O2+2CO2=2Na2CO3+O2£¬¹żŃõ»ÆÄĘÖŠŃõŌŖĖŲ»ÆŗĻ¼Ū“Ó£1¼Ū²æ·ÖÉżøßµ½0¼Ū”¢²æ·Ö½µµĶµ½£2¼Ū£¬¹żŃõ»ÆÄĘ¼ČŹĒŃõ»Æ¼Į£¬Ņ²ŹĒ»¹Ō¼Į”£0.1mol¹żŃõ»ÆÄĘ²ĪÓėøĆ·“Ó¦£¬×ŖŅʵē×ÓµÄøöŹżĪŖ0.1NA”££Ø3£©ĒāŃõ»ÆÄĘÓėĀČ»ÆŃĒĢś·“Ӧɜ³ÉĒāŃõ»ÆŃĒĢśµÄĄė×Ó·½³ĢŹ½ĪŖFe2++2OH-=Fe(OH)2”ż”££Ø4£©Ņ»°ćÓĆKSCNČÜŅŗ¼ģŃéĢśĄė×Ó£¬¼“¼ģŃéHČÜŅŗÖŠ½šŹōŃōĄė×ӵďµŃé·½·ØŹĒČ”ŹŹĮæ“ż¼ģČÜŅŗÉŁŠķÓŚŹŌ¹ÜÖŠ£¬µĪ¼Ó¼øµĪKSCNČÜŅŗ£¬ČōČÜŅŗ³Ź£ØŃŖ£©ŗģÉ«£¬ŌņÖ¤Ć÷ŗ¬Fe3+£¬·“Ó¦µÄĄė×Ó·“Ó¦·½³ĢŹ½ĪŖFe3++3SCN- =Fe(SCN)3”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĪļÖŹ£¬¶¼ÄÜÓėNa·“Ó¦·Å³öH2£¬Ęä²śÉśH2µÄĖŁĀŹÅÅĮŠĖ³ŠņÕżČ·µÄŹĒ
¢ŁC2H5OH””¢ŚCH3COOH(aq)””¢ŪNaOH(aq)
A. ¢Ł>¢Ś>¢ŪB. ¢Ś>¢Ł>¢ŪC. ¢Ū>¢Ł>¢ŚD. ¢Ś>¢Ū>¢Ł
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ¼×ŹĒŅ»ÖÖæÉÓĆÓŚ¾»Ė®ŗĶÅņ»ÆŹ³Ę·µÄŃĪ£¬ÓÉA”¢B”¢C”¢D”¢EĪåÖÖ¶ĢÖÜĘŚŌŖĖŲ×é³É£®¼×ČÜÓŚĖ®ŗóæɵēĄė³öČżÖÖĄė×Ó£¬ĘäÖŠŅ»ÖÖŹĒÓÉA”¢BŠĪ³ÉµÄ10µē×ÓŃōĄė×Ó£®AŌŖĖŲŌ×ÓŗĖÄŚÖŹ×ÓŹż±ČEµÄÉŁl£¬D”¢EĶ¬Ö÷×壮ijĶ¬Ń§ĪŖĢ½¾æ¼×µÄ×é³É¶ų½ųŠŠČēĻĀŹµŃé£ŗ ¢ŁČ”mg¼×µÄ¾§ĢåČÜÓŚÕōĮóĖ®£¬Åä³É500mLČÜŅŗ£»
¢ŚČ”ÉŁĮæ¼×ČÜŅŗÓŚŹŌ¹ÜÖŠ£¬ÖšµĪµĪČėBa£ØOH£©2ČÜŅŗ£¬Éś³É³ĮµķµÄĪļÖŹµÄĮæÓėµĪČėBa£ØOH£©2ČÜŅŗĢå»żµÄ¹ŲĻµČēĶ¼ĖłŹ¾£»
¢ŪČ”20mL¼×ČÜŅŗÓŚŹŌ¹ÜÖŠ£¬¼ÓČė¹żĮæNaOHČÜŅŗŗó¼ÓČČ²¢ŹÕ¼Æ²śÉśµÄĘųĢå£¬Č»ŗóÕŪĖć³É±ź×¼×“æöĻĀµÄĢå»żĪŖ224mL£®
»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©DŌŚŌŖĖŲÖÜĘŚ±ķÖŠµÄĪ»ÖĆĪŖ £®
£Ø2£©¾²ā¶Ø¾§Ģå¼×µÄĦ¶ūÖŹĮæĪŖ453gmol©1 £¬ ĘäÖŠŃōĄė×ÓŗĶŅõĄė×ÓĪļÖŹµÄĮæÖ®±ČĪŖ1£ŗ1£® Ōņ¾§Ģå¼×µÄ»ÆѧŹ½ĪŖ £®
£Ø3£©Ķ¼ĻóÖŠV£ØOa£©£ŗV£Øab£©£ŗV£Øbc£©= £®
£Ø4£©Š“³öab¶Ī·¢Éś·“Ó¦µÄĄė×Ó·½³ĢŹ½£ŗ £®
£Ø5£©Åä³ÉµÄ¼×ČÜŅŗĪļÖŹµÄĮæÅØ¶ČŹĒ £®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ£Ø1£©¢ŁCu ¢ŚCO2 ¢ŪH2SO3¢ÜH2O¢ŻŅŗĢ¬HCl ¢ŽH2SO4¢ßBa£ØOH£©2 ¢ąNaCl ¢įÕįĢĒ ¢āNaOHČÜŅŗ
ÉĻŹöĪļÖŹÖŠŹōÓŚµē½āÖŹµÄŹĒ______________£¬ŹōÓŚ·Ēµē½āÖŹµÄŹĒ________£¬Äܵ¼µēµÄŹĒ_________”£ £ØĢīŠņŗÅ£¬±ŲŠėĢīČ«£¬·ńŌņ²»µĆ·Ö£©
£Ø2£©Óė16gŃõĘųĖłŗ¬Ō×Ó×ÜŹżĻąĶ¬µÄ°±ĘųŹĒ_________________g”£
£Ø3£©ŅŃÖŖŹµŃéŹŅÖĘČ”ĀČĘųµÄ·“Ó¦ŌĄķĪŖMnO2+4HCl£ØÅØ£©![]() MnCl2+Cl2”ü+2H2O
MnCl2+Cl2ӟ+2H2O
¢ŁøĆ·“Ó¦ÖŠŃõ»Æ¼ĮŗĶ»¹Ō¼ĮµÄĪļÖŹµÄĮæÖ®±ČĪŖ________
¢Śµ±2 mol MnO2²Ī¼Ó·“Ó¦Ź±×ŖŅʵē×Ó______mol
¢Ūµ±×ŖŅĘ1 molµē×ÓŹ±ÄÜÉś³É±ź×¼×“æöĻĀµÄCl2______L
¢ÜÅØŃĪĖįŌŚ·“Ó¦ÖŠĻŌŹ¾³öĄ“µÄŠŌÖŹŹĒ______£ØĢī×ÖÄø£©
a.»¹ŌŠŌ b.ĖįŠŌ c.Ńõ»ÆŠŌ d. »Ó·¢ŠŌ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æNA±ķŹ¾°¢·ü¼ÓµĀĀŽ³£ŹżÖµ£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø £©
A. 18gĖ®Ėłŗ¬µē×ÓŹżĪŖNA B. 14gCOŗĶN2µÄ»ģŗĻĘųĢåĖłŗ¬·Ö×ÓŹżĪŖNA
C. 16gO2ŗĶO3µÄ»ģŗĻĘųĢåĖłŗ¬ÖŹ×ÓŹżĪŖ8NA D. 58.5gNaClĖłŗ¬µÄĄė×ÓŹżĪŖNA
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĶ¼Ź¾Óė¶ŌÓ¦µÄŠšŹöĻą·ūµÄŹĒ£Ø £©
A.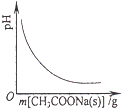 ĻņCH3COOHČÜŅŗÖŠÖš²½¼ÓČėCH3COONa¹ĢĢåŗó£¬ČÜŅŗpHµÄ±ä»Æ
ĻņCH3COOHČÜŅŗÖŠÖš²½¼ÓČėCH3COONa¹ĢĢåŗó£¬ČÜŅŗpHµÄ±ä»Æ
B.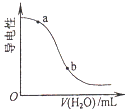 ĻņCH3COOHČÜŅŗÖŠ¼ÓĖ®Ź±ČÜŅŗµÄµ¼µēŠŌ±ä»Æ£¬ŌņCH3COOHČÜŅŗµÄpH£ŗa£¾b
ĻņCH3COOHČÜŅŗÖŠ¼ÓĖ®Ź±ČÜŅŗµÄµ¼µēŠŌ±ä»Æ£¬ŌņCH3COOHČÜŅŗµÄpH£ŗa£¾b
C.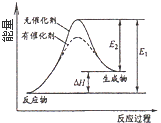 “߻ƼĮÄÜøıä»Æѧ·“Ó¦µÄģŹ±ä
“߻ƼĮÄÜøıä»Æѧ·“Ó¦µÄģŹ±ä
D.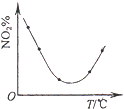 µČĮæNO2ŌŚČŻ»żĻąĶ¬µÄŗćČŻĆܱÕČŻĘ÷ÖŠ£¬²»Ķ¬ĪĀ¶ČĻĀ·Ö±š·¢Éś·“Ó¦£ŗ2NO2£Øg£©N2O4£Øg£©£¬ĻąĶ¬Ź±¼äŗó²āµĆNO2ŗ¬ĮæµÄĒśĻߣ¬ŌņøĆ·“Ó¦µÄ”÷H£¼0
µČĮæNO2ŌŚČŻ»żĻąĶ¬µÄŗćČŻĆܱÕČŻĘ÷ÖŠ£¬²»Ķ¬ĪĀ¶ČĻĀ·Ö±š·¢Éś·“Ó¦£ŗ2NO2£Øg£©N2O4£Øg£©£¬ĻąĶ¬Ź±¼äŗó²āµĆNO2ŗ¬ĮæµÄĒśĻߣ¬ŌņøĆ·“Ó¦µÄ”÷H£¼0
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÄ³Ń§ÉśÓĆ0.4000mol/L NaOHČÜŅŗµĪ¶ØĪ“ÖŖÅØ¶ČµÄŃĪĖįČÜŅŗ£¬Ęä²Ł×÷æÉ·Ö½āĪŖČēĻĀ¼ø²½£ŗ
£ØA£©ÓƱź×¼ČÜŅŗČóĻ“µĪ¶Ø¹Ü2©3“Ī
£ØB£©Č”±ź×¼NaOHČÜŅŗ×¢Čė¼īŹ½µĪ¶Ø¹ÜÖĮ0æĢ¶ČŅŌÉĻ2©3cm
£ØC£©°ŃŹ¢ÓŠ±ź×¼ČÜŅŗµÄ¼īŹ½µĪ¶Ø¹Ü¹Ģ¶ØŗĆ£¬µ÷½ŚŅŗĆęŹ¹µĪ¶Ø¹Ü¼ā×ģ³äĀśČÜŅŗ
£ØD£©µ÷½ŚŅŗĆęÖĮ0»ņ0æĢ¶ČŅŌĻĀ£¬¼ĒĻĀ¶ĮŹż
£ØE£©ŅĘČ”10.00mL“ż²āµÄŃĪĖįČÜŅŗ×¢Čė½ą¾»µÄ׶ŠĪĘ棬²¢¼ÓČė2©3µĪ·ÓĢŖ
£ØF£©ŌŚ×¶ŠĪĘæĻĀµęŅ»ÕÅ°×Ö½£¬ÓƱź×¼NaOHČÜŅŗµĪ¶ØÖĮÖÕµć£¬¼ĒĻĀµĪ¶Ø¹ÜŅŗĆęµÄæĢ¶Č
Ķź³ÉŅŌĻĀĢīæÕ£ŗ
£Ø1£©ÅÅČ„¼īŹ½µĪ¶Ø¹ÜÖŠĘųÅŻµÄ·½·ØÓ¦²ÉÓĆČēĶ¼µÄ²Ł×÷£¬Č»ŗóĒįĒį¼·Ń¹²£Į§ĒņŹ¹¼ā×ģ²æ·Ö³äĀś¼īŅŗ£®
£Ø2£©E²Ł×÷ÖŠŌŚ×¶ŠĪĘæĻĀµęŅ»ÕÅ°×Ö½µÄ×÷ÓĆŹĒ
£Ø3£©ŹµŃéÖŠ£¬ÓĆ×óŹÖæŲÖĘ£ØĢīŅĒĘ÷¼°Ćū³Ę£©£¬ŃŪ¾¦Ó¦×¢ŹÓ £¬ Ö±ÖĮµĪ¶ØÖÕµć£®
£Ø4£©¼ø“ĪµĪ¶ØĻūŗÄNaOHČÜŅŗµÄĢå»żČē±ķ£ŗ
ŹµŃéŠņŗÅ | 1 | 2 | 3 | 4 |
ĻūŗÄNaOHČÜŅŗµÄĢå»ż£ØmL£© | 20.05 | 20.00 | 18.80 | 19.95 |
ŌņøĆŃĪĖįČÜŅŗµÄ×¼Č·ÅضČĪŖ £® £Ø±£ĮōŠ”Źżµćŗó4Ī»£©
£Ø5£©ÓƱź×¼µÄNaOHµĪ¶ØĪ“ÖŖÅØ¶ČµÄŃĪĖį£¬Ń”ÓĆ·ÓĢŖĪŖÖøŹ¾¼Į£¬Ōģ³É²ā¶Ø½į¹ūĘ«øßµÄŌŅņæÉÄÜŹĒ£ŗ £Ø“ķєȫæŪ£©
A.µĪ¶ØÖÕµć¶ĮŹżŹ±£¬ø©ŹÓµĪ¶Ø¹ÜµÄæĢ¶Č£¬ĘäĖü²Ł×÷¾łÕżČ·
B.Ź¢×°Ī“ÖŖŅŗµÄ׶ŠĪĘæÓĆÕōĮóĖ®Ļ“¹ż£¬Ī“ÓĆ“ż²āŅŗČóĻ“
C.µĪ¶Øµ½ÖÕµć¶ĮŹżŹ±·¢ĻÖµĪ¶Ø¹Ü¼ā×ģ“¦Šü¹ŅŅ»µĪČÜŅŗ
D.Ī“ÓƱź×¼ŅŗČóĻ“¼īŹ½µĪ¶Ø¹Ü
E.¼īŹ½µĪ¶Ø¹ÜµĪ¶ØĒ°ĪŽĘųÅŻ£¬µĪ¶Øŗó¼ā×ģ²æ·ÖÓŠĘųÅŻ£®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĮņ»ÆÄĘÖ÷ŅŖÓĆӌʤøļ”¢Ć«·Ä”¢øßµµÖ½ÕÅ”¢Č¾ĮĻµČŠŠŅµ£®Éś²śĮņ»ÆÄĘ“ó¶ą²ÉÓĆĪŽĖ®Ć¢Ļõ£ØNa2SO4£©©Ģæ·Ū»¹Ō·Ø£¬ĘäĮ÷³ĢŹ¾ŅāĶ¼ČēĶ¼1£ŗ 
£Ø1£©ÉĻŹöĮ÷³ĢÖŠ”°¼ī½ž”±ŗó£¬ĪļÖŹA±ŲŠė¾¹ż£ØĢīŠ“²Ł×÷Ćū³Ę£©“¦Ąķŗ󣬷½æÉ”°ģŃÉÕ”±£»ČōģŃÉÕĖłµĆĘųĢåĪŖµČĪļÖŹµÄĮæµÄCOŗĶCO2 £¬ Š“³öģŃÉÕŹ±·¢ÉśµÄ×ܵĻÆѧ·“Ó¦·½³ĢŹ½ĪŖ £®
£Ø2£©ÉĻŹöĮ÷³ĢÖŠ²ÉÓĆĻ”¼īŅŗ±ČÓĆČČĖ®øüŗĆ£¬ĄķÓÉŹĒ £®
£Ø3£©Č”Įņ»ÆÄĘ¾§Ģå£Øŗ¬ÉŁĮæNaOH£©¼ÓČėµ½ĮņĖįĶČÜŅŗÖŠ£¬³ä·Ö½Į°č£®Čō·“Ó¦ŗó²āµĆČÜŅŗµÄpH=4£¬Ōņ“ĖŹ±ČÜŅŗÖŠc£Ø S2©£©= £® £ØŅŃÖŖ£ŗ³£ĪĀŹ±CuS”¢Cu£ØOH£©2µÄKsp·Ö±šĪŖ8.8”Į10©36”¢2.2”Į10©20£©
£Ø4£©¢ŁĘ¤øļ¹¤Ņµ·ĻĖ®ÖŠµÄ¹Æ³£ÓĆĮņ»ÆÄĘ³żČ„£¬¹ÆµÄČ„³żĀŹÓėČÜŅŗµÄpHŗĶx£Øx“ś±ķĮņ»ÆÄʵďµ¼ŹÓĆĮæÓėĄķĀŪÓĆĮæµÄ±ČÖµ£©ÓŠ¹Ų£ØČēĶ¼2ĖłŹ¾£©£®ĪŖŹ¹³ż¹ÆŠ§¹ū×ī¼Ń£¬Ó¦æŲÖʵÄĢõ¼žŹĒ”¢ £® ¢ŚÄ³Ć«·Ä³§·ĻĖ®ÖŠŗ¬0.001 molL©1µÄĮņ»ÆÄĘ£¬ÓėÖ½ÕÅĘÆ°×ŗóµÄ·ĻĖ®£Øŗ¬0.002 molL©1 NaClO£©°“1£ŗ2µÄĢå»ż±Č»ģŗĻ£¬ÄÜĶ¬Ź±½ĻŗĆ“¦ĄķĮ½ÖÖ·ĻĖ®£¬“¦ĄķŗóµÄ·ĻĖ®ÖŠĖłŗ¬µÄÖ÷ŅŖŅõĄė×ÓÓŠ £® 
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÓĆNA±ķŹ¾°¢·ü¼ÓµĀĀŽ³£Źż£¬ĻĀĮŠŠšŹöÕżČ·µÄŹĒ
A. ±ź×¼×“æöĻĀ£¬22.4 L H2Oŗ¬ÓŠµÄ·Ö×ÓŹżĪŖNA
B. ³£ĪĀ³£Ń¹ĻĀ£¬1.06 g Na2CO3ČÜÓŚĖ®ŗ¬ÓŠµÄNa£«Ąė×ÓŹżĪŖ0.02 NA
C. Ķس£×“æöĻĀ£¬NAøöCO2·Ö×ÓÕ¼ÓŠµÄĢå»żĪŖ22.4 L
D. ĪļÖŹµÄĮæÅضČĪŖ0.5 mol/LµÄMgCl2ČÜŅŗÖŠ£¬ŗ¬ÓŠCl£øöŹżĪŖNA
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com