
| A. | 完全反应后不可能有O2剩余 | |
| B. | 原混合气体中C2H4与C2H2的体积共为1.9L | |
| C. | 完全反应后生成水的质量为9 g | |
| D. | 原混合气体中CO与CH4的体积之比一定为1:1 |
分析 A.用极值法判断,当完全为乙烯时消耗氧气体积最大,据此判断氧气是否过量;
B.根据生成二氧化碳的体积判断乙烯和乙炔的总体积;
C.题中数据无法判断甲烷、乙烯和乙炔的体积,则无法计算水的物质的量、质量;
D.能够计算出CO和甲烷的总体积,但是无法计算二者的具体体积.
解答 解:A.5.6L由CO、CH4、C2H4、C2H2完全燃烧,当完全为乙烯时消耗氧气体积最大,最大体积为:5.6L×$\frac{5}{2}$=14L,所以反应后氧气有剩余,故A错误;
B.根据C原子守恒,二氧化碳比原气体增大的体积即为乙烯和乙炔的体积,则生成二氧化碳体积比混合物体积增大了:7.5L-5.6L=1.9L,所以乙烯和乙炔的总体积为1.9L,故B正确;
C.题干信息无法判断CH4、C2H4、C2H2的体积,则无法计算反应后生成水的物质的量,故C错误;
D.根据B可知,混合气体中CO和甲烷的总体积为:5.6L-1.9L=3.7L,但是题中数据无法计算一氧化碳和甲烷的具体体积,故D错误;
故选B.
点评 本题考查了混合物反应的计算,题目难度中等,明确掌握极值法、差量法在化学计算中的应用为解答关键,试题培养了学生的分析、理解能力及化学计算能力.


 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案科目:高中化学 来源: 题型:解答题
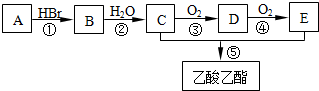
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
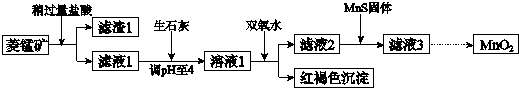
| Mn(OH)2 | Fe(OH)2 | Fe(OH)3 | Cu(OH)2 | |
| 开始沉淀时 | 8.3 | 6.3 | 2.7 | 4.7 |
| 完全沉淀时 | 9.8 | 8.3 | 3.7 | 6.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 原子晶体的熔点一定比分子晶体高 | |
| B. | SO2和SO3均是非极性分子 | |
| C. | PCl3分子中P-Cl的键角小于109°28? | |
| D. | 晶体中有阳离子必有阴离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ②④ | C. | ③④ | D. | ①② |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3CHO | B. | CH3COOC2H5 | C. | CH3COOH | D. | CH3CH2OH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙醇、甲苯、硝基苯 | B. | 苯、苯酚、己烯 | ||
| C. | 苯、甲苯、环己烷 | D. | 苯酚、硫氰化钾溶液、氢氧化钠溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
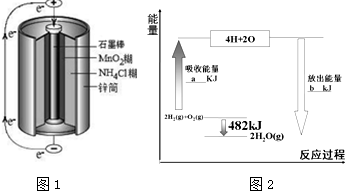 按要求回答下列各题:
按要求回答下列各题:
 ;第三周期元素中,形成简单离子半径最小的是Al3+(填离子符号)
;第三周期元素中,形成简单离子半径最小的是Al3+(填离子符号)| 共价键 | H-H | O=O | H-O |
| 键能/kJ•mol-1 | 436 | 498 | X |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 是碳元素的一种同素异形体 | B. | 是碳元素的一种同位素原子 | ||
| C. | 全部由12C组成 | D. | 能溶于水 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com