
| A£® | ¼×»ł£ŗ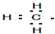 | B£® | CaC2£ŗ | C£® | NH4+£ŗ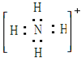 | D£® | ĀČ·Ā£ŗ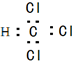 |
·ÖĪö Ź×ĻČÅŠ¶ĻĪ¢Į£µÄĄąŠĶ£¬Ąė×Ó»ÆŗĻĪļŅõĄė×Ó£¬ø“ŌÓŃōĄė×ÓÓĆ”°[]”±²¢ŌŚÓŅÉĻ½Ē±ź×¢Ėł“ųµēŗÉ£¬¹²¼Ū»ÆŗĻĪļ²»“ųµēŗÉ£¬×¢Ņāø÷Ō×Ó»ņĄė×ÓĀś×ćĪČ¶Ø½į¹¹£®
½ā“š ½ā£ŗA£®¼×»łÖŠCÓė3øöH¹²ÓĆ3¶Ōµē×Ó¶Ō£¬CµÄ×īĶā²ć4øöµē×Ó£¬¹Ź¼×»łÖŠCµÄ×īĶā²ćĪŖ7øöµē×Ó£¬µē×ÓŹ½ĪŖ £¬¹ŹAÕżČ·£»
£¬¹ŹAÕżČ·£»
B£®CaC2ÓÉCa2+”¢C22-¹¹³É£¬C22-ÖŠĆæøöCŌ×Ó×īĶā²ćĘ½¾łÓŠ5øöµē×Ó£¬øł¾Ż8µē×ÓĪČ¶Ø½į¹¹æÉÖŖ£¬CŌ×ÓÖ®¼äÓ¦ŠĪ³É3¶Ō¹²ÓƵē×Ó¶Ō£¬ĖłŅŌµē×ÓŹ½ĪŖ £¬¹ŹBÕżČ·£»
£¬¹ŹBÕżČ·£»
C£®NH4+ĪŖø“ŌÓŃōĄė×Ó£¬µē×ÓŹ½ÖŠŅŖ“ųµēŗÉ£¬²¢ÓĆ[]£¬µē×ÓŹ½ĪŖ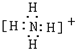 £¬¹ŹCÕżČ·£»
£¬¹ŹCÕżČ·£»
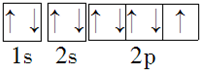
D£®ČżĀČ¼×ĶéÖŠ£¬ClµÄ×īĶā²ćĪŖ8µē×ÓµÄĪČ¶Ø½į¹¹£¬µē×ÓŹ½Ó¦ĪŖ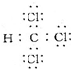 £¬¹ŹD“ķĪó£»
£¬¹ŹD“ķĪó£»
¹ŹŃ”D£®
µćĘĄ ±¾Ģāæ¼²éµē×ÓŹ½µÄŹéŠ“£¬»ÆѧÓĆÓļµÄŹéŠ“ŹĒøßæ¼ČȵćĢāŠĶ£¬ĢāÄæÄŃ¶Č²»“ó£¬×¢Ņāµē×ÓŹ½µÄŹéŠ“·½·Ø£¬×¢ŅāĄė×ÓŗĶŌ×Ó”¢·Ö×Óµē×ÓŹ½µÄ²»Ķ¬£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | äå±½ŗĶĖ® | B£® | ±ū“¼ŗĶŅŅ¶ž“¼ | C£® | µāŗĶŅŅ“¼ | D£® | øŹÓĶŗĶĖ® |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
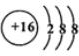 £»
£»²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¶”Ļ© | B£® | ŅŅ“¼ | C£® | ±½·Ó | D£® | ŅŅĖį |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŌŖĖŲŌ×Ó°ė¾¶“󊔳ŹÖÜĘŚŠŌ±ä»Æ | |
| B£® | ŌŖĖŲŌ×ÓĮæŅĄ“ĪµŻŌö | |
| C£® | ŌŖĖŲµÄ×īøßÕż»ÆŗĻ¼Ū³ŹÖÜĘŚŠŌ±ä»Æ | |
| D£® | ŌŖĖŲŌ×Ó×īĶā²ćµē×ÓÅŲ¼³ŹÖÜĘŚŠŌ±ä»Æ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 2H2O2 $\frac{\underline{\;MnO_2\;}}{\;}$ 2H2O+O2”ü | |
| B£® | NH4Cl$\frac{\underline{\;\;”÷\;\;}}{\;}$NH3”ü+HCl”ü | |
| C£® | 2Al+Fe2O3 $\frac{\underline{\;øßĪĀ\;}}{\;}$ 2Fe+Al2O3 | |
| D£® | Cu+2H2SO4£ØÅØ£©$\frac{\underline{\;\;”÷\;\;}}{\;}$CuSO4+SO2”ü+2H2O |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
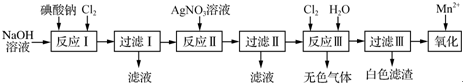
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com