
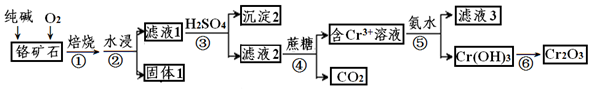
·ÖĪö øõĢśæó£ØÖ÷ŅŖ³É·ÖŹĒCr2O3£¬ŗ¬FeO”¢SiO2µČŌÓÖŹ£©¼ÓČėĢ¼ĖįÄĘģŃÉÕ£¬æÉÉś³ÉNa2CrO4”¢Fe2O3”¢Na2SiO3µČ£¬¼ÓČėĖ®½žČ”£¬µĆµ½¹ĢĢå1ĪŖFe2O3£¬¹żĀĖµĆĀĖŅŗ1ĪŖNa2CrO4”¢Na2SiO3µČ£¬ĻņĀĖŅŗ1ÖŠ¼ÓČėĻ”ĮņĖįµ÷½ŚpHµĆµ½³Įµķ2ĪŖH2SiO3£¬¹żĀĖŗóĻņĀĖŅŗÖŠ¼ÓČėÕįĢĒ£¬ÓĆÕįĢĒ»¹Ō£¬µĆµ½¶žŃõ»ÆĢ¼ŗĶŗ¬ÓŠNa+”¢Cr3+µÄČÜŅŗ£¬ŌŁÓė°±Ė®·“Ó¦£¬ĀĖŅŗ3µÄÖ÷ŅŖČÜÖŹŹĒĮ½ÖÖŃĪĪŖ£ØNH4£©2SO4”¢Na2SO4£¬µĆµ½Cr£ØOH£©3³Įµķ£¬×ĘÉÕ¾ŻCr£ØOH£©3³ĮµķµĆµ½Cr2O3£¬¾Ż“Ė·ÖĪö“šĢā£®
½ā“š ½ā£ŗ£Ø1£©ĪŖĮĖĢįøß·“Ó¦ĖŁĀŹ£¬æÉŅŌŹŹµ±ÉżĪĀ”¢·ŪĖéøõæóŹÆ”¢½Į°čµČ£»
¹Ź“š°øĪŖ£ŗŹŹµ±ÉżĪĀ”¢·ŪĖéøõæóŹÆ”¢½Į°čµČ£»
£Ø2£©øł¾Ż·“Ó¦ÖŠø÷ĪļÖŹµÄŌŖĖŲ»ÆŗĻ¼Ū±ä»ÆæÉÖŖ£¬CrŌŖĖŲ“Ó+3¼Ū±äĪŖ+6¼Ū£¬ŃõŌŖĖŲ“Ó0¼Ū±äĪŖ-2¼Ū£¬øł¾Ż»ÆŗĻ¼ŪÉż½µ·Ø¼°ŌŖĖŲŹŲŗćæÉÅäĘ½»Æѧ·½³ĢŹ½£¬ÓƵ„ĻßĒűķŹ¾µē×Ó×ŖŅʵķ½ĻņĪŖ£ŗ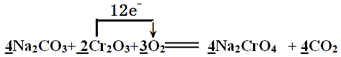 £»
£»
¹Ź“š°øĪŖ£ŗ4£»2£»3£»4£»4£»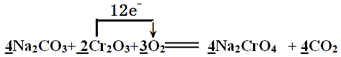 £»
£»
£Ø3£©ĀĖŅŗ1ĪŖNa2CrO4”¢Na2SiO3µČ£¬ĻņĀĖŅŗ1ÖŠ¼ÓČėĻ”ĮņĖįµ÷½ŚpHµĆµ½³Įµķ2ĪŖH2SiO3£»
¹Ź“š°øĪŖ£ŗH2SiO3£»
£Ø4£©·“Ó¦ÖŠCrŌŖĖŲ»ÆŗĻ¼ŪÓÉ+6¼Ū½µµĶĪŖ+3¼Ū£¬CŌŖĖŲÓÉ0¼ŪÉżøßĪŖ+4£¬øł¾Żµē×Ó×ŖŅĘŹŲŗćŌņ£ŗ6n£ØCr2O72-£©=48n£ØÕįĢĒ£©£¬¹Źn£ØCr2O72-£©£ŗn£ØÕįĢĒ£©=8£ŗ1£»
¹Ź“š°øĪŖ£ŗ8£ŗ1£»
£Ø5£©Cr3+³ĮµķĶźČ«µÄÅضČĪŖ10-5mol/L£¬øł¾ŻKSP[Cr£ØOH£©3]=c£ØCr3+£©”Įc3£ØOH-£©=6.4”Į10-31£¬æÉÖŖc£ØOH-£©=4”Į10-9mol/L£¬Ōņc£ØH+£©=$\frac{1{0}^{-14}}{4”Į1{0}^{-9}}$mol/L=$\frac{1}{4}$”Į10-5mol/L£¬ŌņpH=-lg$\frac{1}{4}$”Į10-5=5.6£»
¹Ź“š°øĪŖ£ŗ5.6£»
£Ø6£©ÓÉ·ÖĪöæÉÖŖĀĖŅŗ3µÄÖ÷ŅŖČÜÖŹŹĒĮ½ÖÖŃĪŹĒ£ØNH4£©2SO4”¢Na2SO4£»
¹Ź“š°øĪŖ£ŗ£ØNH4£©2SO4”¢Na2SO4£»
£Ø7£©½«NaCrO2ČܽāŗóĶØČėCO2µĆµ½øüĪŖ“æ¾»µÄCr£ØOH£©3£¬ŹōÓŚĖ®½ā·“Ó¦£¬»¹Éś³ÉĢ¼ĖįĒāÄĘ£¬·“Ó¦Ąė×Ó·½³ĢŹ½ĪŖ£ŗCrO2-+CO2+2H2O=Cr£ØOH£©3”ż+HCO3-£»
¹Ź“š°øĪŖ£ŗCrO2-+CO2+2H2O=Cr£ØOH£©3”ż+HCO3-£®
µćĘĄ ±¾Ģāæ¼²éĪļÖŹÖʱø¹¤ŅÕĮ÷³Ģ£¬Éę¼°¶Ō²Ł×÷Óė·“Ó¦ŌĄķµÄ·ÖĪöĘĄ¼Ū”¢ĪļÖŹµÄ·ÖĄėĢį“攢ČܶȻżÓŠ¹Ų¼ĘĖć”¢»Æѧ¼ĘĖć¼ĘĖćµČ£¬²ąÖŲӌѧɜ¶ŌŌĄķµÄ·ÖĪöÓ¦ÓĆ¼°¼ĘĖćÄÜĮ¦µÄ漲飬×ŪŗĻŠŌ½ĻĒ棬ĢāÄæÄѶČÖŠµČ£®


 ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø
ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ś¢Ū¢Ü¢Ż | B£® | ¢Ł¢Ū¢Ü¢Ż | C£® | ¢Ł¢Ś¢Ū¢Ü | D£® | ¢Ł¢Ś¢Ü¢Ż |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | pH=2µÄHAČÜŅŗÓėpH=12µÄMOHČÜŅŗČĪŅā±Č»ģŗĻ£ŗc£ØH+£©+c£ØM+ £©=c£ØOH- £©+c£ØA- £© | |
| B£® | 25”ꏱ£¬pH=4.7ÅØ¶Č¾łĪŖ0.1mol•L-1µÄCH3COOH”¢CH3COONa»ģŗĻČÜŅŗÖŠ£ŗ£ØCH3COO-£©+c£ØOH-£©£¾c£ØCH3COOH£©+c£ØH+£© | |
| C£® | ĒāĮņĖįµÄĖįŠŌ±ČĢ¼ĖįČõ£¬ŌņNaHSČÜŅŗÖŠ£ŗc£ØNa+£©£¾c£ØHS-£©£¾c£ØH+£©£¾c£ØOH-£© | |
| D£® | ¢Ł0.2mol•L-1NH4ClČÜŅŗ¢Ś0.1mol•L-1£ØNH4£©2Fe£ØSO4£©2ČÜŅŗ¢Ū0.2mol•L-1NH4HSO4ČÜŅŗ¢Ü0.1mol•L-1£ØNH4£©2CO3ČÜŅŗÖŠ£¬c£ØNH4+ £©“󊔣ŗ¢Ū£¾¢Ś£¾¢Ł£¾¢Ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Y”¢Z×Å»šŹ±¾łæÉÓĆÅŻÄĆš»šĘ÷½ųŠŠĆš»š | |
| B£® | ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦Ė®»ÆĪļµÄ¼īŠŌ£ŗY£¾Z | |
| C£® | Y”¢Z”¢WµÄ¼ņµ„Ąė×Ó¶¼ÄÜ“Ł½ųĖ®µÄµēĄė | |
| D£® | Ō×Ó°ė¾¶ÓÉŠ”µ½“óµÄĖ³Šņ£ŗX£¼W£¼Z£¼Y |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| t/min | 0 | 3 | 10 | 12 |
| n£ØCO£©/mol | 2 | 1 | 0.5 | 0.5 |
| n£ØCH3OH£©/mol | 0 | 1 | 1.5 | 1.5 |
| A£® | ŌŚ0”«3minÄŚ£¬ÓĆH2±ķŹ¾µÄĘ½¾ł·“Ó¦ĖŁĀŹĪŖ0.33mol•L-1•min-1 | |
| B£® | ŌŚøĆĢõ¼žĻĀ£¬ÉĻŹö·“Ó¦µÄĘ½ŗā³£ŹżĪŖ3 | |
| C£® | ·“Ó¦“ļĘ½ŗāŹ±£¬CH3OH £Øg£©µÄĢå»ż·ÖŹżĪŖ50% | |
| D£® | ŅŖŌö“ó·“Ó¦ĖŁĀŹĒŅŌö“ó CH3OH £Øg£©ŌŚ»ģŗĻĪļÖŠµÄĢå»ż·ÖŹż£¬æɲÉÓĆŃ¹ĖõĢå»ż£¬Ōö“óĢåĻµŃ¹ĒæµÄ“ėŹ© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ½«µēŹÆÓėĖ®·“Ó¦²śÉśµÄĘųĢåĻČĶØČėCuSO4ČÜŅŗŌŁĶØČėĖįŠŌKMnO4ČÜŅŗÖŠ£¬ČÜŅŗĶŹÉ«ĖµĆ÷ÓŠŅŅČ²Éś³É | |
| B£® | ij¼ŲŃĪČÜÓŚŃĪĖį£¬²śÉśÄÜŹ¹³ĪĒåŹÆ»ŅĖ®±ä»ė×ĒµÄĪŽÉ«ĘųĢ壬ĖµĆ÷øĆ¼ŲŃĪŹĒK2CO3»ņK2SO3 | |
| C£® | ½«ÅØĮņĖįŗĶŅŅ“¼ČÜŅŗ¹²ČČ²śÉśµÄĘųĢåøÉŌļŗóĶØČėäåµÄĖÄĀČ»ÆĢ¼ČÜŅŗ£¬ČÜŅŗĶŹÉ«£¬ĖµĆ÷ÓŠŅŅĻ©Éś³É | |
| D£® | ½«±½”¢Ņŗä唢Ģś·Ū»ģŗĻĪļ·“Ó¦²śÉśµÄĘųĢåĶØČėµ½AgNO3ČÜŅŗÖŠÓŠµ»ĘÉ«³Įµķ²śÉś£¬²»ÄÜĖµĆ÷ÓŠHBrÉś³É |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¹żĀĖ | B£® | ÕōĮó | C£® | ·ÖŅŗ | D£® | ŻĶČ” |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com