
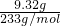 =0.04mol,碳酸钡的质量为29.02g-9.32g=19.7g,故n(BaCO3)=
=0.04mol,碳酸钡的质量为29.02g-9.32g=19.7g,故n(BaCO3)=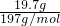 =0.1mol,
=0.1mol, =1mol/L,
=1mol/L, =0.4mol/L,
=0.4mol/L, 计算碳酸钡、硫酸钡的物质的量,
计算碳酸钡、硫酸钡的物质的量, 计算;
计算;

 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
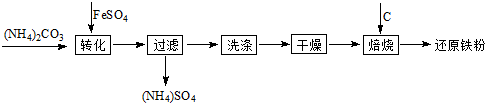
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
 +2H2O
+2H2O查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com